
题目列表(包括答案和解析)
| A.向NH4HCO3溶液中加过量Ca(OH)2溶液:HCO3-+OH-+Ca2+=CaCO3↓+H2O |
B.用惰性电极MgCl2电解水溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
C.向偏铝酸钠溶液中加入少量硫酸氢钠溶液:2AlO2 +H +H +H2O=Al(OH)3↓ +H2O=Al(OH)3↓ |
D.浓盐酸跟二氧化锰混合共热:MnO2+4H +4Cl +4Cl =Mn =Mn +2H2O+2Cl2↑ +2H2O+2Cl2↑ |
下列离子方程式书写正确的是
| A.向NH4HCO3溶液中加过量Ca(OH)2溶液:HCO3-+OH-+Ca2+=CaCO3↓+H2O |
B.用惰性电极MgCl2电解水溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
C.向偏铝酸钠溶液中加入少量硫酸氢钠溶液:2AlO2 +H +H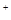 +H2O=Al(OH)3↓ +H2O=Al(OH)3↓ |
D.浓盐酸跟二氧化锰混合共热:MnO2+4H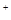 +4Cl +4Cl =Mn =Mn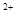 +2H2O+2Cl2↑ +2H2O+2Cl2↑ |
下列反应的离子方程式错误的是
A.向碳酸氢钙溶液中加人过量氢氧化钠
Ca2++2HCO3-+2OH- = CaCO3↓+2H2O+CO32-
B.氢氧化铝与足量盐酸反应 Al(OH)3+3H+ = Al3++3 H2O
C. 金属钠跟水反应 2Na+2H2O==2Na++2OH-+H2↑
D. 浓盐酸跟二氧化锰混合共热 MnO2+4H++4Cl-![]() Mn2++2H2O+2Cl2↑
Mn2++2H2O+2Cl2↑
|
下列反应的离子方程式错误的是 | |
| [ ] | |
A. |
向碳酸氢钙溶液中加人过量氢氧化钠 Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
B. |
氢氧化铝与足量盐酸反应Al(OH)3+3H+=Al3++3H2O |
C. |
金属钠跟水反应2Na+2H2O==2Na++2OH-+H2↑ |
D. |
浓盐酸跟二氧化锰混合共热MnO2+4H++4Cl- |
|
下列离子方程式书写正确的是 | |
| [ ] | |
A. |
碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液 Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
B. |
氯化铝溶液中加入过量氨水Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
C. |
0.1 mol溴化亚铁中滴入含Cl2 0.1 mol氯水: 2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
D. |
浓盐酸跟二氧化锰混合共热MnO2+4H++4Cl- |
1.C 2.C 3.D 4.B 5.B 6.A 7.AD 8.AC 9.BD 10.AC 11.C
12.D 13.AC 14.D 15.B 16.D 17.B 18.B 19.A 20.D 21.D 22.B
23.(1) ;
; ;生成了弱电解质
;生成了弱电解质 ,破坏了
,破坏了 的溶解平衡.
的溶解平衡.
(2)①


②
24.(1) 在溶液中存在
在溶液中存在 的电离,
的电离,

 ,同时还存在
,同时还存在 离子的水解,
离子的水解,

 ,
, 溶液呈弱碱性,说明
溶液呈弱碱性,说明 的水解反应占优势.
的水解反应占优势.
(2) 在溶液中存在着
在溶液中存在着 离子的电离,同时又存在
离子的电离,同时又存在 离子的水解,
离子的水解, 呈弱酸性说明
呈弱酸性说明 离子的电离比水解来得强.
离子的电离比水解来得强.
(3)
25.A: B:
B: C:
C: D:
D: E:
E:
① ②
② ③
③
④
26.(1)粉红 


(2)放出气体,溶液变浑浊,红色加深红

27.(1)溶液变成紫红色,0.25 (2) ,
, w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
28.(1)硫 (2) ;
;
(3) ,可能含有
,可能含有 (4)
(4) 、
、 、
、 、
、 和
和 、
、 和
和
(5) 、
、 、
、
29.解析:①溶液中 被完全沉淀出后,
被完全沉淀出后, 才开始沉淀.图中曲线第二段为平行直线,沉淀总物质的量没有增减.故这段是因
才开始沉淀.图中曲线第二段为平行直线,沉淀总物质的量没有增减.故这段是因 的溶解和
的溶解和 的继续生成导致,且溶解的
的继续生成导致,且溶解的 的物质的量和生成的
的物质的量和生成的 物质的量相等.故加入的物质:
物质的量相等.故加入的物质:
 这段的离子方程式为:
这段的离子方程式为:


②第一段生成的沉淀为 、
、 和
和 ,且B为90 mL时,
,且B为90 mL时, 、
、 恰好沉淀完全.这段反应的离子方程式为:
恰好沉淀完全.这段反应的离子方程式为: ,
,
 ,
,
③图中曲线第三段(100-110 mL),B为100 mL时 恰好沉淀完全.这段中
恰好沉淀完全.这段中 继续溶解,B为110 mL时,沉淀中
继续溶解,B为110 mL时,沉淀中 已完全溶解.这段中溶解了
已完全溶解.这段中溶解了 ,消耗了10 mL NaOH,故
,消耗了10 mL NaOH,故 ,则100 mL时,共加入
,则100 mL时,共加入 为0.1 mol,共生成
为0.1 mol,共生成 ,故A溶液中
,故A溶液中 .这段
.这段 溶解的离子方程式为:
溶解的离子方程式为:
④图中曲线第四段中,沉淀为 、
、 共0.11 mol,则
共0.11 mol,则
 为0.11 mol,A中
为0.11 mol,A中 .
.
⑤第二、三段间共消耗 ,则共溶解的
,则共溶解的 为0.02 mol,则A中
为0.02 mol,则A中 .w.w.w.k.s.5.u.c.o.m
.w.w.w.k.s.5.u.c.o.m
30.(1) ;
;
(2) ;
; ;
; ,
,

(3) ;
; ;
; ,
,
(4) ;
;
(5)
(6)
 www.ks5u.com
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com