
题目列表(包括答案和解析)
| 高温 |
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。完成下列填空:
(1)铝原子核外电子云有 种不同的伸展方向,有 种不同运动状态的电子。
(2)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式。
(3)硅与铝同周期。SiO2是硅酸盐玻璃(Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成Na2O·CaO·6SiO2。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 。
长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为
(4)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:
2Al+4BaO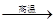 3Ba↑+BaO·Al2O3
3Ba↑+BaO·Al2O3
常温下Al的金属性比Ba的金属性 (选填“强”“弱”)。利用上述方法可制取Ba的主要原因是 。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。完成下列填空:
(1)铝原子核外电子云有 种不同的伸展方向,有 种不同运动状态的电子。
(2)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式。
(3)硅与铝同周期。SiO2是硅酸盐玻璃(Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成Na2O·CaO·6SiO2。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 。
长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为
(4)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:
2Al+4BaO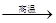 3Ba↑+BaO·Al2O3
3Ba↑+BaO·Al2O3
常温下Al的金属性比Ba的金属性 (选填“强”“弱”)。利用上述方法可制取Ba的主要原因是 。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
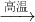 3Ba↑+BaO?Al2O3.常温下Al的金属性比Ba的金属性______(选填“强”“弱”).利用上述方法可制取Ba的主要原因是______.
3Ba↑+BaO?Al2O3.常温下Al的金属性比Ba的金属性______(选填“强”“弱”).利用上述方法可制取Ba的主要原因是______.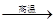 3Ba↑+BaO·Al2O3
3Ba↑+BaO·Al2O3(每题2分)
题号
1
2
3
4
5
6
7
8
9
10
答案
B
D
C
A
A
B
B
B
B
A
题号
11
12
13
14
15
16
17
18
19
20
答案
B
C
A
D
B
D
C
B
C
C
21.(每空1分,共3分)ClO- 和 Cl-; 1
22.(6分,每空2分)(1)Na2SiO3+ CO2+ H2O= H2SiO3↓+ Na2CO3
(2)Na2SiO3+2HCl= H2SiO3↓+ 2NaCl
(3)Na2CO3+2HCl= 2NaCl+ CO2↑+ H2O
23.(4分,每空1分)A:CaBr2;B:AgNO3;C:CuSO4;D:K2CO3。
24.(7分,其中⑴2分,其余每空1分)⑴ ;
沸腾炉
;
沸腾炉
(2)SO3、SO2、O2;C、B、A (3)98%浓硫酸,接触室
25.(8分,每空2分) (1)CO2
(2)Al3++4OH- = AlO2-+ 2H2O
(3)2Al+3CuO 3Cu+Al2O3
3Cu+Al2O3
(4)0.75
26.(每空1分,共7分)
(1)甲 丙 戊
(2)乙 有较多气泡放出的为稀硫酸
(3)丁 浓硫酸不具有挥发性
27.(10分,其中(3)4分,(4)2分,其余每空1分)
(1)乙 亚铁盐在空气中易被氧气氧化 (2) 还原
(3) 2Fe2++H2O2+2H+=2Fe3++2H2O Fe3++3SCN-=Fe(SCN)3 。
(4)再加过量KSCN,如果变血红色,则第二种合理;如果不变色,则第一种合理 (5) 未能测其成分。
28.(7分,其中(1)3分,(2)4分) (1)3分 (2)55.79%
29.(8分)
(2分)(1)Al3+ + 3OH―= Al (OH)3↓;Al (OH)3 + OH―= AlO2―+ 2H2O
(6分)(2)1.5 mol?L―1或3.5 mol?L―1
已知:n (AlCl3)
=  = 0.1mol (1分)
= 0.1mol (1分)
n (Al (OH)3) =  = 0.05mol (1分)
= 0.05mol (1分)
①NaOH溶液不足 Al3+ + 3OH―= Al (OH)3↓
0.15mol 0.05mol
c (NaOH) =  = 1.5 mol?L―1 (2分)
= 1.5 mol?L―1 (2分)
②NaOH溶液过量Al3+ + 3OH―= Al (OH)3↓ Al (OH)3 + OH―= AlO2―+ 2H2O
0.1mol 0.3mol 0.1mol 0.05mol 0.05mol
c (NaOH) =  = 3.5 mol?L―1(2分)
= 3.5 mol?L―1(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com