
题目列表(包括答案和解析)
| ① | ② | ③ | |
| 硫酸溶液体积/mL | 50 | 50 | 50 |
| 称取铁钉质量/g | 5.0 | 6.0 | 7.0 |
| 再投入铜粉质量/g | 1.0 | 1.0 | 1.0 |
| 标准状况下的体积/L | 1.97 | 2.24 | 2.24 |
已知锌能溶解在NaOH溶液中,产生H2。某同学据此设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6 mol·L-1 NaOH溶液中,当石墨棒上不再有气泡产生时,取出铁片用水冲洗、烘干后称量,得质量为m2。下列说法正确的是(双选)( )
A.设锌镀层单侧厚度为h,锌的密度为ρ,则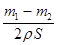 =h
=h
B.锌电极上发生还原反应
C.锌和石墨形成原电池,外电路中电流从锌流向石墨
D.当石墨不再产生气泡时,应立即取出铁皮
| A、一个化学反应是否能在常温下发生与该反应的反应热大小没有必然联系 | B、已知中和热△H=-57.3KJ?mol-1,所以1.00mol?L-1H2SO4与稀NaOH溶液恰好完全反应时放出57.3 kJ的热量 | C、由C(石墨)=C(金刚石)△H=+1.90KJ?mol-1可知,金刚石比石墨稳定 | D、在 101 kPa时,l mol CH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
(11分)某学生在实验室中欲配制480mL 0.26 mol/L NaOH溶液,请帮助该生完成下列实验过程并回答问题:
①称量:用托盘天平称量NaOH固体 g,称量时应将NaOH固体放在 (填实验用品)中,并置于天平的 (填“左”或“右”)盘。
②溶解:加少量水用玻璃棒搅拌溶解,并 。
③转移:将烧杯中的氢氧化钠溶液用玻璃棒引流转移到 中。
④定容:加水至离刻度线1-2cm时,改用胶头滴管滴加至刻度线。
⑤摇匀、装瓶、贴标签。
请回答下列问题:
(1)该生在配制过程中缺少一个实验步骤,这一实验步骤的位置和具体操作是
。
(2)下列操作会使实际配制的溶液浓度偏高的是 。
A.称量前,氢氧化钠固体已潮解 B.称量时,砝码和物品放反了
C.转移时有溶液溅出 D.读数时俯视刻度
一、选择题(共10分)
1、C 2、D 3、C 4、A 5、B
二、选择题(共45分)
6、C 7、C 8、B 9、B 10、C
11、D 12、C 13、B 14、A 15、C
16、D 17、B 18、D 19、C 20、C
三、填空题(共34分)
21、(2分) △H1<△H3<△H2
|