
(2009?泰州模拟)二氧化硫是常用的化工原料,但也是大气的主要污染物.
(1)硫酸生产中,SO
2催化氧化生成SO
3:
2SO
2(g)+O
2(g)
2SO
3(g)
某温度下,将SO
2和O
2按体积比2:1充入密闭容器中,SO
2的平衡转化率(α)与体系总压强(p)的关系如右图所示.根据图示回答下列问题:
①将2.0mol SO
2和1.0mol O
2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa.平衡时c(SO
3)=
0.16
0.16
mol/L;
②达到平衡状态B,O
2的转化率α(O
2)=
0.85
0.85
.
(2)因为SO
2排放造成的环境问题有
b
b
.
a.光化学烟雾 b.酸雨 c.赤潮 d.破坏臭氧层
(3)大气中的SO
2主要源于化石燃料的燃烧和含硫矿石的冶炼.在SO
2污染的治理中湿法石灰石-石膏法脱硫工艺是烟气脱硫技术中最成熟的一种方法.其工艺流程是:烟气经锅炉预热器出来,进入电除尘器除掉大部分粉煤灰烟尘,再经过一个专门的热交换器,然后进入吸收塔,烟气中的SO
2与含有石灰石的浆液进行气液接触,通入空气后生成石膏(CaSO
4?2H
2O),烟气脱硫后排入大气.
①写出湿法石灰石-石膏法脱硫所涉及的化学反应方程式
SO2+CaCO3=CaSO3+CO2
SO2+CaCO3=CaSO3+CO2
,
2CaSO3+O2+4H2O=2(CaSO4?2H2O)
2CaSO3+O2+4H2O=2(CaSO4?2H2O)
.
②烟气在通入石灰石的浆液前通过热交换器的目的是
热能的综合利用、有利于SO2的吸收
热能的综合利用、有利于SO2的吸收
.


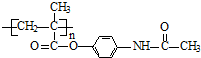 .
.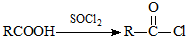

 可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式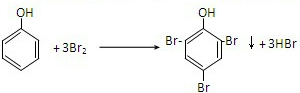







 (2009?泰州模拟)二氧化硫是常用的化工原料,但也是大气的主要污染物.
(2009?泰州模拟)二氧化硫是常用的化工原料,但也是大气的主要污染物.