
题目列表(包括答案和解析)

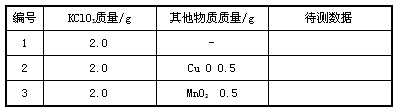


某实验小组欲制取氧化铜,并证明氧化铜能加快氯酸钾的分解,进行如下实验:
Ⅰ.制取氧化铜
①称取2gCuSO4•5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是 (填实验步骤序号)。
(2)步骤、中研磨固体所用仪器的名称是 。
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进
行比较用右图装置进行实验,实验时均以生成25mL气体为准,其它
 可能影响实验的因素均已忽略。相关数据见下表:
可能影响实验的因素均已忽略。相关数据见下表:

(3)上述实验中的“待测数据”指 。
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a. ;
b.检验CuO的化学性质是否改变。
Abc查阅资料后了解,MnO2对KclO3的催化过程由以下三个反应组成,请将第二个反应补充完整。

电解水实验可以确定水的组成。甲、乙、丙三位同学对电解水后液体的酸碱性进行探究。
【提出问题】电解水后的液体一定呈中性吗?
【查阅资料】
图Ⅰ所示装置可用于电解水实验;
硫酸钠可增强水的导电性,硫酸钠溶液呈中性。
【实验与讨论】
三位同学分别向U形管中加入含有酚酞的硫酸钠溶液,接通直流电,观察现象,点解一段时间后,断开电源。
(1) 实验中发现试管①电极附近的溶液迅速变红,管②电极附
(2) 近的溶液任为无色,乙同学用pH试纸测定管②电极附近的溶液,pH小于7。
说明试管①电极附近的溶液呈 性,管②附近的溶液呈 (选填“酸”、“碱”或“中”)性。
(2)甲同学将实验后U形管中的溶液按图Ⅱ所示倒入烧杯中,
发现红色立刻消失。
乙同学、丙同学将试验后U形管中的溶液按图Ⅲ所示分别倒入烧杯中,发现红色不完全消失。
经讨论与分析,乙、丙同学的试验中溶液的红色不消失,原因可能是酸 。
(3)甲、乙、丙同学分别用蒸馏水洗涤U形管、碳棒等,再将洗涤液倒入自己实验的烧杯中,观察现象:
甲同学的溶液仍为无色。
乙同学的溶液中红色仍不消失。
![]() 丙同学的溶液中红色 。
丙同学的溶液中红色 。
(4)甲、乙、丙同学分析了实验现象,为确证溶液的酸碱性,又进行下列实验:
甲同学用 来测定溶液,原因是 。
乙同学向溶液中滴加 ,使溶液中红色刚好褪去。因为造成(3)中溶液的红色仍不消失的原因是 。
【解释与结论】
用硫酸钠增强水的导电性时,点解后溶液混合均匀,呈中性。
【交流与反思】
甲同学取55g质量分数为2%的硫酸钠溶液进行电解,消耗了5g水后,则电解后硫酸钠溶液的质量分数为 。
甲同学的老师上课时用NaOH增强水的导电性,点解后溶液的碱性 。
乙同学的老师上课时用H2SO4增强水的导电性,点解后溶液的酸性 。


某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞溶液变红,Na2CO3溶液也能使酚酞溶液变红。碱溶液可以使酚酞溶液变红,是因为碱在水溶液中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞溶液变红呢?他们设计了下图3个实验,请你和他们一起探究。
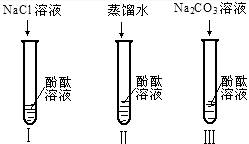
⑴实验Ⅰ可以证明 。
⑵实验Ⅱ加入蒸馏水的目的是 。小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是 。
⑶实验Ⅲ滴入K2CO3溶液,振荡,酚酞溶液变红,向变红后的溶液中再逐渐滴入过量的CaCl2溶液,红色逐渐消失,同时还观察到 现象。由实验Ⅰ、Ⅱ、Ⅲ得出结论: CO32-可以使酚酞溶液变红。
⑷小组同学在与老师交流上述结论时,老师说:“其实Na2CO3溶液能使酚酞溶液变红也是由于溶液中存在OH-。”你认为Na2CO3溶液存在OH-的原因是 。
某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞溶液变红,Na2CO3溶液 也能使酚酞溶液变红。碱溶液可以
也能使酚酞溶液变红。碱溶液可以 使酚酞溶液变红,是因为碱在水溶液中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞溶液变红呢?他们设计了下图3个实验,请你和他们一起探究。
使酚酞溶液变红,是因为碱在水溶液中解离出了OH-,那么Na2CO3溶液中究竟是哪种粒子可以使酚酞溶液变红呢?他们设计了下图3个实验,请你和他们一起探究。
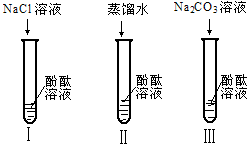
(1)实验Ⅰ可以证明 。
(2)实验Ⅱ加入蒸馏水的目的是 。小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是 。
(3)实验Ⅲ滴入Na2CO3溶液,振荡,酚酞溶液变红,向变红后的溶液中再逐渐滴入过量的CaCl2溶液,红色逐渐消失,同时还观察到 现象。由实 验Ⅰ、Ⅱ、Ⅲ得出结论: CO32-可以使酚酞溶液变红。
验Ⅰ、Ⅱ、Ⅲ得出结论: CO32-可以使酚酞溶液变红。
(4)小组同学在与老师交流上述结论时,老师说:“其 实Na2CO3溶液能使酚酞溶液变红也是由于溶液中存在OH-。”你认为Na2CO3溶液存在OH-的原因是 。
实Na2CO3溶液能使酚酞溶液变红也是由于溶液中存在OH-。”你认为Na2CO3溶液存在OH-的原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com