Μ·―ßΈο÷ ÷°ΦδΒΡΖ¥”ΠΑ¬ΟνΈό«νΘ°‘Ύ“Μ¥ΈΜ·―ßΧΫΨΩΜνΕ·÷–Θ§Ά§―ßΟ«¥”≤ΜΆ§Ϋ«Ε»Ε‘œΓΝρΥα”κ«β―θΜ·ΡΤ»ή“ΚΒΡΖ¥”ΠΫχ––ΝΥΧΫΨΩΘ§«κΡψ≤Έ”κ≤ΔΧν–¥“‘œ¬Ω’ΑΉΘ°
Θ®1Θ©»γΚΈ”Ο Β―ι―ι÷ΛœΓΝρΥα”κ«β―θΜ·ΡΤ»ή“ΚΖΔ…ζΝΥΖ¥”Π
ΒΎ“ΜΉιΆ§―ß…ηΦΤΝΥ Β―ιΖΫΑΗ“ΜΘΚ
| Β―ι≤Ϋ÷η |
Β―ιœ÷œσ |
Ϋα¬έ |
| œ»”ΟPH ‘÷Ϋ≤βΕ®œΓΝρΥαΒΡPHΘ§‘Ό÷πΫΞΒΈΦ”«β―θΜ·ΡΤ»ή“ΚΘ§≤Δ≤ΜΕœ’ώΒ¥Θ§Ά§ ±≤βΕ®ΜλΚœ“ΚΒΡPHΘ° |
PH÷πΫΞ±δ¥σΘ§
ΉνΚσ PHΓί7 |
œΓΝρΥα”κ«β―θΜ·ΡΤ»ή“ΚΡήΖΔ…ζΖ¥”Π |
ΔΌ«κΡψΖ÷Έω…œ ωΖΫΑΗ÷–ΈΣ ≤Ο¥«ΩΒς÷Μ”–≤βΒΟΒΡPHΓί7≤≈Ρή÷ΛΟςΖ¥”ΠΖΔ…ζΝΥΘΩ
≈≈≥ΐ“ρ«β―θΜ·ΡΤ»ή“ΚΒΡΦ”»κΘ§œΓ ΆΝρΥαΕχ“ΐΤπPH±δ¥σ
≈≈≥ΐ“ρ«β―θΜ·ΡΤ»ή“ΚΒΡΦ”»κΘ§œΓ ΆΝρΥαΕχ“ΐΤπPH±δ¥σ
Μρ÷Μ”–PHΓί7≤≈ΡήΥΒΟςΝρΥα“―Ψ≠Ζ¥”ΠΒτΝΥ
Μρ÷Μ”–PHΓί7≤≈ΡήΥΒΟςΝρΥα“―Ψ≠Ζ¥”ΠΒτΝΥ
Θ°
ΔΎ–¥≥ωœΓΝρΥα”κ«β―θΜ·ΡΤ»ή“ΚΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ
2NaOH+H2SO4=Na2SO4+2H2O
2NaOH+H2SO4=Na2SO4+2H2O
Θ°
Θ®2Θ©…ηΦΤ Β―ιΘ§ΧΫΨΩœΓΝρΥα”κ«β―θΜ·ΡΤ»ή“ΚΒΡΖ¥”Π «ΖώΖ≈»»
Β―ι“«Τς”κ“©ΤΖΘΚ10%ΒΡΝρΥαΓΔ10%ΒΡ«β―θΜ·ΡΤ»ή“ΚΓΔ…’±≠ΓΔΈ¬Ε»ΦΤΓΔ≤ΘΝßΑτΓΔΫΚΆΖΒΈΙήΘ°
«κΡψΆξ≥… Β―ιΖΫΑΗ…ηΦΤΘΚ
| Β ―ι ≤Ϋ ÷η |
Β―ιœ÷œσ |
Ϋα¬έ |
|
|
œΓΝρΥα”κ«β―θΜ·ΡΤ»ή“ΚΖ¥”ΠΖ≈»» |
Θ®3Θ©ΧΫΨΩœΓΝρΥα”κ«β―θΜ·ΡΤ»ή“Κ «Ζώ«ΓΚΟΆξ»ΪΖ¥”Π
ΒΎΕΰΉιΆ§―ß‘ΎΉωΆξœΓΝρΥα”κ«β―θΜ·ΡΤ»ή“ΚΖ¥”ΠΒΡ Β―ιΚσΘ§ΈΣΧΫΨΩœΓΝρΥα”κ«β―θΜ·ΡΤ»ή“Κ «Ζώ«ΓΚΟΆξ»ΪΖ¥”ΠΘ°
…ηΦΤΝΥ Β―ιΖΫΑΗΕΰΘΚ
| Β―ι≤Ϋ÷η |
Β―ιœ÷œσ |
Ϋα¬έ |
| »Γ…ΌΝΩ…œ ωΖ¥”ΠΚσΒΡ»ή“Κ”Ύ ‘Ιή÷–Θ§ΒΈΦ”ΝρΥαΆ≠»ή“ΚΘ° |
»τ …ζ≥…άΕ…Ϊ≥ΝΒμ …ζ≥…άΕ…Ϊ≥ΝΒμ |
«β―θΜ·ΡΤ»ή“ΚΙΐΝΩ |
| »τΟΜ”–Οςœ‘œ÷œσ |
œΓΝρΥα”κ«β―θΜ·ΡΤ»ή“Κ«ΓΚΟΆξ»ΪΖ¥”Π |
¥Υ ±”–Ά§―ßΧα≥ωΖΫΑΗΕΰ≤ΜΡή÷ΛΟςœΓΝρΥα”κ«β―θΜ·ΡΤ»ή“Κ«ΓΚΟΆξ»ΪΖ¥”ΠΘ§Τδ‘≠“ρ «
»τ―ΈΥαΙΐΝΩΘ§Φ”»κΝρΥαΆ≠»ή“Κ ±“≤ΈόΟςœ‘œ÷œσΘ®ΜρΝρΥαΩ…Ρή”– Θ”ύΘ©ΘΜ
»τ―ΈΥαΙΐΝΩΘ§Φ”»κΝρΥαΆ≠»ή“Κ ±“≤ΈόΟςœ‘œ÷œσΘ®ΜρΝρΥαΩ…Ρή”– Θ”ύΘ©ΘΜ
Θ°ΈΣ¥ΥΘ§ΜΙ–η“Σ―Γ‘ώ
Ήœ…Ϊ ·»ο ‘“ΚΘ®Μρ–ΩΝΘΓΔΧΦΥαΡΤΓΔ―θΜ·Ά≠ΓΔ«β―θΜ·Ά≠ΓΔpH ‘÷ΫΒ»Θ©Θ°
Ήœ…Ϊ ·»ο ‘“ΚΘ®Μρ–ΩΝΘΓΔΧΦΥαΡΤΓΔ―θΜ·Ά≠ΓΔ«β―θΜ·Ά≠ΓΔpH ‘÷ΫΒ»Θ©Θ°
Θ®Χν“Μ÷÷ ‘ΦΝΘ©Θ§‘ΌΫχ–– Β―ιΦ¥Ω…Θ°
ΡήΝΠΧα…ΐΘΚ
Ρ≥ΒΊ–¬Ϋ®“ΜΜ·ΙΛ≥ß”–“Μ÷÷≤ζΤΖ τ”ΎΓΑΗ¥―ΈΓ±Θ§ΗΟ≤ζΤΖΩ…”ΟΉςΧζ ςΓΔΉΊιΒΒ»Μ®ΡΨΒΡΖ ΝœΘ°Ρ≥Μ·―ßΩΈΆβ–Υ»Λ–ΓΉιΧΫΨΩΗΟ≤ζΤΖΒΡΉι≥…Θ§Ϋχ––ΝΥ»γœ¬ΒΡ Β―ιΘΚΘ®≤ι‘ΡΉ ΝœΜώ÷ΣΘΚΓΑΗ¥―ΈΓ± «÷Η”…ΝΫ÷÷―τάκΉ”ΚΆ“Μ÷÷ΥαΗυάκΉ”Ήι≥…ΒΡ―ΈΘ°»γΙ⬱ ·Θ®KCl?MgCl
2?6H
2OΘ©Θ©Θ°
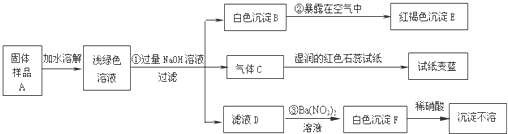
‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©–¥≥ωœ¬Ν–Έο÷ ΒΡΜ·―ß ΫΘΚC
NH3
NH3
ΓΔE
FeΘ®OHΘ©3
FeΘ®OHΘ©3
ΓΔF
BaSO4
BaSO4
Θ®2Θ©–¥≥ωœ¬Ν–±δΜ·ΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
ΔΎ
4FeΘ®OHΘ©2+O2+2H2O®T4FeΘ®OHΘ©3
4FeΘ®OHΘ©2+O2+2H2O®T4FeΘ®OHΘ©3
Δέ
Na2SO4+BaΘ®NO3Θ©2®TBaSO4Γΐ+2NaNO3
Na2SO4+BaΘ®NO3Θ©2®TBaSO4Γΐ+2NaNO3
Θ®3Θ©…œ ωΧΫΨΩΫαΙϊΥΒΟς―υΤΖA÷–Κ§”–ΒΡάκΉ””–
Fe2+ΓΔNH4+ΓΔSO42-
Fe2+ΓΔNH4+ΓΔSO42-
Θ°

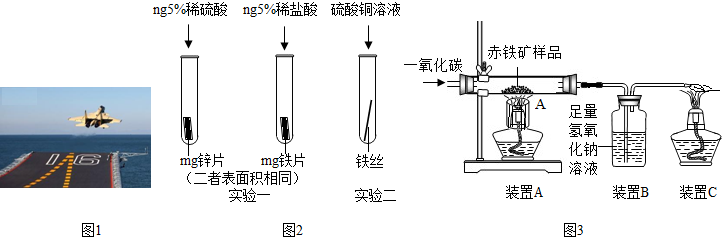

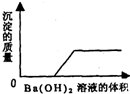 Θ®1Θ©Ρ≥“Μ”…―ΈΥαΓΔΧΦΥαΡΤ»ή“ΚΓΔœΓΝρΥαΓΔ¬»Μ·Ά≠»ή“ΚΥΡ÷÷Έο÷ ÷–ΒΡΝΫ÷÷ΜλΚœ–Έ≥…ΒΡΜλΚœ»ή“ΚΘ§œ÷œρΗΟΜλΚœ»ή“Κ÷–ΒΈ»κ«β―θΜ·±Β»ή“ΚΘ§≤ζ…ζ≥ΝΒμΒΡ÷ ΝΩ”κΦ”»κ«β―θΜ·±Β»ή“ΚΧεΜΐΒΡΙΊœΒ»γΆΦΥυ ΨΘ°ΗΟΜλΚœ»ή“ΚΒΡΉι≥… «
Θ®1Θ©Ρ≥“Μ”…―ΈΥαΓΔΧΦΥαΡΤ»ή“ΚΓΔœΓΝρΥαΓΔ¬»Μ·Ά≠»ή“ΚΥΡ÷÷Έο÷ ÷–ΒΡΝΫ÷÷ΜλΚœ–Έ≥…ΒΡΜλΚœ»ή“ΚΘ§œ÷œρΗΟΜλΚœ»ή“Κ÷–ΒΈ»κ«β―θΜ·±Β»ή“ΚΘ§≤ζ…ζ≥ΝΒμΒΡ÷ ΝΩ”κΦ”»κ«β―θΜ·±Β»ή“ΚΧεΜΐΒΡΙΊœΒ»γΆΦΥυ ΨΘ°ΗΟΜλΚœ»ή“ΚΒΡΉι≥… «