
题目列表(包括答案和解析)
下列各组金属粉末的质量均为1.12 g,分别与足量的稀硫酸反应,生成的气体的质量小于0.04 g的是
A.锌和铁
B.铁和镁
C.铁和铝
D.铝和镁
(6分)质量守恒定律应用的研究对化学科学发展具有重大作用。
(1)对质量守恒定律的微观解释是:在化学反应中,反应前后原子的 、 、 都不改变。
(2)在一定条件下,将100 mL的CO2缓缓通过足量的淡黄色固体Na2O2,充分反应后,生成50mL纯净的气体X,X能使带火星的木条复燃,淡黄色固体部分变为白色固体Y。
友情提示:在同温同压下,气体的体积比等于分子个数比。
请回答:X气体是 ;该反应的化学方程式可表示为:a Na2O2 + b CO2 = c X + d Y (其中a、b、c、d为化学计量数),则b:c = ;已知a:b=1:1,则Y是 。
(3)汽车安装安全气囊可以有效保护乘车人员,在车辆发生剧烈碰撞的瞬间,安全装置通电点火,使其中的粉末迅速分反应放出大量的氮气,形成气囊。该粉末由Fe2O3固体和化合物甲组成,加热13.0 g化合物甲,完全分解生成8.4 g氮气和单质乙。单质乙可在高温隔绝空气的条件下与Fe2O3发生置换反应生成Na2O。则化合物甲的化学式是 。
(6分)质量守恒定律应用的研究对化学科学发展具有重大作用。
(1)对质量守恒定律的微观解释是:在化学反应中,反应前后原子的 、 、 都不改变。
(2)在一定条件下,将100 mL的CO2缓缓通过足量的淡黄色固体Na2O2,充分反应后,生
成50mL纯净的气体X,X能使带火星的木条复燃,淡黄色固体部分变为白色固体Y。
友情提示:在同温同压下,气体的体积比等于分子个数比。
请回答:X气体是 ;该反应的化学方程式可表示为:a Na2O2 + b CO2 = c X + d Y (其中a、b、c、d为化学计量数),则b:c = ;已知a:b=1:1,则Y是 。
(3)汽车安装安全气囊可以有效保护乘车人员,在车辆发生剧烈碰撞的瞬间,安全装置通电点火,使其中的粉末迅速分反应放出大量的氮气,形成气囊。该粉末由Fe2O3固体和化合物甲组成,加热13.0 g化合物甲,完全分解生成8.4 g氮气和单质乙。单质乙可在高温隔绝空气的条件下与Fe2O3发生置换反应生成Na2O。则化合物甲的化学式是 。
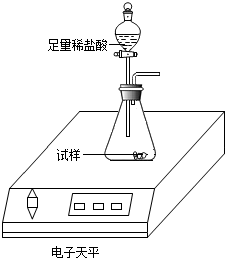 测定食用纯碱粉末的纯度取食用纯碱粉末试样,利用如图装置进行实验测定.数据记录如下:
测定食用纯碱粉末的纯度取食用纯碱粉末试样,利用如图装置进行实验测定.数据记录如下:| 称量项目 | 称量时间 | 质量/g |
| 试样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com