课外小组研究“影响H
2O
2 生成O
2反应速率的因素”的课题.通过查阅资料,他们提出如下猜想.
【提出猜想】催化剂和反应物浓度都会影响H
2O
2 生成O
2的反应速率
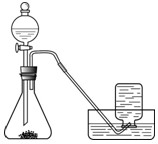
【实验过程】实验装置如图:
实验操作:检查装置的气密性良好.将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.
实验记录:
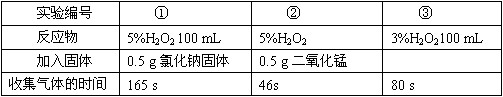
| 实验编号 |
① |
② |
③ |
| 反应物 |
5%H2O250mL |
5%H2O2 50mL 50mL |
3%H2O250mL |
| 加入固体 |
0.5gCuO |
0.5gMnO2 |
0.5gMnO2 |
| 收集等体积O2所需时间 |
105s |
45s |
78s |
(1)实验②中加入H
2O
2溶液的体积为
50
50
mL;
(2)充分反应后,将实验②中剩余物质里的MnO
2提取的方法是
过滤
过滤
;
【结论】该探究过程得出的结论是
催化剂的种类和过氧化氢溶液的质量分数能影响反应速率
催化剂的种类和过氧化氢溶液的质量分数能影响反应速率
;
【反思】H
2O
2在常温加入MnO
2后反应速率加快.小敏提出,为了更好的证明二氧化锰是否对H
2O
2 生成O
2的反应速率有影响,还应该增加一组对比实验.该实验选用的药品和用量为
50mL5%过氧化氢溶液(不加催化剂)
50mL5%过氧化氢溶液(不加催化剂)
;
【实验拓展】小敏用收集的气体进行氧气的性质实验.
(1)铁丝在氧气中燃烧,其反应的化学方程式为
;
(2)小敏发现用收集的气体进行铁丝燃烧实验时,没有产生明显的火星四射现象.造成这种结果的可能原因是
没等气泡连续、均匀的产生时就开始收集,导致所收集到的氧气不纯
没等气泡连续、均匀的产生时就开始收集,导致所收集到的氧气不纯
.

 课外小组研究“影响H2O2 生成O2反应速率的因素”的课题.通过查阅资料,他们提出如下猜想.
课外小组研究“影响H2O2 生成O2反应速率的因素”的课题.通过查阅资料,他们提出如下猜想.