
题目列表(包括答案和解析)
按要求写出下列反应的化学方程式,并说明该反应在实际中的一种应用。
| 化学方程式 | 实验中的就用 | |
| 有红磷参加的化合反应 | ||
| 有氧化钙生成的分解反应 |
学习热情和学习方法是成才的必备条件,灵活掌握不同的学习方法可以取得事半功倍的效果.请用以下方法解决下列问题:
(1)分类法:利用下列4组物质请按要求填写下表空白(填写物质的化学式或分类标准)
(分类标准包括:酸、碱、盐、金属氧化物、非金属氧化物、金属单质、非金属单质)
A.ZnO、MgO、CO2、Na2O B.Cu、N2、C、Cl2
C.KNO3、NaHCO3、KClO3、Fe(OH)3 D.H2SO4、H2O、HCl、HNO3
| A | B | C | D | |
| 分类标准 | 金属氧化物 | 盐 | ||
| 不属于该类别的物质 | Cu | H2O |
(2)对比法:
A.通过对CO2+H2O→H2CO3 和 6CO2+6H2O 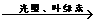 C6H12O6+6O2两个化学反应的
C6H12O6+6O2两个化学反应的
 对比,你能得出的结论是:相同的反应物在不同的条件下
对比,你能得出的结论是:相同的反应物在不同的条件下
.
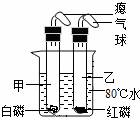
B.如图所示:小海同学将盛有干燥白磷的甲试管和干燥红磷的乙
试管插入盛有80℃的烧杯里(甲、乙试管均套有气球密封).过
一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请
根据小海同学的实验现象,对比得出可燃物燃烧所需的条件之
一: 。
(3)归纳演绎法:
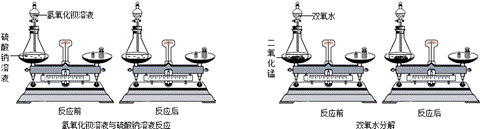
某同学通过对大量化学反应前后各物质的质量总和的测定分析(如上图中的氢氧化钡溶
液与硫酸钠溶液,用少量的双氧水和二氧化锰分解),得出参加化学反应的各物质的质量总和 (填“大于”、“小于”或“等于”)反应后生成的各种物质的质量总和.根据该同学得出的结论可推出:高温煅烧含有杂质的石灰石125g(杂质不发生反应),
充分反应后剩余固体质量为81g,则反应过程中生成二氧化碳的质量为 g。
请根据化学反应方程式列式计算①该石灰石中含碳酸钙的物质的量是多少?②该石灰石
中含碳酸钙的质量分数是多少?
请按要求填空。
(1)请写出相应的化学符号或名称
①2个磷原子 ;②+2价的锌元素 ;③2SO42- ;④2 H2O 。
(2)请在H、O、N、S、Cl、Na等6种元素中选择恰当的元素,组成符合下列要求的物质,并将其化学式填写在相对应的位置上
①一种重要化工产品,能使湿润的红色石蕊试纸变蓝的气体是 ;
②一种大气污染物,容易造成硫酸型酸雨的气体是 ;
③空气中含量最高的气体是 ;
④海水中含量最高的盐是 ;
⑤既可作为消毒剂,也可用于实验室制取氧气的液体试剂是 。
(3)请用化学方程式表示下列反应
①生石灰与水反应转变成熟石灰 ;
②高锰酸钾受热分解制氧气 ;
③盐酸和氢氧化钠的反应 。
一、选择题(本大题共10题,每小题2分,共20分)每小题给出的四个选项中,只有一个最符合题意,请将其序号涂在答题卡上。
题号
1
2
3
4
5
6
7
8
9
10
答案
C
C
B
D
B
D
C
D
A
D
二、选择题(本大题共5题,每小题2分,共10分)每小题给出的四个选项中,有1~2个符合题意。只有一个选项符合题意的多选不给分;有2个选项符合题意的只选一个且符合题意给1分,若选2个有一个不符合题意则不给分。
题号
11
12
13
14
15
答案
A
B
CD
BC
C
三、(本大题共4题 共20分)
16.(6分)(每空1分)(1)④ (2)⑤ (3)⑥ (4)① (5)③ (6)②
17.(3分)(每空1分) 31 B 质子数(核电荷数)不同
18.(7分)(每空1分) (1)① (2)氢气 (3)②④ (4)铁与氧气、水接触 保持铁刀表面的洁净和干燥(其他合理答案也给分) (5)合成橡胶 用布袋代替塑料袋(其他合理答案也给分)
19.(4分)(每空1分)(1)<;空气中有CO2,雨水溶解CO2,形成碳酸(2)是(3)化学方程式略
四、(本大题共3题 共16分)
20.(5分)(每个化学方程式1分)化学方程式略
21.(5分)(1)汽油将油污溶解 洗涤剂有乳化作用,将油污分散成无数细小的油滴随水流走 (2)化学方程式略 (3)紫色石蕊(无色酚酞)试液 (4)化学方程式略
22.(6分)(每空1分)(1)t
五、(本大题共3题 共24分)
23.(10分)(每空1分)(1)①酒精灯;;②a、d(2)①B;固体与液体混合且不需加热;化学方程式略;E;二氧化碳的密度大于空气且能溶于水;②蜡烛由下至上依次熄灭;二氧化碳的密度大于空气,不能燃烧且不支持燃烧);③不合理
24.(9分)(每空1分)(1) CO2 Cu (2) Cu、Na2CO3、CaCl2;(每种物质1分)(3)CuSO4、H2SO4(4)CuO+H2SO4==CuSO4+H2O或Cu(OH)2+H2SO4==CuSO4+2H2O(5)NaOH,取溶液B少许滴加过量的稀硝酸,待反应完全后向溶液中加入硝酸银溶液,若出现白色沉淀则含有NaCl,反之则无NaCl。
25.(5分)(每空1分)
【作出猜想】水里散发出一股与氮肥厂附近相似的刺激性气味
【表达交流】(1)受热易分解(2)与碱性物质可以反应
【反思评价】用废水作样品进行实验(或用纯净水溶解氮肥进行实验)
【探究启示】将水煮沸后再饮用(或用活性炭吸附净化后饮用)
评分说明: 【反思评价】答案合理,意思表达清楚即可;【探究启示】意思表达清楚即可。只答“净化”或“用碱净化”不给分。
六、(本大题共2题 共10分)
26.(3分)解:(1)
(2)盐酸中溶质的质量分数为x。

160 219
 1分
1分
x=10% 1分
答:略。
27.(7分)解:50mL氢氧化钠溶液中NaOH的质量为:50mL×
设与盐酸反应的NaOH的质量为x,生成的氯化钠质量为m1;与NaOH反应的氯化镁的质量为y,生成的氢氧化镁沉淀质量为z,生成的氯化钠质量为m2。
NaOH+HCl ===== NaCl+H2O
40 36.5 58.5
x
40 : x = 36.5 :
58.5 : m1 = 36.5 :
与氯化镁反应的NaOH的质量为:
MgCl2+2NaOH ===== Mg(OH)2↓+2NaCl
95 80 58 117
y
95 : y = 80:
58 : z = 80:
117 : m2 =80:
 1分
1分
答:略
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com