
21.(12分)有E、Q、T、X、Z五种前四周期元素,原子序数E<Q<T<X<Z。E、Q、T三种元素的基态原子具有相同的能层和能级,且I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且
QT2+与ET2互为等电子体。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。
请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)写出QT2+的电子式 、基态Z原子的核外电子排布式 。
(2) Q的简单氢化物极易溶于T的简单氢化物,其主要原因有 等两种。
(3)化合物甲由T、X两元素组成,其晶胞如图1,甲的化学式为 。
(4)化合物乙的晶胞如图2,乙由E、Q两元素组成,硬度超过金刚石。
①乙的晶体类型为 ,其硬度超过金刚石的原因是 。
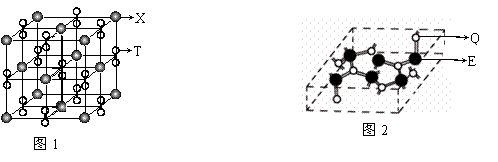 ②乙的晶体中E、Q两种元素原子的杂化方式均为 。
②乙的晶体中E、Q两种元素原子的杂化方式均为 。
20.(10分)工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化:
2SO2(g)+O2 (g) 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1
(1)生产中为提高反应速率和SO2的转化率,下列措施可行的是 (填字母)。
A.向装置中充入N2 B.向装置中充入过量的O2
C.使用更高效的催化剂 D.升高温度
(2)在一密闭容器中充入4 mol SO2和一定量O2,当放出353.6 kJ热量时,SO2的转化率最接近于
(填字母)。
A.40% B.50% C.80% D.90%
(3)580℃时,在一密闭容器中充入一定量的SO2和O2,当反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3 mol·L-1、8.0×10-3 mol·L-1和4.4×10-2 mol·L-1。该温度下反应2SO2(g)+O2 (g) 2SO3(g)的平衡常数K=
。
2SO3(g)的平衡常数K=
。
(4)硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需要加以处理后才能排放。现用右图所示装置测定尾气中SO2的含量,当通入尾气11.2 L(标准状况下测定)时,碘水恰好褪色。通过计算说明,该尾气能否直接排放(写出计算过程)。
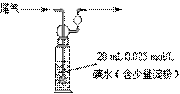
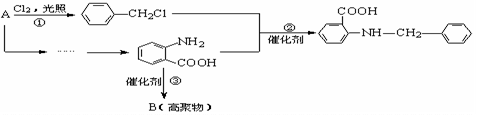
19.(14分)化合物C是一种合成药品的中间体,其合成路线为:
|
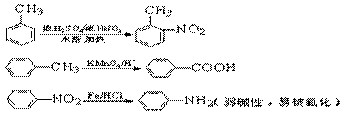
已知:
(1)写出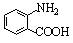 中官能团的名称
。
中官能团的名称
。
(2)写出反应①的化学方程式 。
(3)反应②属于 反应,反应③属于 (填有机反应类型)。
(4)写出满足下列条件的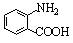 的同分异构体的结构简式 。
的同分异构体的结构简式 。
① 苯环上的一取代产物只有两种; ② 具有弱碱性,能发生银镜反应;
③ 水解后的产物能与FeCl3溶液发生显色反应。
(5)请你设计由A合成B的合成路线。
提示:①合成过程中无机试剂任选;②合成路线表示方法示例如下:
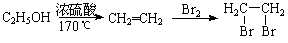
18.(10分)高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂。
(1)已知:4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2。
4Fe(OH)3+8OH-+3O2。
K2FeO4在处理水的过程中所起的作用有 。
(2)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-) =1.0 mmol·L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅰ。该实验的目的是 ;发生反应的△H 0(填“>”、“<”或“=”)。
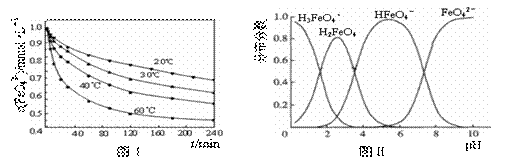
(3)FeO42-在水溶液中的存在形态如图Ⅱ所示。下列说法正确的是 (填字母)。
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4- 的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:
HFeO4-+OH-=FeO42-+H2O
(4)测定某K2FeO4溶液浓度的实验步骤如下:
步骤1:准确量取V mL K2FeO4溶液加入到锥形瓶中
步骤2:在强碱性溶液中,用过量CrO2-与FeO42-反应生成Fe(OH)3和CrO42-
步骤3:加稀硫酸,使CrO42-转化为Cr2O72-,CrO2-转化为Cr3+,Fe(OH)3转化为Fe3+
步骤4:加入二苯胺磺酸钠作指示剂,用c mol·L-1 (NH4)2Fe(SO4) 2标准溶液滴定至终点,消耗(NH4)2Fe(SO4) 2溶液V1 mL。滴定时发生的反应为:Fe2++Cr2O72-+H+→Fe3++Cr3++H2O
(未配平)
① 写出步骤2中发生反应的离子方程式 。
② 根据上述实验数据,测定该溶液中K2FeO4的浓度为 mol·L-1(用含字母的代数式表示)。
17.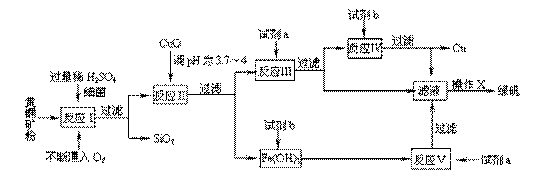 (10分)以黄铜矿(主要成份为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下:
(10分)以黄铜矿(主要成份为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下:
|
已知:① 4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
② 部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表
|
沉淀物 |
Cu(OH)2 |
Fe(OH)3 |
Fe(OH)2 |
|
开始沉淀pH |
4.7 |
2.7 |
7.6 |
|
完全沉淀pH |
6.7 |
3.7 |
9.6 |
(1)试剂a是 ,试剂b是 。
(2)操作X应为蒸发浓缩、 、 。
(3)反应Ⅱ中加CuO调pH为3.7-4的目的是 ;
(4)反应Ⅴ的离子方程式为 。
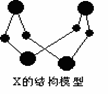
16.(8分)已知A、B、E是常见的非金属单质,其中A为淡黄色固体,Y是常见的金属单质,C的相对分子质量比A大32,D、G均是重要的工业产品,Y、F、H、I均含有同种元素。X含有两种元素,具有摇篮形的分子结构,球棍模型如图所示。H为红褐色沉淀。图中部分反应条件和产物已略去。
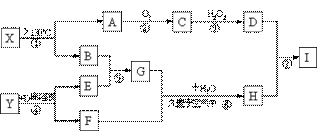
试回答下列问题
(1)写出X的化学式: 。
(2)写出G的电子式: 。
(3)写出反应③的化学方程式 。
(4)写出C和I溶液反应生成F的离子方程式 。
15.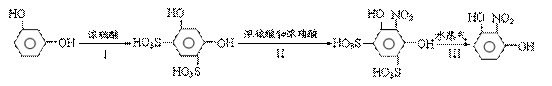 (10分)已知:2-硝基-1,3-苯二酚是桔黄色固体,易溶于水、溶液呈酸性,沸点为88℃,是重要的医药中间体。实验室常以间苯二酚为原料分以下三步合成:
(10分)已知:2-硝基-1,3-苯二酚是桔黄色固体,易溶于水、溶液呈酸性,沸点为88℃,是重要的医药中间体。实验室常以间苯二酚为原料分以下三步合成:
具体实验步骤如下:
① 磺化:称取5.5g碾成粉状的间苯二酚放入烧杯中,慢慢加入浓硫酸并不断搅拌,控制温度为60℃-
65℃约15min。
② 硝化:将烧杯置于冷水中冷却后加入混酸,控制温度(25 ±5)℃左右继续搅拌15 min。
③ 蒸馏:将反应混合物移入圆底烧瓶B中,小心加入适量的水稀释,再加入约0.1g尿素,然后用右图
所示装置进行水蒸气蒸馏;将馏出液冷却后再加入乙醇-水混合剂重结晶。
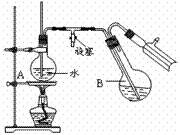 根据以上知识回答下列问题:
根据以上知识回答下列问题:
(1)实验中设计I、Ⅲ两步的目的是 。
(2)烧瓶A中玻璃管起稳压作用,既能防止装置中
压强过大引起事故、又能 。
(3)步骤②的温度应严格控制不超过30℃,原因是
。
(4)步骤③所得2-硝基-1,3-苯二酚中仍含少量
杂质,可用少量乙醇-水混合剂洗涤。请设计简单的证明2-硝基-1,3-苯二酚已经洗涤干净 。
(5)本实验最终获得1.0g桔黄色固体,则2-硝基-1,3-苯二酚的产率约为 。
14.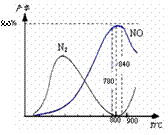 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度
的关系如右图。
4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905 kJ·mol-1 ①
4NO(g)+6H2O(g) △H=-905 kJ·mol-1 ①
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=-1268 kJ·mol-1 ②
2N2(g)+6H2O(g) △H=-1268 kJ·mol-1 ②
下列说法中正确的是
A.工业上氨催化氧化生成 NO时,温度应控制
在780-840℃之间
B.工业上采用物料比n(O2)/n(NH3)在1.7-2.0,主要是为了提高反应速率
C.加压可提高NH3生成NO的转化率
D.N2氧化为NO的热化学方程式为:N2(g)+O2(g) 2NO(g) △H=+181.5 kJ·mol-1
2NO(g) △H=+181.5 kJ·mol-1
非 选 择 题(共78分)
13.下列溶液中微粒的物质的量浓度关系正确的是
A.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:
c(NaOH)<c(CH3COONa)<c(Na2CO3)
B.pH=2的HA溶液与pH=12的MOH溶液以任意比混合:
c(H+)+c(M+)=c(OH-)+c(A-)
C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
D.某二元弱酸的酸式盐NaHA溶液中:c(H+)+2c(A2-)=c(OH-)+c(H2A)
12. LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。下列有关
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。下列有关
LiFePO4电池说法正确的是
A.可加入硫酸以提高电解质的导电性 B.放电时电池内部Li+向负极移动
C.充电过程中,电池正极材料的质量减少 D.放电时电池正极反应为:FePO4+Li++e-=LiFePO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com