
3、若以ω1和ω2分别表示浓度为amol/L和bmol/L氨水的质量分数,有知2a=b,则下列推断正确的是(氨水的密度比纯水的小)
A、2ω1=ω2 B、2ω2=ω1 C、ω2>2ω1 D、ω1<ω2 <2ω1
例4、25℃时,某物质(无结晶水)溶解度为Sg,其摩尔质量为Mg/mol,饱和溶液密度为dg/cm3,则其饱和溶液的物质的量浓度为( )
A、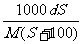 mol/L B、
mol/L B、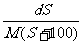 mol/L
mol/L
C、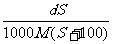 mol/L
D、
mol/L
D、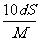 mol/L
mol/L
练习:将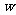 gNa2CO3•10H2O晶体溶解在
gNa2CO3•10H2O晶体溶解在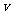 L水中,在相同的温度下配成密度为
L水中,在相同的温度下配成密度为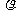 g/cm3的饱和溶液,若用C表示该饱和溶液的物质的量浓度(mol/L),A%表示质量分数,用S表示Na2CO3的溶解度g,则下列表示式正确的是( )
g/cm3的饱和溶液,若用C表示该饱和溶液的物质的量浓度(mol/L),A%表示质量分数,用S表示Na2CO3的溶解度g,则下列表示式正确的是( )
A、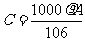 B、
B、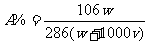
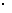 100%
100%
C、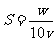 D、
D、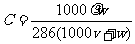

2、在100g浓度为18mol/L、密度为ρg/cm3的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加入水的体积为( )
A、小于100mL B、等于100mL C、大于100mL D、等于100/ρmL
3、质量分数不等的两种Na2SO4溶液等质量混合时,混合溶液的质量分数为a%,而等体积混合时为b%,质量分数不等的两种乙醇溶液等质量混合时,混合液的质量分数为a%,而等体积混合时为c%,则a、b、c的大小关系中( )
A、a>b>c B、b > a >c C、c >a>b D、a> c > b
例3、已知98%的浓硫酸的物质的量浓度是18.4mol/L,则49%的硫酸溶液的物质的量浓度是(单位:mol/L) ( )
A、等于9.2 B、小于9.2 C、大于9.2 D、不能确定
练习:1、已知质量分数为95%的酒精溶液的物质的量浓度为16.52mol/L试判断47.5%酒精溶液的物质的量浓度为( )
A、大于8.26mol/L B、等于8.26mol/L C、小于8.26mol/L D、无法判断
2、已知甲、乙溶质质量分数与密度的关系如下表:
|
溶质质量分数 |
甲溶液密度(g/cm3) |
乙溶液密度(g/cm3) |
|
1% |
0. 95 |
1.02 |
|
5% |
0.92 |
1.04 |
|
10% |
0.90 |
1.07 |
甲物质的1%的溶液与9%的溶液等体积混合, 乙物质的1%的溶液与9%的溶液等体积混合后,下列叙述正确的是( )
A、 混合后甲、乙溶液质量分数均大于5%
B、 混合后乙溶液质量分数大于5%,甲溶液质量分数小于5%
C、 混合后甲溶液质量分数大于5%,乙溶液质量分数小于5%
D、 混合后甲、乙溶液质量分数均等于5%
例1、常温时A的物质的溶解度为15g,B物质的饱和溶液的质量分数为15%,而浓度为15%的C物质的溶液100g,蒸发掉15g水,恢复到常温时析出晶体1g,则此三种物质在常温时的溶解度SA、SB、SC由大到小的顺序正确的是( )
A、SA>SB>SC B、 SC>SB>SA C、 SC> SA>SB D、SC =SB>SA
练习:1、某温度下,甲、乙两个烧杯中各盛有100g相同浓度的KCl溶液,现将甲烧杯中的溶液蒸发掉35g水,析出晶体5g,乙烧杯中溶液蒸发掉45g水,析出晶体10g,则原溶液中KCl的质量分数为( )
A、10% B、15% C、20% D、25%
2、t℃时,将一定质量的某物质的不饱和溶液分成三份,分别加热蒸发溶液,然后把温度降至t℃,已知从三份溶液中蒸发的溶剂质量分别为10g、20g、30g,析出晶体(不含结晶水)质量分别为a、b、c(单位g,且a、b、c均大于零),则a、b、c三者的关系为( )
A、c=2b-a B、c=a+b C、c=a+2b D、c=2a+b
例2:密度为0.91g/cm3的氨水,质量分数为25%,该氨水用等体积的水稀释后,所得溶液的质量分数为( )
A、等于12.5% B、大于12.5% C、小于12.5% D、无法确定
练习:1、把质量分数为70%的HNO3(密度为1.40g/cm3)加到等体积的水中,稀释后硝酸溶液中溶质的质量分数为( )
A、35% B、大于35% C、小于35% D、≤35%
4、以上各量间的综合计算
3、溶液的质量分数
2、溶液的物质的量浓度
1、溶解度
35.(8分)研究人员用黑色美西螈的受精卵做了如下实验


|






(1)实验一的结果说明: 。
(2)导致实验二结果的原因: 。
(3)导致实验三结果的原因: 。
(4)以上实验说明: 。
昆明三中、滇池中学2010--2011学年上学期期中考试
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com