
17.(10分)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制减法”两
种工艺。请按要求回答下列问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:
。
(2)写出“联合制减法”有关反应的化学方程式: ; 。
(3)CO2是制碱工业的重要原料,“联合制减法”和“氨碱法”中CO2的来源有何不同?
。
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制减法”的总反应,
列出计算原子利用率的表达式:原子利用率(%)= 。
16.(7分)苯甲醛在医药、染料、香料等行业有着广泛的应用。实验室通过下图所示的流程
由甲苯氧化制备苯甲醛。
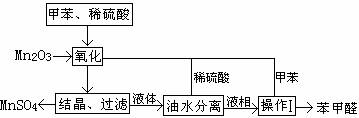
试回答下列问题:
(1)Mn2O3氧化甲苯的反应需要不断的搅拌,搅拌的作用是 。
(2)甲苯经氧化后的得到的混合物通过结晶、过滤进行分离。该过程需要将混合物冷却,
其目的是 。
(3)实验过程中,可循环使用的物质分别为 、 。
(4)实验中分离甲苯和苯甲醛采用的操作Ⅰ的名称是 ,其原理是 。
(5)实验中发现,反应时间不同苯甲醛的产率也不同(数据见下表)
|
反应时间/h |
1 |
2 |
3 |
4 |
5 |
|
苯甲醛产率/% |
76.0 |
87.5 |
83.6 |
72.5 |
64.8 |
请结合苯甲醛的结构,分析当反应时间过长时,苯甲醛产率下降的原因是 。
15.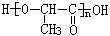 现在大量使用的塑料,如聚苯乙烯,因难以分解而造成严重的“白色污染”,为此,铁道
现在大量使用的塑料,如聚苯乙烯,因难以分解而造成严重的“白色污染”,为此,铁道
部下令全国铁路餐车停止使用聚苯乙烯制造的餐具,改用可降解塑料
以降低“白色垃圾”的污染。该塑料在乳酸菌的作用下能迅速分解为无
毒物质,下列有关降解塑料的叙述正确的是 ( )
A.降解塑料是一种纯净物 B.它是经缩聚反应生成的
C.其相对分子质量为72 D.合成它的单体为:HO-CH2CH2COOH
第Ⅱ卷(55分)
|
14.已知某有机物的分子结构如下图,1mol该有机物分别与足量的钠、氢氧化钠、新制氢氧
化铜悬浊液(可加热)反应时,所消耗的钠、氢氧化钠、氢氧化铜的物质的量之比为
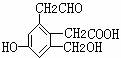 ( )
( )
A.6:4:5 B.3:2:2
C.3:2:3 D.6:4:1
13.由苯乙烯(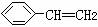 )和羟基乙酸乙酯(
)和羟基乙酸乙酯(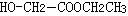 )组成的混合物中,
)组成的混合物中,
氢元素的质量分数为 ( )
A.4.6% B.7.7% C.15.6 % D.无法计算
12.下列说法不正确的是 ( )
A.乙醇的沸点远高于丙烷,是由于乙醇分子间存在氢键
B.氨基酸与酸、碱都能反应生成盐
C.2-丁烯不存在顺反异构体
D.乙醛的核磁共振氢谱中有两个峰且峰面积之比为1:3
11.下列变化需要吸收能量的是 ( )
A.1s22s22p63s1→1s22s22p6 B.3s23p5→3s23p6
C.2px22py12pz1→2px12py12pz2 D.2H→H-H
10.下列各组元素性质的递变情况错误的是
A.Li、Be、B原子的最外层电子数依次增多
B.P、S、Cl元素的最高正价依次升高
C.N、O、F元素的电负性依次增大
D.Na、K、Rb的第一电离能逐渐增大
9.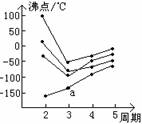 右图中每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代
右图中每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代
表一种氢化物,其中a点代表的是 ( )
A.H2S B.HCl
C.PH3 D.SiH4
8.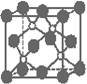 磷化硼是一种超硬耐磨涂层材料。下图为其晶体结构中最小的重复结构单元,其中的每
磷化硼是一种超硬耐磨涂层材料。下图为其晶体结构中最小的重复结构单元,其中的每
个原子均满足8电子稳定结构。下列有关说法正确的是 ( )
A.磷化硼晶体的化学式为BP,属于离子晶体
B.磷化硼晶体的熔点高,且熔融状态下能导电
C.磷化硼晶体中每个原子均形成4条共价键
D.磷化硼晶体结构微粒的空间堆积方式与氯化钠相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com