
16.下列离子方程式不正确的是 ( )
A.用两个铜电极电解饱和食盐水:2Cl-+2H2O 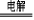 2OH- + H2↑+ Cl2↑
2OH- + H2↑+ Cl2↑
B.AgCl悬浊液中加入硫化钠饱和溶液:2AgCl + S2-=Ag2S +2Cl-
C.氢氧化镁与稀硫酸反应:H++OH-=H2O
D.向20mL沸水中滴入1mL饱和FeCl3溶液,继续煮沸至溶液呈红褐色:
Fe3++3H2O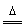 Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
15.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是 ( )
A 常温常压下,18.0g重水(D2O)所含的电子数约为10×6.02×1023
B 2.24LCl2中含有的原子数为0.2 ×6.02×1023
C. 室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023
D.7.8g过氧化钠粉末与水反应转移的电子数为0.1×6.02×1023
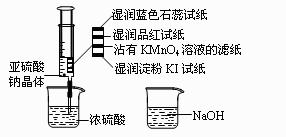
14.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是 ( )
A.蓝色石蕊试纸先变红后褪色
B.品红试纸、沾有KMnO4溶液滤纸均褪色证明了SO2漂白性
C.湿润淀粉KI试纸未变蓝说明SO2的氧化性弱于I2
D.可用NaOH溶液除去实验中多余的SO2
13.下列物质长期露置空气中易变质的是 ( )
①漂白粉 ②氯水 ③水玻璃 ④硫酸钠⑤烧碱 ⑥亚硫酸钠 ⑦胆矾 ⑧重晶石(硫酸钡晶体) ⑨十水碳酸钠 ⑩绿矾
A.除④⑦⑧外 B.除④⑦外 C.除⑥⑦⑧外 D.全易变质
12.用固体NaOH配制一定物质的量浓度的溶液时,下列操作会导致溶液浓度偏高( )
A.在烧杯中溶解后,马上转移入容量瓶中 B.定容时俯视容量瓶刻度线
C.容量瓶使用前未干 D.洗涤液未转移入容量瓶中
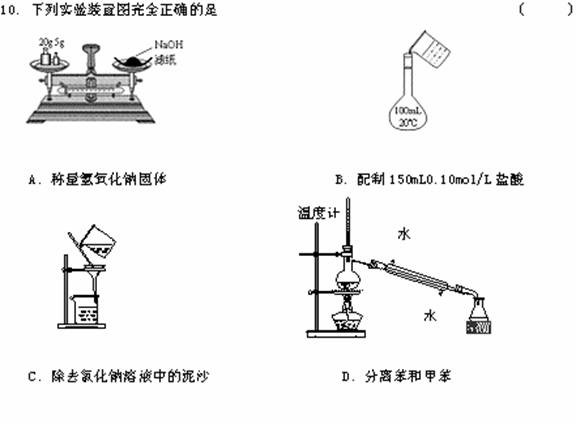
11.下列实验操作正确的是 ( )
A.粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体
B.容量瓶检漏:在容量瓶中注入适量的水,塞上玻璃瓶塞,左手五指托住瓶底,右手食指顶住瓶塞,反复倒置数次,观察是否漏水
C.用分液法分离C2H5OH与H2O的混合物
D.测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较
9.氯化铁溶液和氢氧化铁胶体具有的共同性质是 ( )
A.分散系颗粒直径都在1~100nm之间 B.能透过滤纸
C.滴加几滴稀盐酸均无沉淀现象 D.呈红褐色
8.分类是化学研究中常用的方法。下列分类方法中,不正确的是 ( )
A.根据元素原子最外层电子数的多少将元素分为金属和非金属
B.依据有无电子转移,将化学反应分为氧化还原反应和非氧化还原反应
C.根据电解质在熔融状态下或水溶液中能否完全电离将电解质分为强电解质和弱电解质
D.依据组成元素的种类,将纯净物分为单质和化合物
7. X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法正确的是( )
A.X的原子半径一定大于Y的原子半径
B.X与Y的简单离子不可能具有相同电子层结构
C.两元素形成的化合物中原子个数比不可能为1︰1
D.X2Y可能是离子化合物,也可能是共价化合物
6.若不断地升高温度,实现"雪花→水→水蒸气→氧气和氢气"的变化。在变化的各阶段被破坏的粒子间的主要相互作用依次是 ( )
A.氢键;分子间作用力;非极性键
B.氢键;氢键;极性键
C.氢键;极性键;分子间作用力
D.分子间作用力;氢键;非极性键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com