
科目:初中化学 来源: 题型:阅读理解
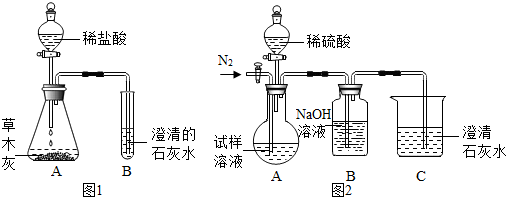
| 化合物所含金属元素 | 钙元素 | 钾元素 | 铜元素 |
| 灼烧产生火焰颜色 | 砖红色 | 紫色(透过蓝色钴玻璃片) | 绿色 |
科目:初中化学 来源: 题型:阅读理解
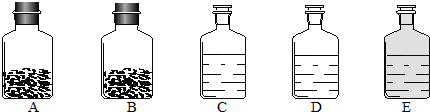

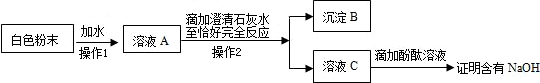
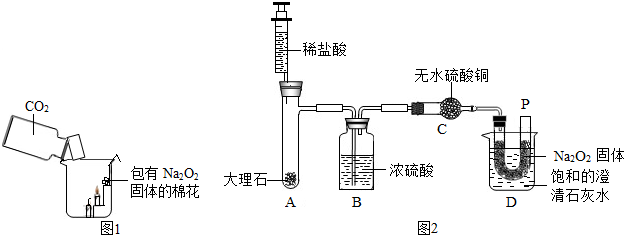

| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.30 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 248.20 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 248.00 |
科目:初中化学 来源: 题型:阅读理解
科目:初中化学 来源: 题型:阅读理解
能源、资源、环境与人类的生活和社会的发展密切相关。
(1)煤、石油和天然气等化石燃料是 ▲ 能源(选填“可再生”或“不可再生”)。
①将煤块粉碎成煤粉后燃烧,其目的是 ▲ 。煤燃烧时排放出 ▲ ,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。
②为节约化石燃料及减少环境污染,人类需要利用和开发新能源,如地热能、生物质能、
▲ 等(填一种即可)。
(2)水是地球上最普通、最常见的物质之一。
①浑浊的天然水经沉淀、过滤、吸附等净化处理后,得到澄清的水是 ▲ (选填“纯净物”或“混合物”)。生活中通过 ▲ 的方法可以降低水的硬度。
②海水中溶解了大量的氯化钠,海水晒盐的原理是 ▲ (选填“蒸发溶剂”或“冷却热的饱和溶液”),氯化钠在溶液中是以 ▲ 的形式存在的(填粒子符号)。
(3)人类每年都要从大自然中提取大量的金属,用于工农业生产和其他领域。
①铁制品锈蚀的过程,实际上是铁与空气中的 ▲ 发生化学反应的过程。铝具有很好的抗腐蚀性能,原因是 ▲ (用文字叙述)。
②铁钉浸入硫酸铜溶液中,发生反应的化学方程式为 ▲ ,反应后溶液的质量会 ▲ (选填“增大”、“减小”或“不变”)。
③某工厂的废液中含有硝酸银和硝酸铜,为回收资源和防止污染,向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入稀盐酸,无气体产生。下列说法正确的是 ▲
(选填字母)。
A.滤渣中一定含有银,可能含有铜
B.滤渣中一定含有银和铜,一定没有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银
D.滤液中一定含有硝酸亚铁,一定没有硝酸铜
科目:初中化学 来源:2013-2014学年江苏省南京市秦淮区九年级上学期期末考试化学试卷(解析版) 题型:填空题
能源、资源、环境与人类的生活和社会的发展密切相关。
(1)煤、石油和天然气等化石燃料是 能源(选填“可再生”或“不可再生”)。
①将煤块粉碎成煤粉后燃烧,其目的是 。煤燃烧时排放出 ,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。
②为节约化石燃料及减少环境污染,人类需要利用和开发新能源,如地热能、生物质能、 等(填一种即可)。
(2)水是地球上最普通、最常见的物质之一。
①浑浊的天然水经沉淀、过滤、吸附等净化处理后,得到澄清的水是 (选填“纯净物”或“混合物”)。生活中通过 的方法可以降低水的硬度。
②海水中溶解了大量的氯化钠,海水晒盐的原理是 (选填“蒸发溶剂”或“冷却热的饱和溶液”),氯化钠在溶液中是以 的形式存在的(填粒子符号)。
(3)人类每年都要从大自然中提取大量的金属,用于工农业生产和其他领域。
①铁制品锈蚀的过程,实际上是铁与空气中的 发生化学反应的过程。铝具有很好的抗腐蚀性能,原因是 (用文字叙述)。
②铁钉浸入硫酸铜溶液中,发生反应的化学方程式为 ,反应后溶液的质量会 (选填“增大”、“减小”或“不变”)。
③某工厂的废液中含有硝酸银和硝酸铜,为回收资源和防止污染,向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入稀盐酸,无气体产生。下列说法正确的是
(选填字母)。
A.滤渣中一定含有银,可能含有铜
B.滤渣中一定含有银和铜,一定没有铁
C.滤液中一定含有硝酸亚铁,一定没有硝酸银
D.滤液中一定含有硝酸亚铁,一定没有硝酸铜
科目:初中化学 来源:不详 题型:填空题
| A.滤渣中一定含有银,可能含有铜 |
| B.滤渣中一定含有银和铜,一定没有铁 |
| C.滤液中一定含有硝酸亚铁,一定没有硝酸银 |
| D.滤液中一定含有硝酸亚铁,一定没有硝酸铜 |
科目:初中化学 来源:0110 月考题 题型:填空题

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com