
t℃时将一定质量的某物质的不饱和溶液分为三等份,分别加热蒸发溶剂.然后再把温度降至t℃.已知三份溶液中蒸发的溶剂分别为10g、20g、30g,析出的晶体(不含结晶水)分别为ag、bg、cg.则a、b、c三者的关系为( )
|
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:单选题
| A.c=2b-a | B.c=b+a | C.c=2b+a | D.c=2a+b |
科目:高中化学 来源:2013年高考化学备考复习卷C3:溶液(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源: 题型:
t℃时,将一定质量的某物质的不饱和溶液均匀分为三份,分别加热蒸发溶液,然后把温度降到t℃,已知从三份溶液中蒸发溶剂的质量分别为10g,20g,30g,析出晶体(不含结晶水)分别为a、b、c单位g,且a、b、c均大于零,则a、b、c三者的关系为 ( )
A.c=2b-a B.c=a+b C.c=a+2b D.c=2a+b
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| △ |
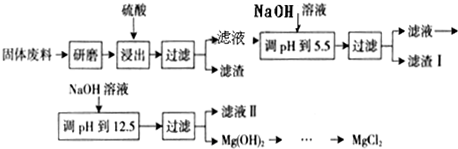
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
科目:高中化学 来源: 题型:
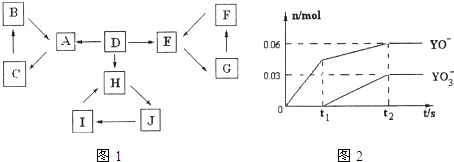
| 信 息 | |
| 1 | D为地壳中含量最高的元素组成的单质 |
| 2 | E为酸性氧化物,不溶于水,能与某种酸反应 |
| 3 | F不溶于水 |
| 4 | H为淡黄色固体化合物 |
| 5 | 电解饱和J溶液是工业重要反应 |
| 6 | C为离子化合物,阴、阳离子均含有金属元素. |
科目:高中化学 来源: 题型:阅读理解
已知2A(g)+B(g) ![]() 2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
⑴比较a b(填“>”“=”或“<”)。
⑵下表为不同温度下该反应的平衡常数。由此可推知,表中T1 T2(填“>” “=”或“<”)。
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
若在原来的容器中,只加入2molC,500℃时充分反应达平衡后,吸收热量为c kJ,C 的浓度 (填“>”、“=”或“<”)ωmol/L,a、b、c之间满足何种关系 (用代数式表示)。
⑶在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是 。
A.4molA和2molB B.4molA、2molB和2molC
C.4molA和4molB D.6molA和4molB
⑷为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
A.及时分离出C气体 B.适当升高温度
C.增大B的浓度 D.选择高效催化剂
⑸若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和1molB,500℃时充分反应达平衡后,放出热量为d kJ,则d b(填“>”“=”或“<”),理由是 。
⑹在一定温度下,向一个容积可变的容器中,通入3molA和2molB及固体催化剂,使之反应,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量 (填“不变”“变大”“变小”或“无法确定”)。
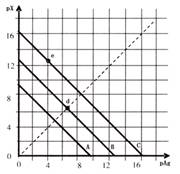
⑺某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小。已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX-pAg的坐标系可表示出 AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系。下列说法错误的是
A.A线是AgCl,C线是AgI
B.e点表示由过量的KI与AgNO3反应产生AgI沉淀
C.d点是在水中加入足量的AgBr形成的饱和溶液
D.B线一定是AgBr
科目:高中化学 来源:2010-2011学年浙江省高三高考全真压轴考试(理综)化学试题 题型:填空题
已知2A(g)+B(g)  2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
⑴比较a b(填“>”“=”或“<”)。
⑵下表为不同温度下该反应的平衡常数。由此可推知,表中T1 T2(填“>” “=”或“<”)。
|
T/K |
T1 |
T2 |
T3 |
|
K |
1.00×107 |
2.45×105 |
1.88×103 |
若在原来的容器中,只加入2molC,500℃时充分反应达平衡后,吸收热量为c kJ,C 的浓度 (填“>”、“=”或“<”)ωmol/L,a、b、c之间满足何种关系 (用代数式表示)。
⑶在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是 。
A.4molA和2molB B.4molA、2molB和2molC
C.4molA和4molB D.6molA和4molB
⑷为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
A.及时分离出C气体 B.适当升高温度
C.增大B的浓度 D.选择高效催化剂
⑸若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和1molB,500℃时充分反应达平衡后,放出热量为d kJ,则d b(填“>”“=”或“<”),理由是 。
⑹在一定温度下,向一个容积可变的容器中,通入3molA和2molB及固体催化剂,使之反应,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量 (填“不变”“变大”“变小”或“无法确定”)。
⑺某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl,AgBr,AgI的Ksp依次减小。已知pAg=-lgc(Ag+),pX=-lgc(X-),利用pX-pAg的坐标系可表示出 AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系。下列说法错误的是
A.A线是AgCl,C线是AgI
B.e点表示由过量的KI与AgNO3反应产生AgI沉淀
C.d点是在水中加入足量的AgBr形成的饱和溶液
D.B线一定是AgBr
科目:高中化学 来源: 题型:
(1)提出假设:该反应的气体产物全部是二氧化碳。
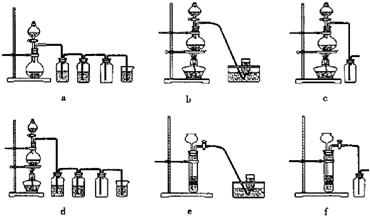
(2)设计方案:将一定量的氧化铁在隔绝氧气条件下与过量炭粉完全反应(如下图),测定参加反应的碳元素与氧元素的质量比。
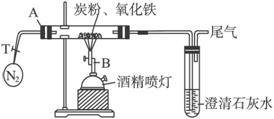
(3)查阅资料:氮气不与碳、氧化铁发生反应,可采用隔绝氧气。实验室可以用氯化铵饱和溶液和亚硝酸钠饱和溶液混合加热反应制得氮气。请写出该反应的离子方程式:
___________________________。
(4)实验操作:
操作步骤及实验现象 | 简答 |
称取 | — |
②加热前,先通一段时间纯净、干燥的氮气 | 其目的是:_________________ |
③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 该现象说明:_________________ |
④完全反应后,冷却至室温,称得玻璃管和固体的总质量为 | — |
(5)数据处理:经计算,参加反应的碳元素质量为
(6)得到结论:根据数据处理结果,得出原假设不成立,理由是:__________________________。
(7)根据数据处理结果,反应生成的气体是_________,且气体的物质的量之比是_________,该实验的化学方程式为:___________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com