
已知A、B、C、D、E是原子序数依次增大的5种短周期主族元素,其中A在反应中既不容易得到电子,也不容易失去电子,B原子的最外层电子数是其电子层数的3倍,D与A位于同一族,C与E形成的化合物CE是海水中的重要成分.下列说法正确的是( )
|
科目:高中化学 来源: 题型:
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:单选题
| A.离子半径:E>B>C |
| B.熔点:CE<DE |
| C.C与B形成的两种化合物中化学键类型完全相同 |
| D.A、D、E的最高价氧化物对应水化物的酸性逐渐增强 |
科目:高中化学 来源:2013年高考化学备考复习卷C4:物质结构和元素周期律(解析版) 题型:选择题
科目:高中化学 来源: 题型:

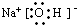
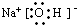
 H++HO2ˉ
H++HO2ˉ H++HO2ˉ
H++HO2ˉ| c2(SO3) |
| c(O2)?c2(SO2) |
| c2(SO3) |
| c(O2)?c2(SO2) |
科目:高中化学 来源: 题型:
科目:高中化学 来源: 题型:
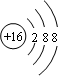
已知A、B、C、D、E为原子序数依次增大的五种短周期元素。其中A与D、B与E同主族,C元素的最外层电子数是内层电子数的3倍,D元素在地壳中的含量仅次于氧,D的单质是良好的半导体材料,E元素的最高正价与最低负价的代数和为2。请回答:
(1)E元素的氢化物是 分子(填“极性”或“非极性”),电子式是 。
(2)A、B、C三种元素形成的氢化物的熔点由高到低的顺序是 。(用化学式表示)
(3)B、D、E三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是 。(用化学式表示)
(4)工业上用A单质制备D单质的化学方程式是 。
D和C形成的固体物质属于 晶体。
科目:高中化学 来源:2011届云南省昆明三中高三上学期第二次月考(理综)化学部分 题型:填空题
已知A、B、C、D、E为原子序数依次增大的五种短周期元素。其中A与D、B与E同主族,C元素的最外层电子数是内层电子数的3倍,D元素在地壳中的含量仅次于氧,D的单质是良好的半导体材料,E元素的最高正价与最低负价的代数和为2。请回答:
(1)E元素的氢化物是 分子(填“极性”或“非极性”),电子式是 。
(2)A、B、C三种元素形成的氢化物的熔点由高到低的顺序是 。(用化学式表示)
(3)B、D、E三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是 。(用化学式表示)
(4)工业上用A单质制备D单质的化学方程式是 。
D和C形成的固体物质属于 晶体。
科目:高中化学 来源:2012-2013学年北京市石景山区高三第一学期期末考试化学试卷(解析版) 题型:选择题
A、B、C、D、E是原子序数依次增大的五种短周期元素且B、C相邻,A元素可以与B、C、E元素分别形成甲、乙、丙三种物质且甲、乙均为10电子化合物,丙为18电子化合物。D元素的最外层电子数与核外电子层数相等。已知:甲+E2=丙+B2,甲+丙=丁,下列说法正确的是
A.离子半径:D>C>B
B.A与C两种元素共同形成的10电子粒子有3种
C.D元素在周期表中的位置可以是第二周期第ⅡA族
D.丁物质均由非金属元素构成,只含共价键
科目:高中化学 来源: 题型:单选题
A、B、C、D、E是原子序数依次增大的五种短周期元素且B、C相邻,A元素可以与B、C、E元素分别形成甲、乙、丙三种物质且甲、乙均为10电子化合物,丙为18电子化合物。D元素的最外层电子数与核外电子层数相等。已知:甲+E2=丙+B2,甲+丙=丁,下列说法正确的是
A.离子半径:D>C>B
B.A与C两种元素共同形成的10电子粒子有3种
C.D元素在周期表中的位置可以是第二周期第ⅡA族
D.丁物质均由非金属元素构成,只含共价键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com