
œ¬¡–∏˜πÿœµ Ω÷–ƒÐÀµ√˜∑¥”¶N2+3H2?2NH3“—¥ÔµΩ∆Ω∫‚◊¥Ã¨µƒ «£®°°°°£©
|
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£Æ3¶‘’˝£®N2£©=¶‘’˝£®H2£© | B£Æ¶‘’˝£®N2£©=¶‘ƒÊ£®NH3£© |
| C£Æ¶‘’˝£®N2£©=3¶‘ƒÊ£®H2£© | D£Æ2¶‘’˝£®H2£©=3¶‘ƒÊ£®NH3£© |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2012-2013—߃Í∫˛ƒœ °…€—Ù –¬°ªÿœÿÕÚ∫Õ µ—È—ß–£∏þ∂˛£®…œ£©∆⁄÷–ªØ—ß ‘æÌ£®¿Ìø∆£©£®Ω‚Œˆ∞Ê£© –գ∫—°‘ÒÂ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫ÃÓø’Â
£®14∑÷£©∫œ≥…∞± «»À¿ý—–æøµƒ÷ÿ“™øŒÃ‚£¨ƒø«∞𧓵∫œ≥…∞±µƒ‘≠¿ÌŒ™£∫
∫œ≥…∞± «»À¿ý—–æøµƒ÷ÿ“™øŒÃ‚£¨ƒø«∞𧓵∫œ≥…∞±µƒ‘≠¿ÌŒ™£∫
N2£®g£©+3H2£®g£© 2NH3£®g£©°˜H=-93.0kJ?mol-1£¨‘⁄3∏ˆ2Lµƒ√б’»ð∆˜÷–£¨ π”√œýÕ¨µƒ¥þªØº¡£¨∞¥≤ªÕ¨∑Ω ΩÕ∂»Î∑¥”¶ŒÔ£¨∑÷±Ω¯––∑¥”¶£∫
2NH3£®g£©°˜H=-93.0kJ?mol-1£¨‘⁄3∏ˆ2Lµƒ√б’»ð∆˜÷–£¨ π”√œýÕ¨µƒ¥þªØº¡£¨∞¥≤ªÕ¨∑Ω ΩÕ∂»Î∑¥”¶ŒÔ£¨∑÷±Ω¯––∑¥”¶£∫
œý≥÷∫„Œ¬°¢∫„»ð£¨≤‚µƒ∑¥”¶¥ÔµΩ∆Ω∫‚ ±πÿœµ ˝æð»Áœ¬£∫
| »ð∆˜ | º◊ | ““ | ±˚ |
| ∑¥”¶ŒÔÕ∂»Î¡ø | 3molH2°¢2molN2 | 6molH2°¢4molN2 | 2mol NH3 |
| ¥ÔµΩ∆Ω∫‚µƒ ±º‰/min | | 6 | 8 |
| ∆Ω∫‚ ± N2µƒÃª˝√Ð∂» | C1 | 1.5 | |
| ªÏ∫œ∆¯ÃÂ√Ð∂»/g°§L-1 |  | 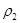 | |
| ∆Ω∫‚≥£ ˝/ L2°§mol-2 | Kº◊ | K““ | K±˚ |
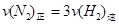 d.ªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
d.ªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰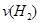 =
= 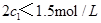 b.µ™∆¯µƒ◊™ªØ¬ £∫
b.µ™∆¯µƒ◊™ªØ¬ £∫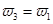 c.
c. 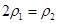 d.
d.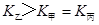
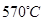 µƒµÁΩ‚≥ÿ£¨¿Ó”¬ƒÐÕ®π˝µƒ«‚¿Î◊”µƒ∂ýø◊Ã’¥…πÃÃÂ◊˜µÁΩ‚÷ £¨«‚∆¯∫Õµ™∆¯‘⁄µÁº´…œ∫œ≥…¡À∞±£¨◊™ªØ¬ ¥ÔµΩ78%£¨‘⁄µÁΩ‚∑®∫œ≥…∞±µƒπ˝≥Ã÷–£¨”¶Ω´N2≤ª∂œµÿÕ®»Î º´£¨∏√µÁº´∑¥”¶ ΩŒ™ °£
µƒµÁΩ‚≥ÿ£¨¿Ó”¬ƒÐÕ®π˝µƒ«‚¿Î◊”µƒ∂ýø◊Ã’¥…πÃÃÂ◊˜µÁΩ‚÷ £¨«‚∆¯∫Õµ™∆¯‘⁄µÁº´…œ∫œ≥…¡À∞±£¨◊™ªØ¬ ¥ÔµΩ78%£¨‘⁄µÁΩ‚∑®∫œ≥…∞±µƒπ˝≥Ã÷–£¨”¶Ω´N2≤ª∂œµÿÕ®»Î º´£¨∏√µÁº´∑¥”¶ ΩŒ™ °£ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2013-2014ƒ⁄√…π≈≥ý∑ –∏þ»˝œ¬—ß∆⁄4‘¬Õ≥“ªøº ‘¿Ì◊€ªØ—ß ‘æÌ£®Ω‚Œˆ∞Ê£© –գ∫ÃÓø’Â
£®14∑÷£©∫œ≥…∞± «»À¿ý—–æøµƒ÷ÿ“™øŒÃ‚£¨ƒø«∞𧓵∫œ≥…∞±µƒ‘≠¿ÌŒ™£∫
∫œ≥…∞± «»À¿ý—–æøµƒ÷ÿ“™øŒÃ‚£¨ƒø«∞𧓵∫œ≥…∞±µƒ‘≠¿ÌŒ™£∫
N2£®g£©+3H2£®g£© 2NH3£®g£©°˜H=-93.0kJ?mol-1£¨‘⁄3∏ˆ2Lµƒ√б’»ð∆˜÷–£¨ π”√œýÕ¨µƒ¥þªØº¡£¨∞¥≤ªÕ¨∑Ω ΩÕ∂»Î∑¥”¶ŒÔ£¨∑÷±Ω¯––∑¥”¶£∫
2NH3£®g£©°˜H=-93.0kJ?mol-1£¨‘⁄3∏ˆ2Lµƒ√б’»ð∆˜÷–£¨ π”√œýÕ¨µƒ¥þªØº¡£¨∞¥≤ªÕ¨∑Ω ΩÕ∂»Î∑¥”¶ŒÔ£¨∑÷±Ω¯––∑¥”¶£∫
œý≥÷∫„Œ¬°¢∫„»ð£¨≤‚µƒ∑¥”¶¥ÔµΩ∆Ω∫‚ ±πÿœµ ˝æð»Áœ¬£∫
»ð∆˜ | º◊ | ““ | ±˚ |
∑¥”¶ŒÔÕ∂»Î¡ø | 3molH2°¢2molN2 | 6molH2°¢4molN2 | 2mol NH3 |
¥ÔµΩ∆Ω∫‚µƒ ±º‰/min |
| 6 | 8 |
∆Ω∫‚ ± N2µƒÃª˝√Ð∂» | C1 | 1.5 |
|
ªÏ∫œ∆¯ÃÂ√Ð∂»/g°§L-1 |
|
|
|
∆Ω∫‚≥£ ˝/ L2°§mol-2 | Kº◊ | K““ | K±˚ |
£®1£©œ¬¡–∏˜œÓƒÐÀµ√˜∏√∑¥”¶“—µΩ¥Ô∆Ω∫‚◊¥Ã¨µƒ « £®ÃÓ–¥–Ú∫≈◊÷ƒ∏£©
a.»ð∆˜ƒ⁄H2°¢N2 °¢NH3µƒ≈®∂»÷ª±»Œ™1£∫3£∫2 b.»ð∆˜ƒ⁄—π«ø±£≥÷≤ª±‰
c. d.ªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
d.ªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
e.ªÏ∫œ∆¯Ãµƒ∆Ωæ˘œý∂‘∑÷◊”÷ ¡ø≤ª±‰
£®2£©»ð∆˜““÷–∑¥”¶¥”ø™ ºµΩ¥Ô∆Ω∫‚µƒ∑¥”¶ÀŸ∂»Œ™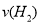 =
=
£®3£©‘⁄∏√Œ¬∂»œ¬º◊»ð∆˜÷–∑¥”¶µƒ∆Ω∫‚≥£ ˝K £®”√∫¨C1µƒ¥˙ ˝ Ω±Ì æ£©
£®4£©∑÷Œˆ…œ±Ì ˝æ𣨜¬¡–πÿœµ’˝»∑µƒ « £®ÃÓ–Ú∫≈£©£∫
a. b.µ™∆¯µƒ◊™ªØ¬ £∫
b.µ™∆¯µƒ◊™ªØ¬ £∫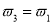 c.
c.  d.
d.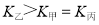
£®5£©¡Ìæð±®µ¿£¨≥£Œ¬°¢≥£—πœ¬£¨N2‘⁄≤Ù”–…Ÿ¡ø—ıªØÃ˙µƒ∂˛—ıªØÓ—¥þªØº¡±Ì√ʃДÎÀÆ∑¢…˙∑¥”¶£¨…˙≥…NH3∫ÕO2°£“—÷™£∫H2µƒ»º…’»»°˜H=-286KJ/mol£¨‘Ú”…¥Œ‘≠¿Ì÷∆NH3∑¥”¶µƒ»»ªØ—ß∑Ω≥Ã ΩŒ™
£®6£©œ£¿∞∞¢¿ÔÀπ∂ýµ¬¥Û—ßµƒGeorge Mamellos∫ÕMichacl Stoukides,∑¢√˜¡À“ª÷÷∫œ≥…∞±µƒ–¬∑Ω∑®£¨‘⁄≥£—πœ¬£¨∞—«‚∆¯∫Õ”√∞±∆¯œ° Õµƒµ™∆¯∑÷±Õ®»Î“ª∏ˆº”»»µΩ µƒµÁΩ‚≥ÿ£¨¿Ó”¬ƒÐÕ®π˝µƒ«‚¿Î◊”µƒ∂ýø◊Ã’¥…πÃÃÂ◊˜µÁΩ‚÷ £¨«‚∆¯∫Õµ™∆¯‘⁄µÁº´…œ∫œ≥…¡À∞±£¨◊™ªØ¬ ¥ÔµΩ78%£¨‘⁄µÁΩ‚∑®∫œ≥…∞±µƒπ˝≥Ã÷–£¨”¶Ω´N2≤ª∂œµÿÕ®»Î º´£¨∏√µÁº´∑¥”¶ ΩŒ™ °£
µƒµÁΩ‚≥ÿ£¨¿Ó”¬ƒÐÕ®π˝µƒ«‚¿Î◊”µƒ∂ýø◊Ã’¥…πÃÃÂ◊˜µÁΩ‚÷ £¨«‚∆¯∫Õµ™∆¯‘⁄µÁº´…œ∫œ≥…¡À∞±£¨◊™ªØ¬ ¥ÔµΩ78%£¨‘⁄µÁΩ‚∑®∫œ≥…∞±µƒπ˝≥Ã÷–£¨”¶Ω´N2≤ª∂œµÿÕ®»Î º´£¨∏√µÁº´∑¥”¶ ΩŒ™ °£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫ÃÓø’Â
 2NH3£®g£©°˜H=-93.0kJ?mol-1£¨‘⁄3∏ˆ2Lµƒ√б’»ð∆˜÷–£¨ π”√œýÕ¨µƒ¥þªØº¡£¨∞¥≤ªÕ¨∑Ω ΩÕ∂»Î∑¥”¶ŒÔ£¨∑÷±Ω¯––∑¥”¶£∫
2NH3£®g£©°˜H=-93.0kJ?mol-1£¨‘⁄3∏ˆ2Lµƒ√б’»ð∆˜÷–£¨ π”√œýÕ¨µƒ¥þªØº¡£¨∞¥≤ªÕ¨∑Ω ΩÕ∂»Î∑¥”¶ŒÔ£¨∑÷±Ω¯––∑¥”¶£∫| »ð∆˜ | º◊ | ““ | ±˚ |
| ∑¥”¶ŒÔÕ∂»Î¡ø | 3molH2°¢2molN2 | 6molH2°¢4molN2 | 2mol NH3 |
| ¥ÔµΩ∆Ω∫‚µƒ ±º‰/min | | 6 | 8 |
| ∆Ω∫‚ ± N2µƒÃª˝√Ð∂» | C1 | 1.5 | |
| ªÏ∫œ∆¯ÃÂ√Ð∂»/g°§L-1 |  |  | |
| ∆Ω∫‚≥£ ˝/ L2°§mol-2 | Kº◊ | K““ | K±˚ |
 d.ªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
d.ªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰ =
=  b.µ™∆¯µƒ◊™ªØ¬ £∫
b.µ™∆¯µƒ◊™ªØ¬ £∫ c.
c.  d.
d.
 µƒµÁΩ‚≥ÿ£¨¿Ó”¬ƒÐÕ®π˝µƒ«‚¿Î◊”µƒ∂ýø◊Ã’¥…πÃÃÂ◊˜µÁΩ‚÷ £¨«‚∆¯∫Õµ™∆¯‘⁄µÁº´…œ∫œ≥…¡À∞±£¨◊™ªØ¬ ¥ÔµΩ78%£¨‘⁄µÁΩ‚∑®∫œ≥…∞±µƒπ˝≥Ã÷–£¨”¶Ω´N2≤ª∂œµÿÕ®»Î º´£¨∏√µÁº´∑¥”¶ ΩŒ™ °£
µƒµÁΩ‚≥ÿ£¨¿Ó”¬ƒÐÕ®π˝µƒ«‚¿Î◊”µƒ∂ýø◊Ã’¥…πÃÃÂ◊˜µÁΩ‚÷ £¨«‚∆¯∫Õµ™∆¯‘⁄µÁº´…œ∫œ≥…¡À∞±£¨◊™ªØ¬ ¥ÔµΩ78%£¨‘⁄µÁΩ‚∑®∫œ≥…∞±µƒπ˝≥Ã÷–£¨”¶Ω´N2≤ª∂œµÿÕ®»Î º´£¨∏√µÁº´∑¥”¶ ΩŒ™ °£ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫¡…ƒ˛ °‘¬øºÃ‚ –գ∫ÃÓø’Â

 2NH3(g) °˜H < 0 £¨∆‰∆Ω∫‚≥£ ˝K”ÎŒ¬∂»Tµƒπÿœµ»Áœ¬±Ì£∫
2NH3(g) °˜H < 0 £¨∆‰∆Ω∫‚≥£ ˝K”ÎŒ¬∂»Tµƒπÿœµ»Áœ¬±Ì£∫
¢Ÿ∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô Ω£∫K= _____________
¢⁄ ‘≈–∂œK1 __________K2£®ÃÓ–¥°∞>°±£¨°∞=°±ªÚ°∞<°±£©
¢€œ¬¡–∏˜œÓƒÐÀµ√˜∏√∑¥”¶“—¥ÔµΩ∆Ω∫‚◊¥Ã¨µƒ «___________ £®ÃÓ◊÷ƒ∏£©
a£Æ»ð∆˜ƒ⁄N2°¢H2°¢NH3µƒ≈®∂»÷Ʊ»Œ™1°√3°√2
b£Æv(N2)’˝ = 3v(H2)ƒÊ
c£Æ»ð∆˜ƒ⁄—π«ø±£≥÷≤ª±‰
d£ÆªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
£®3£©∂‘∑¥”¶N2O4(g) 2NO2(g) °˜H > 0 £¨‘⁄Œ¬∂»∑÷±Œ™T1°¢T2 ±£¨∆Ω∫‚ÃÂœµ÷–NO2µƒÃª˝∑÷ ˝ÀÊ—π«ø±‰ªØ«˙œþ»Áœ¬ÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «______________ °£
2NO2(g) °˜H > 0 £¨‘⁄Œ¬∂»∑÷±Œ™T1°¢T2 ±£¨∆Ω∫‚ÃÂœµ÷–NO2µƒÃª˝∑÷ ˝ÀÊ—π«ø±‰ªØ«˙œþ»Áœ¬ÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «______________ °£

ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫¡…ƒ˛ °…Ú—Ù∂˛÷–2011£≠2012—߃Í∏þ∂˛…œ—ß∆⁄12‘¬‘¬øºªØ—ß ‘ –գ∫022
µ™ «µÿ«Ú…œ∫¨¡ø∑·∏ªµƒ“ª÷÷‘™Àÿ
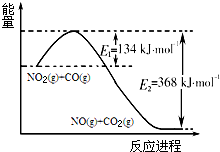
£¨µ™‘™Àÿµƒµ•÷ º∞∆‰ªØ∫œŒÔ‘⁄π§≈©“µ…˙≤˙°¢…˙ªÓ÷–”–◊≈÷ÿ“™◊˜”√£Æ(1)∏˘æðœ¬≤ýƒÐ¡ø±‰ªØ æ“‚Õº£¨«Î–¥≥ˆNO2∫ÕCO∑¥”¶µƒ»»ªØ—ß∑Ω≥à Ω________£Æ

(2)‘⁄πÃ∂®Ãª˝µƒ√б’»ð∆˜÷–£¨Ω¯––»Áœ¬ªØ—ß∑¥”¶£∫
N2(g)£´3H2(g)![]() 2NH3(g)°°¶§H£º0£¨
2NH3(g)°°¶§H£º0£¨
∆‰∆Ω∫‚≥£ ˝K”ÎŒ¬∂»Tµƒπÿœµ»Áœ¬±Ì£∫

¢Ÿ∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô Ω£∫K£Ω________
¢⁄ ‘≈–∂œK1________K2(ÃÓ–¥°∞£æ°±£¨°∞£Ω°±ªÚ°∞£º°±)
¢€œ¬¡–∏˜œÓƒÐÀµ√˜∏√∑¥”¶“—¥ÔµΩ∆Ω∫‚◊¥Ã¨µƒ «________(ÃÓ◊÷ƒ∏)
a£Æ»ð∆˜ƒ⁄N2°¢H2°¢NH3µƒ≈®∂»÷Ʊ»Œ™1°√3°√2
b£Æv(N2)’˝£Ω3v(H2)ƒÊ
c£Æ»ð∆˜ƒ⁄—π«ø±£≥÷≤ª±‰
d£ÆªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
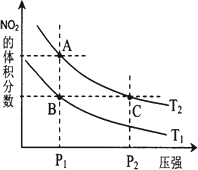
(3)∂‘∑¥”¶N2O4(g)![]() 2NO2(g)°°¶§H£æ0£¨‘⁄Œ¬∂»∑÷±Œ™T1°¢T2 ±£¨∆Ω∫‚ÃÂœµ÷–NO2µƒÃª˝∑÷ ˝ÀÊ—π«ø±‰ªØ«˙œþ»Áœ¬ÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «________£Æ
2NO2(g)°°¶§H£æ0£¨‘⁄Œ¬∂»∑÷±Œ™T1°¢T2 ±£¨∆Ω∫‚ÃÂœµ÷–NO2µƒÃª˝∑÷ ˝ÀÊ—π«ø±‰ªØ«˙œþ»Áœ¬ÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «________£Æ

a£ÆA°¢C¡Ωµ„µƒ∑¥”¶ÀŸ¬ £∫A£æC
b£ÆA°¢C¡Ωµ„µƒªØ—ß∆Ω∫‚≥£ ˝£∫A£æC
c£ÆA°¢C¡Ωµ„N2O4µƒ◊™ªØ¬ £∫A£æC
d£Æ”…◊¥Ã¨BµΩ◊¥Ã¨A£¨ø…“‘”√º”»»µƒ∑Ω∑®
(4)“ª∂®Œ¬∂»œ¬£¨‘⁄1 L√б’»ð∆˜÷–≥‰»Î1 mol°°N2∫Õ3 mol°°H2≤¢∑¢…˙∑¥”¶£Æ»Ù»ð∆˜»ðª˝∫„∂®£¨10 min¥ÔµΩ∆Ω∫‚ ±£¨∆¯Ãµƒ◊ÐŒÔ÷ µƒ¡øŒ™‘≠¿¥µƒ7/8£¨‘ÚN2µƒ◊™ªØ¬ a(N2)£Ω________£¨“‘NH3±Ì æ∏√π˝≥õƒ∑¥”¶ÀŸ¬ v(NH3)£Ω________£Æ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫∫⁄¡˙Ω≠ °¥Û«ÏÃ˙»À÷–—ß2012ΩÏ∏þ»˝…œ—ß∆⁄∆⁄ƒ©øº ‘ªØ—ß ‘ –գ∫058
µ™ «µÿ«Ú…œ∫¨¡ø∑·∏ªµƒ“ª÷÷‘™Àÿ£¨µ™‘™Àÿµƒµ•÷ º∞∆‰ªØ∫œŒÔ‘⁄π§≈©“µ…˙≤˙°¢…˙ªÓ÷–”–◊≈÷ÿ“™◊˜”√£Æ
(1)∏˘æðœ¬≤ýƒÐ¡ø±‰ªØ æ“‚Õº£¨«Î–¥≥ˆNO2∫ÕCO∑¥”¶µƒ»»ªØ—ß∑Ω≥à Ω________£Æ

(2)‘⁄πÃ∂®Ãª˝µƒ√б’»ð∆˜÷–£¨Ω¯––»Áœ¬ªØ—ß∑¥”¶£∫
N2(g)£´3H2(g)![]() 2NH3(g)°°¶§H£º0£¨∆‰∆Ω∫‚≥£ ˝K”ÎŒ¬∂»Tµƒπÿœµ»Áœ¬±Ì£∫
2NH3(g)°°¶§H£º0£¨∆‰∆Ω∫‚≥£ ˝K”ÎŒ¬∂»Tµƒπÿœµ»Áœ¬±Ì£∫

¢Ÿ∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô Ω£∫K£Ω________£Æ
¢⁄ ‘≈–∂œK1________K2(ÃÓ–¥°∞£æ°±£¨°∞£Ω°±ªÚ°∞£º°±)£Æ
¢€œ¬¡–∏˜œÓƒÐÀµ√˜∏√∑¥”¶“—¥ÔµΩ∆Ω∫‚◊¥Ã¨µƒ «________(ÃÓ◊÷ƒ∏)£Æ
a£Æ»ð∆˜ƒ⁄N2°¢H2°¢NH3µƒ≈®∂»÷Ʊ»Œ™1°√3°√2
b£Æv(N2)’˝£Ω3v(H2)ƒÊ
c£Æ»ð∆˜ƒ⁄—π«ø±£≥÷≤ª±‰
d£ÆªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
(3)∂‘∑¥”¶N2O4(g)![]() 2NO2(g)°°¶§H£æ0£¨‘⁄Œ¬∂»∑÷±Œ™T1°¢T2 ±£¨∆Ω∫‚ÃÂœµ÷–NO2µƒÃª˝∑÷ ˝ÀÊ—π«ø±‰ªØ«˙œþ»ÁÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «________£Æ
2NO2(g)°°¶§H£æ0£¨‘⁄Œ¬∂»∑÷±Œ™T1°¢T2 ±£¨∆Ω∫‚ÃÂœµ÷–NO2µƒÃª˝∑÷ ˝ÀÊ—π«ø±‰ªØ«˙œþ»ÁÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «________£Æ
a£ÆA°¢C¡Ωµ„µƒ∑¥”¶ÀŸ¬ £∫A£æC
b£ÆA°¢C¡Ωµ„µƒªØ—ß∆Ω∫‚≥£ ˝£∫A£æC
c£ÆA°¢C¡Ωµ„N2O4µƒ◊™ªØ¬ £∫A£æC
d£Æ”…◊¥Ã¨BµΩ◊¥Ã¨A£¨ø…“‘”√º”»»µƒ∑Ω∑®
(4)“ª∂®Œ¬∂»œ¬£¨‘⁄1 L√б’»ð∆˜÷–≥‰»Î1 mol°°N2∫Õ3 mol°°H2≤¢∑¢…˙∑¥”¶£Æ»Ù»ð∆˜»ðª˝∫„∂®£¨10 min¥ÔµΩ∆Ω∫‚ ±£¨∆¯Ãµƒ◊ÐŒÔ÷ µƒ¡øŒ™‘≠¿¥µƒ7/8£¨‘ÚN2µƒ◊™ªØ¬ a(N2)£Ω________£¨“‘NH3±Ì æ∏√π˝≥õƒ∑¥”¶ÀŸ¬ v(NH3)£Ω________£Æ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
 µ™ «µÿ«Ú…œ∫¨¡ø∑·∏ªµƒ“ª÷÷‘™Àÿ£¨µ™‘™Àÿµƒµ•÷ º∞∆‰ªØ∫œŒÔ‘⁄π§≈©“µ…˙≤˙°¢…˙ªÓ÷–”–◊≈÷ÿ“™◊˜”√£Æ
µ™ «µÿ«Ú…œ∫¨¡ø∑·∏ªµƒ“ª÷÷‘™Àÿ£¨µ™‘™Àÿµƒµ•÷ º∞∆‰ªØ∫œŒÔ‘⁄π§≈©“µ…˙≤˙°¢…˙ªÓ÷–”–◊≈÷ÿ“™◊˜”√£Æ| T/K | 298 | 398 | 498 |
| ∆Ω∫‚≥£ ˝K | 4.1°¡106 | K1 | K2 |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com