
| 在短周期元素组成的化合物中,若其原子个数比为1:2,设两种元素的原子序数分别为a 和b,则下列对a和b可能关系的概括中,正确的是( )? ①a+b=15 ②a=b+6 ③a=b-5 ④a+b=22?
|
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:问答题
| A.①③ | B.①③④ | C.①②③④ | D.①②④? |
科目:高中化学 来源:2010-2011学年浙江省绍兴市越城区稽山中学高一(下)模块检测化学试卷(一)(必修2)(解析版) 题型:选择题
科目:高中化学 来源: 题型:
在短周期元素组成的化合物中,若其原子个数比为1∶2,设两种元素的原子序数分别为a 和b,则下列对a和b可能关系的概括中,正确的是( )
①a+b=15 ②a=b+6 ③a=b-5 ④a+b=22
A. ①③ B. ①③④ C. ①②③④ D. ①②④
科目:高中化学 来源: 题型:
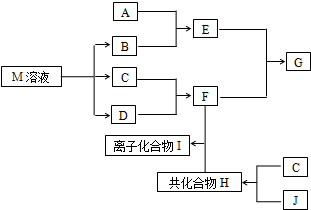 短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则:
短周期元素的单质C、D、J在通常状况下均为气态,且常见双原子单质分子,J分子共价键最多;H分子中含10个电子;物质M由同一短周期的X、Y两种元素组成,X原子最外层电子数是最内层电子数的1/2,Y元素最高正价与它的负价代数和为6.M与其它物质的转化关系如图(部分产物及反应条件已略去)则: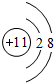
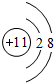
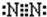
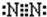
科目:高中化学 来源: 题型:


| 2b |
| a |
| 2b |
| a |
科目:高中化学 来源: 题型:
 短周期元素E、F的离子F+与E2-核外电子排布相同,B、D、E元素的原子序数依次递增,B原子的每个能级上电子数相等,BE2和D2E是等电子体、A是F所在周期非金属性最强的元素,G.E同主族且原子核外电子层数相差两层,
短周期元素E、F的离子F+与E2-核外电子排布相同,B、D、E元素的原子序数依次递增,B原子的每个能级上电子数相等,BE2和D2E是等电子体、A是F所在周期非金属性最强的元素,G.E同主族且原子核外电子层数相差两层,科目:高中化学 来源: 题型:
X | Y | Z |
(1)氢元素与Z形成原子个数比为1∶1的化合物,其电子式为___________。该化合物分子中存在___________(填“共价键”或“离子键”)。
(2)Y最高价氧化物的水化物与Y的氢化物恰好完全反应时,生成物的水溶液呈酸性,其原因是___________________________________________;该溶液中各种离子浓度由大到小顺序为______________________________________________。
(3)恒温恒容下,2 mol H2与2 mol Y的单质反应,达到平衡时,Y的单质为1.8 mol,H2的转化率为__________;若该反应在恒温恒压条件下进行(其他条件相同),反应达到平衡时,H2的转化率比上述条件下H2的转化率__________(填“大”“小”或“相同”)。
(4)由X的最简单气态氢化物、Z的单质和KOH溶液组成的新型燃料电池中,正极上发生反应的电极反应式为____________________________________。
科目:高中化学 来源:2011-2012学年甘肃省兰州一中高一下学期期末考试化学试卷(带解析) 题型:填空题
(10分)短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外第三层电子数目比第一层多1个,C―比A元素的离子多1个电子层,D元素的原子核外第二层比第一层多2个电子。回答下列问题:
(1)A元素的名称是_______;
(2)C―的结构示意图为 ;D元素在周期表中的位置是__________;
(3)元素D的气态氢化物的电子式为____,其分子的结构特点是具有_____结构,在一定条件下该氢化物可与单质C发生取代反应,若将等物质的量的该氢化物与单质C混合,在一定条件下充分反应后,生成物中物质的量最大的是_______(用化学式填写);
(4)工业上冶炼单质A的化学方程式为_____________________________________;
(5)工业上常用单质B冶炼难熔的金属,写出氧化铁和单质B在高温下反应的化学方程式_______,若反应中有0.25mol氧化铁参加反应反应中转移电子的个数为__________;
(6)若将单质A、B用导线连接插入到氢氧化钠溶液中可以组成原电池,则正极材
料是_______(用化学式填写),负极电极反应是___________________________________。
科目:高中化学 来源:2014届甘肃省高一下学期期末考试化学试卷(解析版) 题型:填空题
(10分) 短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外第三层电子数目比第一层多1个,C―比A元素的离子多1个电子层,D元素的原子核外第二层比第一层多2个电子。回答下列问题:
(1)A元素的名称是_______;
(2)C―的结构示意图为 ;D元素在周期表中的位置是__________;
(3)元素D的气态氢化物的电子式为____,其分子的结构特点是具有_____结构,在一定条件下该氢化物可与单质C发生取代反应,若将等物质的量的该氢化物与单质C混合,在一定条件下充分反应后,生成物中物质的量最大的是_______(用化学式填写);
(4)工业上冶炼单质A的化学方程式为_____________________________________;
(5)工业上常用单质B冶炼难熔的金属,写出氧化铁和单质B在高温下反应的化学方程式_______,若反应中有0.25mol氧化铁参加反应反应中转移电子的个数为__________;
(6)若将单质A、B用导线连接插入到氢氧化钠溶液中可以组成原电池,则正极材
料是_______(用化学式填写),负极电极反应是___________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com