
合成氨的反应为:3H2+N2  2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol?L-1?s-1),则下列关系正确的是( )
|
科目:高中化学 来源: 题型:
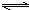 2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol?L-1?s-1),则下列关系正确的是( )
2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol?L-1?s-1),则下列关系正确的是( )科目:高中化学 来源: 题型:
合成氨的反应为:3H2+ N2 2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1),则下列关系正确的是
A、v(H2)=v(N2) = v(NH3) B、v(H2)=3 v(N2) C、v(N2)=2 v(NH3) D、2v(NH3)=3v(H2)
科目:高中化学 来源:2014届四川省高一下学期期中考试化学试卷(解析版) 题型:选择题
合成氨的反应为:3H2
+ N2  2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1),则下列关系正确的是
2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1),则下列关系正确的是
A、v(H2)=v(N2) = v(NH3) B、v(H2)=3 v(N2) C、v(N2)=2 v(NH3) D、2v(NH3)=3v(H2)
科目:高中化学 来源:不详 题型:单选题

| A.v(H2)=v(N2)=v(NH3) | B.v(H2)=3v(N2) | ||
| C.v(N2)=2v(NH3) | D.v(NH3)=
|
科目:高中化学 来源:2012-2013学年山东省聊城市莘县莘州中学高二(上)期中化学试卷(解析版) 题型:选择题
 2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3),则下列关系正确的是( )
2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3),则下列关系正确的是( ) v(H2)
v(H2)科目:高中化学 来源:《第2章 化学反应与能量》2011年单元测试卷(宝鸡市金台区)(解析版) 题型:选择题
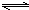 2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3),则下列关系正确的是( )
2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3),则下列关系正确的是( ) v(H2)
v(H2)科目:高中化学 来源: 题型:
合成氨的反应为:3H2 + N2 ![]() 2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol?L-1?s-1),则下列关系正确的是 ( )
2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol?L-1?s-1),则下列关系正确的是 ( )
![]() A.v(H2)=v(N2)= v(NH3) B. v(H2)=3v(N2)
A.v(H2)=v(N2)= v(NH3) B. v(H2)=3v(N2)
![]() C.v(N2)=2v(NH3) D. v(NH3)=3/2v(H2)
C.v(N2)=2v(NH3) D. v(NH3)=3/2v(H2)
科目:高中化学 来源:模拟题 题型:填空题
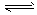 2NH3(g)
2NH3(g) 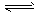 CO2(g) +H2(g) △H>0。
CO2(g) +H2(g) △H>0。 
科目:高中化学 来源: 题型:
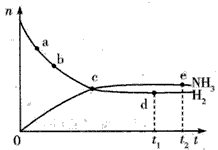
(13分)工业合成氨是硝酸工业中的重要步骤,已知N2(g) +3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1。请回答:
(1) 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示。

图中t1时引起平衡移动的条件可能是 __ , t3时引起平衡移动的条件可能是 __ ___ , 其中表示平衡混合物 中NH3的含量最高的一段时间是 。
(2) 温度为T ℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪。则该反应的化学平衡常数的值为 ___________________。请在答题卷上写出具体的计算过程。
科目:高中化学 来源:2011-2012学年广东省实验中学高二上学期期中考试化学试卷 题型:填空题
(13分)工业合成氨是硝酸工业中的重要步骤,已知N2(g) +3H2(g)  2NH3(g) ΔH=-92.4kJ·mol-1。请回答:
2NH3(g) ΔH=-92.4kJ·mol-1。请回答:
(1) 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、 H2和NH3的量),反应速率与时间的关系如右图所示。
H2和NH3的量),反应速率与时间的关系如右图所示。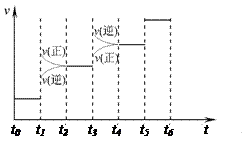
图中t1时引起平衡移动的条件可能是 __ , t3时引起平衡移动的条件可能是 __ ___ , 其中表示平衡混合物中NH3的含量最高的一段时间是 。
(2) 温度为T ℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪。则该反应的化学平衡常数的值为 ___________________。请在答题卷上写出具体的计算过程。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com