
| 一定温度下,向体积为2L的恒容密闭容器中充入1mol PCl5(g),发生反应: PCl5(g)?PCl3(g)+Cl2(g)△H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示.下列说法正确的是( )
 |
科目:高中化学 来源:2012-2013学年四川省达州市高三第一次诊断性考试理综化学试卷(解析版) 题型:选择题
一定温度下,向体积为2L的恒容密闭容器中充入1mol
PCl5(g),发生反应:PCl5(g) PCl3(g)+Cl2(g)
△H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是( )
PCl3(g)+Cl2(g)
△H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是( )
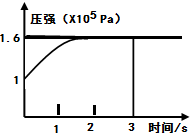
A、3s内的平均速率为:V(PCl3)=0.1mol·L-1·min-1
B、达到平衡时放出0.6QKJ热量
C、其他条件不变,再向容器中充入1molPCl5(g),则达新平衡 时,C(PCl5)>0.4mol·L-1
D、其他条件不变,增大PCl5的浓度,平衡常数减小
科目:高中化学 来源: 题型:单选题
一定温度下,向体积为2L的恒容密闭容器中充入1mol PCl5(g),发生反应:PCl5(g) PCl3(g)+Cl2(g) △H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是( )
PCl3(g)+Cl2(g) △H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是( )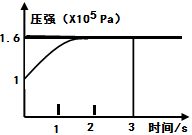
| A.3s内的平均速率为:V(PCl3)=0.1mol·L-1·min-1 |
| B.达到平衡时放出0.6QKJ热量 |
| C.其他条件不变,再向容器中充入1molPCl5(g),则达新平衡 时,C(PCl5)>0.4mol·L-1 |
| D.其他条件不变,增大PCl5的浓度,平衡常数减小 |
科目:高中化学 来源:达州一模 题型:单选题
| A.3s内的平均速率为:V(PCl3)=0.1mol?L-1?min-1 |
| B.达到平衡时放出0.6QKJ热量 |
| C.其他条件不变,再向容器中充入1molPCl5(g),则达新平衡时,C(PCl5)>0.4mol?L-1 |
| D.其他条件不变,增大PCl5的浓度,平衡常数减小 |

科目:高中化学 来源:2013年四川省达州市高考化学一诊试卷(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题
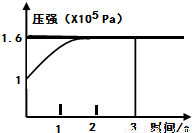
 PCl3(g)+Cl2(g) △H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是( )
PCl3(g)+Cl2(g) △H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是( )
| A.3s内的平均速率为:V(PCl3)=0.1mol·L-1·min-1 |
| B.达到平衡时放出0.6QKJ热量 |
| C.其他条件不变,再向容器中充入1molPCl5(g),则达新平衡 时,C(PCl5)>0.4mol·L-1 |
| D.其他条件不变,增大PCl5的浓度,平衡常数减小 |
科目:高中化学 来源: 题型:
 (2013?达州模拟)一定温度下,向体积为2L的恒容密闭容器中充入1mol PCl5(g),发生反应:
(2013?达州模拟)一定温度下,向体积为2L的恒容密闭容器中充入1mol PCl5(g),发生反应:科目:高中化学 来源: 题型:阅读理解
科目:高中化学 来源:2012-2013学年陕西省宝鸡市高三教学质量检测(二)理综化学试卷(解析版) 题型:填空题
已知体积为2L的恒容密闭容器中发生反应: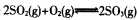 ,请根据化学反应的有关原理同答下列问题
,请根据化学反应的有关原理同答下列问题
(1)一定条件下,充入2 mol SO2(g)和2 mol O2(g),20 s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为____,此时,该密闭容器内混合气体的压强是反应前的____倍。
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)____。
①
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④各气体的浓度都不再发生变化
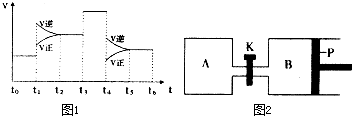
(3)下图表示该反应的速率(v)随时间(t)的变化的关系。则下列不同时间段中,SO3的百分含量最高的是( )
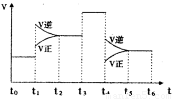

据图分析:你认为t3时改变的外界条件可能是 ;
t6时保持体积不变向体系中充人少量SO3,再次平衡后
SO2的体积百分含量比t6时 (填“大”\“小”或“等于”)。
(4)下图中P是可自由平行滑动的活塞。在相同温度时,向A容器中充入4 mol SO3(g),关闭K,向B容器中充入2 mol SO3(g),两容器分别发生反应。

已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体积为1.2a L,容器B中SO3转
化率为____
②若打开K,一段时间后重新达到平衡,容器B的体积为 __L(连通管中气体体积忽略不计,且不考虑温度的影响)。
(5)已知单质硫的燃烧热为△H=-296kJ/mol,经测定由S(s)生成120gSO3(g)可放热592.5kJ,请写出SO2(g)氧化生成SO3(g)的热化学方程式____。
科目:高中化学 来源:2012-2013学年浙江省宁波市十校联考理综化学试卷(解析版) 题型:选择题
Ⅰ.800℃时,向容积为2L的恒容密闭容器中充入一定量的CO和H2O维持恒温,发生反应CO(g)+H2O(g) H2(g)+CO2(g),反应过程中测定的部分数据见下表:
H2(g)+CO2(g),反应过程中测定的部分数据见下表:
|
反应时间/min |
0 |
2 |
4 |
6 |
|
n(CO)/mol |
1.20 |
0.90 |
|
0.80 |
|
n(H2O)/ mol |
0.60 |
|
0.20 |
|
①反应在2 min内的平均速率为v(H2O)=___________;
②800℃时,化学平衡常数K的值为_______________;
③保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率______(填“增大”或“减小”或“不变”)。
④在恒温恒压密闭容器中通入CO和H2O各1 mol发生该反应,当反应达到平衡后,维持温度与压强不变,t1时再通入各1 mol的CO和H2O的混合气体,请在右图中画出正(v正)、逆(v逆)反应速率在t1后随时间t变化的曲线图。

Ⅱ.实验室中利用复分解反应制取Mg(OH)2。实验数据和现象如下表所示(溶液体积均取用1mL):
|
组别 |
药品1 |
药品2 |
实验现象 |
|
I |
0.01 mol/L NaOH溶液 |
0.01 mol/L MgCl2溶液 |
生成白色沉淀 |
|
II |
0.01 mol/L氨水 |
0.01 mol/L MgCl2溶液 |
无现象 |
|
III |
0.1 mol/L氨水 |
0.1 mol/L MgCl2溶液 |
现象III |
|
IV |
0.1 mol/L氨水 |
0.01 mol/L MgCl2溶液 |
生成白色沉淀 |
|
V |
0.01 mol/L氨水 |
0.1 mol/L MgCl2溶液 |
无现象 |
①现象III是 ;
②如果向0.028 mol/L的MgCl2溶液中加入等体积的NaOH溶液,请计算NaOH溶液的浓度至少达到
mol/L时,溶液中开始出现白色沉淀(Ksp(Mg(OH)2)= 5.6×10-12)。
③MgCl2溶液和氨水混合后存在下列化学平衡:Mg2+(aq)
+ 2NH3·H2O(aq) 2NH4+(aq)
+ Mg(OH)2(s)该反应化学平衡常数的表达式为K=
,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式
。
2NH4+(aq)
+ Mg(OH)2(s)该反应化学平衡常数的表达式为K=
,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式
。
科目:高中化学 来源: 题型:填空题
已知体积为2L的恒容密闭容器中发生反应: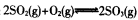 ,请根据化学反应的有关原理同答下列问题
,请根据化学反应的有关原理同答下列问题
(1)一定条件下,充入2 mol SO2(g)和2 mol O2(g),20 s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为____,此时,该密闭容器内混合气体的压强是反应前的____倍。
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)____。
①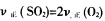
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④各气体的浓度都不再发生变化
(3)下图表示该反应的速率(v)随时间(t)的变化的关系。则下列不同时间段中,SO3的百分含量最高的是( )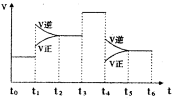

据图分析:你认为t3时改变的外界条件可能是 ;
t6时保持体积不变向体系中充人少量SO3,再次平衡后
SO2的体积百分含量比t6时 (填“大”\“小”或“等于”)。
(4)下图中P是可自由平行滑动的活塞。在相同温度时,向A容器中充入4 mol SO3(g),关闭K,向B容器中充入2 mol SO3(g),两容器分别发生反应。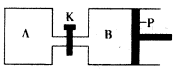
已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体积为1.2a L,容器B中SO3转
化率为____
②若打开K,一段时间后重新达到平衡,容器B的体积为 __L(连通管中气体体积忽略不计,且不考虑温度的影响)。
(5)已知单质硫的燃烧热为△H=-296kJ/mol,经测定由S(s)生成120gSO3(g)可放热592.5kJ,请写出SO2(g)氧化生成SO3(g)的热化学方程式____。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com