二甲醚(CH3OCH3)和乙醇(CH3CH2OH)分子式相同,是同分异构体,但乙醇的沸点比二甲醚高,其原因是( )| A.乙醇的相对分子质量比二甲醚的大 | | B.乙醇分子内化学键牢固 | | C.乙醇分子间形成了氢键 | | D.乙醇分子在水溶液中电离出OH- |
|
相关习题
科目:高中化学
来源:
题型:
二甲醚(CH3OCH3)和乙醇(CH3CH2OH)分子式相同,是同分异构体,但乙醇的沸点比二甲醚高,其原因是( )
查看答案和解析>>
科目:高中化学
来源:不详
题型:单选题
二甲醚(CH
3OCH
3)和乙醇(CH
3CH
2OH)分子式相同,是同分异构体,但乙醇的沸点比二甲醚高,其原因是( )
| A.乙醇的相对分子质量比二甲醚的大 |
| B.乙醇分子内化学键牢固 |
| C.乙醇分子间形成了氢键 |
| D.乙醇分子在水溶液中电离出OH- |
查看答案和解析>>
科目:高中化学
来源:2010-2011学年高一(下)期中化学试卷(文科)(解析版)
题型:选择题
二甲醚(CH3OCH3)和乙醇(CH3CH2OH)分子式相同,是同分异构体,但乙醇的沸点比二甲醚高,其原因是( )
A.乙醇的相对分子质量比二甲醚的大
B.乙醇分子内化学键牢固
C.乙醇分子间形成了氢键
D.乙醇分子在水溶液中电离出OH-
查看答案和解析>>
科目:高中化学
来源:模拟题
题型:填空题
“C1化学”是指以分子中只含一个碳原子的物质为原料进行物质合成的化学。“C1化学”对于缓解日益 严重的能源危机、合理利用煤和天然气等化石燃料、保护环境等都有非常重要的意义。合成气(CO+H2)是 “C1化学”中的常用原料。
(1)煤气化可生成合成气,该反应的化学方程式为____________________,用该方法生产合成气的一个典型缺陷是___________。
(2)将甲烷氧化可制合成气:CH4(g)+1/2O2(g)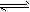 CO(g)+2H2(g) △H=-35.6 kJ/mol。该反应是_____(填“自发”或“非自发”)反应。
CO(g)+2H2(g) △H=-35.6 kJ/mol。该反应是_____(填“自发”或“非自发”)反应。
(3)通过乙醇制取合成气具有良好的应用前景。由乙醇制取合成气有如下两条路线:
a.水蒸气催化重整:CH3CH2OH(g)+H2O(g)→4H2(g)+2CO(g) △H=+255.58 kJ/mol
b.部分催化氧化:CH3CH2OH(g)+1/2O2(g)→ 3H2(g)+2CO(g) △H=+13.76 kJ/mol
下列说法错误的是____。
A.从原料消耗的角度来看,a路线制氢更有价值
B.从能量消耗的角度来看,b路线制氢更加有利
C.a路线制氢由于要消耗很多能量,所以在实际生产中意义不大
D.在以上两个反应中,原子利用率较高的是b反应
(4)工业用合成气制备二甲醚的生产流程如下:
催化反应室中(压力2.0~ 10.0 MPa,温度230~ 280℃)进行下列反应:
CO(g)+2H
2(g)
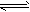
CH
3OH(g) △H=-90.7 kJ/mol ①
2CH
3OH(g)
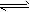
CH
3OCH
3(g)+H
2O(g) △H = -23.5 kJ/mol ②
CO(g) +H
2O(g)
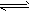
CO
2(g)+H
2(g) △H=-41.2 kJ/mol ③
①催化反应室中总反应3CO(g)+3H
2(g)
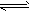
CH
3OCH
3(g)+CO
2(g)的△H=_____。830℃ 时反应③的K=1.0,则在催化反应室中反应③的K_______(填“>”、“<”或“=”)1.0。
②上述流程中,可以循环使用的物质有____________。
查看答案和解析>>
科目:高中化学
来源:2014高考化学名师高考模拟演练练习卷(A)(解析版)
题型:填空题
(2013山东临沂一模)(15分)碳是形成化合物种类最多的元素。
(1)CH2 CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为 (填最简整数比),写出该分子中所有碳原子的杂化方式 。
CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为 (填最简整数比),写出该分子中所有碳原子的杂化方式 。
(2)乙醇(CH3CH2OH)与二甲醚(CH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是 。
(3)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为 。
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能,右图所示的碳化硅的晶胞(其中 为碳原子,
为碳原子, 为硅原子)。每个碳原子周围与其距离最近的硅原子有 个。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为 (用含a、b的式子表示)。
为硅原子)。每个碳原子周围与其距离最近的硅原子有 个。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为 (用含a、b的式子表示)。
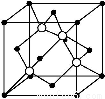
查看答案和解析>>
科目:高中化学
来源:不详
题型:填空题
(2013山东临沂一模)(15分)碳是形成化合物种类最多的元素。
(1)CH
2
CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为
(填最简整数比),写出该分子中所有碳原子的杂化方式
。
(2)乙醇(CH
3CH
2OH)与二甲醚(CH
3OCH
3)的分子式均为C
2H
6O,但CH
3CH
2OH的沸点高于CH
3OCH
3的沸点,其原因是
。
(3)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为
。
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能,右图所示的碳化硅的晶胞(其中

为碳原子,

为硅原子)。每个碳原子周围与其距离最近的硅原子有
个。设晶胞边长为a cm,密度为b g/cm
3,则阿伏加德罗常数可表示为
(用含a、b的式子表示)。

查看答案和解析>>
科目:高中化学
来源:2013年山东省临沂市高考化学一模试卷(解析版)
题型:解答题
【化学--物质结构与性质】
碳是形成化合物种类最多的元素.
(1)CH
2=CH-C≡N是制备晴纶的原料,其分子中σ键和π键的个数之比为______(填最简整数比),写出该分子中所有碳原子的杂化方式______.
(2)乙醇(CH
3CH
2OH)与二甲醚(OH
3OCH
3)的分子式均为C
2H
6O,但CH
3CH
2OH的沸点高于CH
3OCH
3的沸点,其原因是______.
(3)某元素位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为______.
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能.如图所示为碳化硅的晶胞(其中●为碳原子,○为硅原子).每个碳原子周围与其距离最近的硅原子有______个.设晶胞边长为a cm,密度为b g/cm
3,则阿伏加德罗常数可表示为______(用含a、b的式子表示).

查看答案和解析>>
科目:高中化学
来源:
题型:
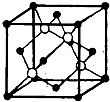
(2013?临沂一模)【化学--物质结构与性质】
碳是形成化合物种类最多的元素.
(1)CH
2=CH-C≡N是制备晴纶的原料,其分子中σ键和π键的个数之比为
2:1
2:1
(填最简整数比),写出该分子中所有碳原子的杂化方式
sp2、sp
sp2、sp
.
(2)乙醇(CH
3CH
2OH)与二甲醚(OH
3OCH
3)的分子式均为C
2H
6O,但CH
3CH
2OH的沸点高于CH
3OCH
3的沸点,其原因是
乙醇分子之间形成氢键
乙醇分子之间形成氢键
.
(3)某元素位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为
3d84s2
3d84s2
.
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能.如图所示为碳化硅的晶胞(其中●为碳原子,○为硅原子).每个碳原子周围与其距离最近的硅原子有
4
4
个.设晶胞边长为a cm,密度为b g/cm
3,则阿伏加德罗常数可表示为
(用含a、b的式子表示).
查看答案和解析>>
科目:高中化学
来源:陕西省模拟题
题型:填空题
Ⅰ.描述弱电解质电离情况可以用电离度(电离度:一定条件下,当弱电解质达到电离平衡时,溶液中已电离的电解质分子数占原电解质分子总数的百分数)和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp)。
请回答下面问题:
⑴下列能使醋酸溶液中CH
3COOH的电离度增大,而电离常数不变的操作是_______(填序号)。
A.升高温度 B.加水稀释 C.加少量的CH
3COONa固体 D.加少量冰醋酸
⑵CH
3COONH
4的水溶液呈______(选填“酸性”、“中性”、“碱性”),理由是____________________。
⑶工业中常将BaSO
4转化为BaCO
3后,再将其制成各种可溶性的钡盐(如:BaCl
2)。具体做法是用饱和的纯碱溶液浸泡BaSO
4粉末,并不断补充纯碱,最后BaSO
4转化为BaCO
3。现有足量的BaSO
4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使c(SO
42- )达到0.0l mol/L以上,则溶液中c(CO
32- )应≥_______ mol/L。
Ⅱ.化学在能源开发与利用中起着重要的作用,如甲醇、乙醇、二甲醚(CH
3OCH
3)等都是新型燃料。
⑴乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇。
2CO
2(g)+6H
2(g)

CH
3CH
2OH(g)+3H
2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。
根据表中数据分析:
①上述反应的 a_______0(填“大于”或“小于”)。
②在一定温度下,提高氢碳(即n(H2)/n(CO2) )比,平衡常数K值_______(填“增大”、“减小”、或“不变”),对生成乙醇______(填“有利”或“不利”)。
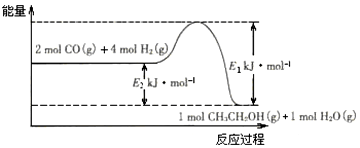
⑵催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应)。该反应过程中能量变化如图所示:
①写出CO和H2制备乙醇的热化学反应方程式_________________。
②在一定温度下,向上述密闭容器中加入1 mol CO、3 mol H2及固体催化剂,使之反应。平衡时,反应产生的热量为Q kJ,若温度不变的条件下,向上述密闭容器中加入4 mol CO、
12 mol H2及固体催化剂,平衡时,反应产生的热量为w kJ,则w的范围为___________。
⑶二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效的优良性能。以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池,其工作原理与甲烷燃料电池原理相类似。该电池中负极上的电极反应式是_________________。
查看答案和解析>>
科目:高中化学
来源:陕西省模拟题
题型:填空题
Ⅰ.描述弱电解质电离情况可以用电离度(电离度:一定条件下,当弱电解质达到电离平衡时,溶液中已电离的电解质分子数占原电解质分子总数的百分数)和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp)。
请回答下面问题:
⑴下列能使醋酸溶液中CH
3COOH的电离度增大,而电离常数不变的操作是_______(填序号)。
A.升高温度 B.加水稀释 C.加少量的CH
3COONa固体 D.加少量冰醋酸
⑵CH
3COONH
4的水溶液呈______(选填“酸性”、“中性”、“碱性”),理由是____________________。
⑶工业中常将BaSO
4转化为BaCO
3后,再将其制成各种可溶性的钡盐(如:BaCl
2)。具体做法是用饱和的纯碱溶液浸泡BaSO
4粉末,并不断补充纯碱,最后BaSO
4转化为BaCO
3。现有足量的BaSO
4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使c(SO
42- )达到0.0l mol/L以上,则溶液中c(CO
32- )应≥_______ mol/L。
Ⅱ.化学在能源开发与利用中起着重要的作用,如甲醇、乙醇、二甲醚(CH
3OCH
3)等都是新型燃料。
⑴乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇。
2CO
2(g)+6H
2(g)

CH
3CH
2OH(g)+3H
2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。
根据表中数据分析:
①上述反应的 a_______0(填“大于”或“小于”)。
②在一定温度下,提高氢碳(即n(H2)/n(CO2) )比,平衡常数K值_______(填“增大”、“减小”、或“不变”),对生成乙醇______(填“有利”或“不利”)。
⑵催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应)。该反应过程中能量变化如图所示:
①写出CO和H2制备乙醇的热化学反应方程式_________________。
②在一定温度下,向上述密闭容器中加入1 mol CO、3 mol H2及固体催化剂,使之反应。平衡时,反应产生的热量为Q kJ,若温度不变的条件下,向上述密闭容器中加入4 mol CO、
12 mol H2及固体催化剂,平衡时,反应产生的热量为w kJ,则w的范围为___________。
⑶二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效的优良性能。以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池,其工作原理与甲烷燃料电池原理相类似。该电池中负极上的电极反应式是_________________。
查看答案和解析>>

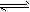 CO(g)+2H2(g) △H=-35.6 kJ/mol。该反应是_____(填“自发”或“非自发”)反应。
CO(g)+2H2(g) △H=-35.6 kJ/mol。该反应是_____(填“自发”或“非自发”)反应。 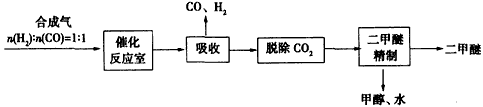
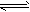 CH3OH(g) △H=-90.7 kJ/mol ①
CH3OH(g) △H=-90.7 kJ/mol ①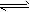 CH3OCH3(g)+H2O(g) △H = -23.5 kJ/mol ②
CH3OCH3(g)+H2O(g) △H = -23.5 kJ/mol ②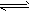 CO2(g)+H2(g) △H=-41.2 kJ/mol ③
CO2(g)+H2(g) △H=-41.2 kJ/mol ③  CH3OCH3(g)+CO2(g)的△H=_____。830℃ 时反应③的K=1.0,则在催化反应室中反应③的K_______(填“>”、“<”或“=”)1.0。
CH3OCH3(g)+CO2(g)的△H=_____。830℃ 时反应③的K=1.0,则在催化反应室中反应③的K_______(填“>”、“<”或“=”)1.0。  CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为 (填最简整数比),写出该分子中所有碳原子的杂化方式 。
CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为 (填最简整数比),写出该分子中所有碳原子的杂化方式 。  为碳原子,
为碳原子, 为硅原子)。每个碳原子周围与其距离最近的硅原子有 个。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为 (用含a、b的式子表示)。
为硅原子)。每个碳原子周围与其距离最近的硅原子有 个。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为 (用含a、b的式子表示)。 
 CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为 (填最简整数比),写出该分子中所有碳原子的杂化方式 。
CH—C≡N是制备腈纶的原料,其分子中σ键和π键的个数之比为 (填最简整数比),写出该分子中所有碳原子的杂化方式 。  为碳原子,
为碳原子, 为硅原子)。每个碳原子周围与其距离最近的硅原子有 个。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为 (用含a、b的式子表示)。
为硅原子)。每个碳原子周围与其距离最近的硅原子有 个。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为 (用含a、b的式子表示)。 

 (2013?临沂一模)【化学--物质结构与性质】
(2013?临沂一模)【化学--物质结构与性质】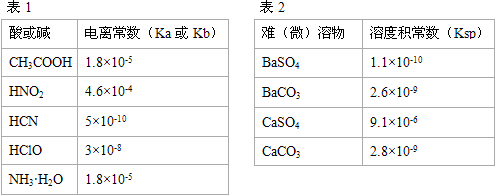
 CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。
CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。 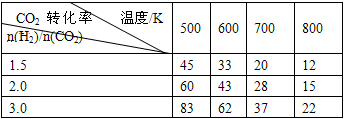

 CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。
CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定压强下,测得上述反应的实验数据如下表。 
