
| 金属汞在加热条件下可以与氧气化合生成氧化汞,反应如下: 2Hg+O2
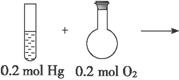
下列哪个选项可以说明0.2mol Hg 与0.2mol O2 充分反应后物质的种类及其量的情况?( )
|
科目:高中化学 来源: 题型:
| ||
科目:高中化学 来源: 题型:
科目:高中化学 来源:2011-2012学年福建省厦门一中高一上学期期中化学试卷 题型:单选题
金属汞在加热条件下可以与氧气化合生成氧化汞,反应如下:2Hg +O2= 2HgO ,下列哪个选项可以说明0.2mol Hg 与0.2mol O2充分反应后物质的种类及其量的情况?( )
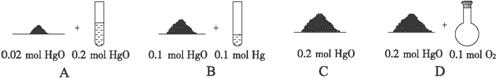
| A.0.02mol HgO + 0.2mol Hg | B.0.2mol HgO + 0.1mol O2 |
| C.0.2mol HgO | D.0.1mol HgO + 0.1mol Hg |
科目:高中化学 来源:不详 题型:单选题
| ||
| A.0.02molHgO+0.2molHg | B.0.1molHgO+0.1molHg |
| C.0.2molHgO | D.0.2molHgO+0.1molO2 |
科目:高中化学 来源:2010-2011学年福建省厦门一中高一(上)期中化学试卷(解析版) 题型:选择题
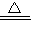 2HgO
2HgO科目:高中化学 来源:不详 题型:单选题
| A.0.02mol HgO + 0.2mol Hg | B.0.2mol HgO + 0.1mol O2 |
| C.0.2mol HgO | D.0.1mol HgO + 0.1mol Hg |
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源:福建省厦门一中2011-2012学年高一上学期期中化学试题 题型:013
|
金属汞在加热条件下可以与氧气化合生成氧化汞,反应如下:2Hg+O2 | |
| [ ] | |
A. |
0.02 mol HgO+0.2 mol Hg |
B. |
0.2 mol HgO+0.1 mol O2 |
C. |
0.2 mol HgO |
D. |
0.1 mol HgO+0.1 mol Hg |
科目:高中化学 来源:志鸿系列训练必修一化学人教版 人教版 题型:021
|
据2007年4月26日报道,河北省保定市满城县一小学发生汞中毒事件,中毒者已达到36人. 已知金属汞在加热条件下可以与氧气化合生成氧化汞:2Hg+O2
| |
A. |
|
B. |
|
C. |
|
D. |
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com