煤的气化是高效、清洁地利用煤炭的重要途径之一.
(1)在25
0C 101kPa时,H
2与0
2化合生成1mol H
2O(g)放出241.8kJ的热量,其热化学 方程式为
又知:①C(s)+O
2(g)═CO
2(g)△H=-393.5kJ/mol
②CO(g)+
O
2(g)═CO
2(g)△H=-283.0kJ/mol
焦炭与水蒸气反应是将固体煤变为气体燃料的方法,C(s)+H
2O(g)?CO(g)+Hi(g)△H=
kj/mol.
(2)CO可以与H
2CXg)进一步发生反应:CO(g)+H
2O(g)?CO
2(g)+H
2(g)△H<0在恒容密闭容器中,起始时n(H
20)=0.20mol,n(CO)=0.10mol,在800
0C时达到平衡状态,K=1.0,则平衡时,容器中CO的转化率是(计算结果保留一位小数).
(3)工业上从煤气化后的混合物中分离出H
2,进行氨的合成,已知反应N
2(g)+3H
2(g)
2NH
3((g) (△H<0)在等容条件下进行.改变其他反应条件,在I、II、III阶段体 系中各物质浓度随时间变化的曲线如图所示:
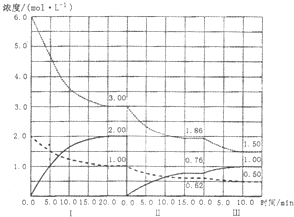
①N
2的平均反应速率v
1(N
2)、v
II(N
2)、v
III(N
2)从大到小排列次序为
;
②由第一次平衡到第二次平衡,平衡移动的方向是
,采取的措施是
③比较第II阶段反应温度(T
2)和第III阶段反应速度(T
3)的高低:T
2
T
3填“>、=、<”判断的理由是
.

