
»ÁÕºÀ˘ 棨‘⁄…’±≠÷–◊∞»Î50mL≈®∂»Œ™0.01mol?L-1µƒBa£®OH£©2»Ð“∫£¨¡¨Ω”∫√µºœþ£¨Ω´ø™πÿ±’∫œ£¨»ª∫ÛœÚBa£®OH£©2»Ð“∫÷–µŒº”0.2mol?L-1H2SO4»Ð“∫÷¡π˝¡ø£¨‘Ú µ—Èπ˝≥Ã÷–…’±≠ƒ⁄µƒ“∫õºµÁƒÐ¡¶±‰ªØŒ™£®°°°°£©
 |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
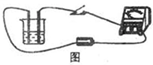 »ÁÕºÀ˘ 棨‘⁄…’±≠÷–◊∞»Î50mL≈®∂»Œ™0.01mol?L-1µƒBa£®OH£©2»Ð“∫£¨¡¨Ω”∫√µºœþ£¨Ω´ø™πÿ±’∫œ£¨»ª∫ÛœÚBa£®OH£©2»Ð“∫÷–µŒº”0.2mol?L-1H2SO4»Ð“∫÷¡π˝¡ø£¨‘Ú µ—Èπ˝≥Ã÷–…’±≠ƒ⁄µƒ“∫õºµÁƒÐ¡¶±‰ªØŒ™£®°°°°£©
»ÁÕºÀ˘ 棨‘⁄…’±≠÷–◊∞»Î50mL≈®∂»Œ™0.01mol?L-1µƒBa£®OH£©2»Ð“∫£¨¡¨Ω”∫√µºœþ£¨Ω´ø™πÿ±’∫œ£¨»ª∫ÛœÚBa£®OH£©2»Ð“∫÷–µŒº”0.2mol?L-1H2SO4»Ð“∫÷¡π˝¡ø£¨‘Ú µ—Èπ˝≥Ã÷–…’±≠ƒ⁄µƒ“∫õºµÁƒÐ¡¶±‰ªØŒ™£®°°°°£©ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£Æœ»ºı»ı£¨∫Û‘ˆ«ø | B£Æœ»‘ˆ«ø£¨∫Ûºı»ı |
| C£Æ“ª÷±‘ˆ«ø | D£Æº∏∫ı≤ª∏ƒ±‰ |

ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2011-2012—߃Í∫”ƒœ °÷Ðø⁄ –…Ú«œÿ∏þ“ª£®…œ£©∆⁄÷–ªØ—ß ‘æÌ£®Ω‚Œˆ∞Ê£© –գ∫—°‘ÒÂ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
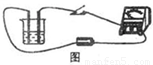
 »ÁÕºÀ˘ 棨‘⁄…’±≠÷–◊∞»Î50mL≈®∂»Œ™0.01mol?L-1µƒBa£®OH£©2»Ð“∫£¨¡¨Ω”∫√µºœþ£¨Ω´ø™πÿ±’∫œ£¨»ª∫ÛœÚBa£®OH£©2»Ð“∫÷–µŒº”0.2mol?L-1H2SO4»Ð“∫÷¡π˝¡ø£¨‘Ú µ—Èπ˝≥Ã÷–…’±≠ƒ⁄µƒ“∫õºµÁƒÐ¡¶±‰ªØŒ™
»ÁÕºÀ˘ 棨‘⁄…’±≠÷–◊∞»Î50mL≈®∂»Œ™0.01mol?L-1µƒBa£®OH£©2»Ð“∫£¨¡¨Ω”∫√µºœþ£¨Ω´ø™πÿ±’∫œ£¨»ª∫ÛœÚBa£®OH£©2»Ð“∫÷–µŒº”0.2mol?L-1H2SO4»Ð“∫÷¡π˝¡ø£¨‘Ú µ—Èπ˝≥Ã÷–…’±≠ƒ⁄µƒ“∫õºµÁƒÐ¡¶±‰ªØŒ™ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫‘ƒ∂¡¿ÌΩ‚
¢Ò.ƒ≥ªØ—ß µ—È–°◊ÈÃΩæø – € ≥”√∞◊¥◊÷–¥◊À·µƒ◊º»∑≈®∂»£¨»°25.00mLƒ≥∆∑≈∆ ≥”√∞◊¥◊”⁄…’±≠÷–£¨œ° Õ≤¢◊™“∆÷¡250mL»ð¡ø∆ø÷–£¨∂®»ð£¨“°‘»°£»°œ° Õ“∫25.00mL”√≈®∂»Œ™cb mol/Lµƒ±Í◊ºNaOH»Ð“∫∂‘∆‰Ω¯––µŒ∂®°£
£®1£©∏√–°◊È”√∑”Ù ‘“∫◊˜÷∏ 溡£¨≈–∂œµΩ¥ÔµŒ∂®÷’µ„µƒ µ—Èœ÷œÛ «£∫ °°°£
£®2£©”“Õº±Ì æ50mLµŒ∂®πÐ÷–“∫√ʵƒŒª÷√£¨»ÙA”ÎCøÃ∂»º‰œý≤Ól mL£¨A¥¶µƒøÃ∂»Œ™25£¨µŒ∂®πÐ÷–“∫√Ê∂¡ ˝”¶Œ™ mL°£

£®3£©Œ™¡Àºı–° µ—ÈŒÛ≤Ó£¨∏√Õ¨—ß“ªπ≤Ω¯––¡À»˝¥Œ µ—È£¨ºŸ…Ë√ø¥ŒÀ˘»°∞◊¥◊ê˝æ˘Œ™25.00mL£¨NaOH±Í◊º“∫≈®∂»Œ™cb mo1/L£¨»˝¥Œ µ—ÈΩ·π˚º«¬º»Áœ¬£∫
| µ—È¥Œ ˝ | µ⁄“ª¥Œ | µ⁄∂˛¥Œ | µ⁄»˝¥Œ |
| œ˚∫ƒNaOH»Ð“∫ê˝/mL | 26.32 | 25.34 | 25.30 |
¥”…œ±Ìø…“‘ø¥≥ˆ£¨µ⁄“ª¥Œ µ—È÷–º«¬ºœ˚∫ƒNaOH»Ð“∫µƒÃª˝√˜œ‘∂ý”⁄∫Û¡Ω¥Œ£¨∆‰‘≠“Úø…ƒÐ « °£
A£ÆµŒ∂®«∞µŒ∂®πк‚◊Ï”–∆¯≈𣨵Œ∂®Ω· ¯ŒÞ∆¯≈ð
B£Æ ¢◊∞±Í◊º“∫µƒµŒ∂®πÐ◊∞“∫«∞”√’Ù¡ÛÀÆœ¥∫Û£¨Œ¥”√±Í◊º“∫»Ûœ¥
C£Æµ⁄“ª¥ŒµŒ∂®”√µƒ◊∂–Œ∆ø”√∞◊¥◊»Ûœ¥
D£Æ∏√NaOH±Í◊º“∫±£¥Ê ±º‰π˝≥§£¨”–≤ø∑÷±‰÷ £¨≈®∂»ΩµµÕ
£®4£©∏˘æðÀ˘∏¯ ˝æ𣨖¥≥ˆº∆À„∏√∞◊¥◊÷–¥◊À·µƒŒÔ÷ µƒ¡ø≈®∂»µƒ±Ì¥Ô Ω(≤ª±ÿªØºÚ)£∫
c£Ω °£
¢Ú. ”√÷–∫ÕµŒ∂®∑®≤‚∂®NaOH∫ÕNa2CO3ªÏ∫œ»Ð“∫÷–µƒNaOHµƒ÷ ¡ø∑÷ ˝ ±£¨ø…œ»‘⁄ªÏ∫œ»Ð“∫÷–º”»Îπ˝¡øµƒBaCl2»Ð“∫£¨ πNa2CO3ÕÍ»´±‰≥…BaCO3≥¡µÌ£¨»ª∫Û”√±Í◊º—ŒÀ·µŒ∂®£®”√∑”Ù◊ˆŒ™÷∏ 溡£©°£ ‘ªÿ¥£∫
£®1£©œÚªÏ”–BaCO3≥¡µÌµƒNaOH»Ð“∫¿ÔµŒº”—ŒÀ·£¨Œ™ ≤√¥≤ªª· πBaCO3»ÐΩ‚∂¯ƒÐ≤‚∂®NaOH»Ð“∫µƒ÷ ¡ø∑÷ ˝£ø
£®2£©∑÷Œˆ‘⁄µŒ∂®π˝≥Ã÷–≤ª∂œ’Òµ¥◊∂–Œ∆øµƒ‘≠“Ú£ø
£®3£©µŒ∂®÷’µ„ ±»Ð“∫—’…´»Á∫Œ±‰ªØ£ø
£®4£©ƒÐ∑Ò∏ƒ”√º◊ª˘≥»◊˜÷∏ 溡£ø≤¢Àµ√˜¿Ì”…°£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫‘ƒ∂¡¿ÌΩ‚
¢Ò.ƒ≥ªØ—ß µ—È–°◊ÈÃΩæø – € ≥”√∞◊¥◊÷–¥◊À·µƒ◊º»∑≈®∂»£¨»°25.00mLƒ≥∆∑≈∆ ≥”√∞◊¥◊”⁄…’±≠÷–£¨œ° Õ≤¢◊™“∆÷¡250mL»ð¡ø∆ø÷–£¨∂®»ð£¨“°‘»°£»°œ° Õ“∫25.00mL”√≈®∂»Œ™cb mol/Lµƒ±Í◊ºNaOH»Ð“∫∂‘∆‰Ω¯––µŒ∂®°£
£®1£©∏√–°◊È”√∑”Ù ‘“∫◊˜÷∏ 溡£¨≈–∂œµΩ¥ÔµŒ∂®÷’µ„µƒ µ—Èœ÷œÛ «£∫ °°°£
£®2£©”“Õº±Ì æ50mLµŒ∂®πÐ÷–“∫√ʵƒŒª÷√£¨»ÙA”ÎCøÃ∂»º‰œý≤Ól mL£¨A¥¶µƒøÃ∂»Œ™25£¨µŒ∂®πÐ÷–“∫√Ê∂¡ ˝”¶Œ™ mL°£
£®3£©Œ™¡Àºı–° µ—ÈŒÛ≤Ó£¨∏√Õ¨—ß“ªπ≤Ω¯––¡À»˝¥Œ µ—È£¨ºŸ…Ë√ø¥ŒÀ˘»°∞◊¥◊ê˝æ˘Œ™25.00mL£¨NaOH±Í◊º“∫≈®∂»Œ™cb mo1/L£¨»˝¥Œ µ—ÈΩ·π˚º«¬º»Áœ¬£∫
| µ—È¥Œ ˝ | µ⁄“ª¥Œ | µ⁄∂˛¥Œ | µ⁄»˝¥Œ |
| œ˚∫ƒNaOH»Ð“∫ê˝/mL | 26.32 | 25.34 | 25.30 |
¥”…œ±Ìø…“‘ø¥≥ˆ£¨µ⁄“ª¥Œ µ—È÷–º«¬ºœ˚∫ƒNaOH»Ð“∫µƒÃª˝√˜œ‘∂ý”⁄∫Û¡Ω¥Œ£¨∆‰‘≠“Úø…ƒÐ « °£
A£ÆµŒ∂®«∞µŒ∂®πк‚◊Ï”–∆¯≈𣨵Œ∂®Ω· ¯ŒÞ∆¯≈ð
B£Æ ¢◊∞±Í◊º“∫µƒµŒ∂®πÐ◊∞“∫«∞”√’Ù¡ÛÀÆœ¥∫Û£¨Œ¥”√±Í◊º“∫»Ûœ¥
C£Æµ⁄“ª¥ŒµŒ∂®”√µƒ◊∂–Œ∆ø”√∞◊¥◊»Ûœ¥
D£Æ∏√NaOH±Í◊º“∫±£¥Ê ±º‰π˝≥§£¨”–≤ø∑÷±‰÷ £¨≈®∂»ΩµµÕ
£®4£©∏˘æðÀ˘∏¯ ˝æ𣨖¥≥ˆº∆À„∏√∞◊¥◊÷–¥◊À·µƒŒÔ÷ µƒ¡ø≈®∂»µƒ±Ì¥Ô Ω(≤ª±ÿªØºÚ)£∫
c£Ω °£
¢Ú. ”√÷–∫ÕµŒ∂®∑®≤‚∂®NaOH∫ÕNa2CO3ªÏ∫œ»Ð“∫÷–µƒNaOHµƒ÷ ¡ø∑÷ ˝ ±£¨ø…œ»‘⁄ªÏ∫œ»Ð“∫÷–º”»Îπ˝¡øµƒBaCl2»Ð“∫£¨ πNa2CO3ÕÍ»´±‰≥…BaCO3≥¡µÌ£¨»ª∫Û”√±Í◊º—ŒÀ·µŒ∂®£®”√∑”Ù◊ˆŒ™÷∏ 溡£©°£ ‘ªÿ¥£∫
£®1£©œÚªÏ”–BaCO3≥¡µÌµƒNaOH»Ð“∫¿ÔµŒº”—ŒÀ·£¨Œ™ ≤√¥≤ªª· πBaCO3»ÐΩ‚∂¯ƒÐ≤‚∂®NaOH»Ð“∫µƒ÷ ¡ø∑÷ ˝£ø
£®2£©∑÷Œˆ‘⁄µŒ∂®π˝≥Ã÷–≤ª∂œ’Òµ¥◊∂–Œ∆øµƒ‘≠“Ú£ø
£®3£©µŒ∂®÷’µ„ ±»Ð“∫—’…´»Á∫Œ±‰ªØ£ø
£®4£©ƒÐ∑Ò∏ƒ”√º◊ª˘≥»◊˜÷∏ 溡£ø≤¢Àµ√˜¿Ì”…°£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2010ƒÍ’„Ω≠ °¥»œ™÷–—ß∏þ∂˛µ⁄∂˛—ß∆⁄∆⁄÷–øº ‘£®∆’Õ®∞ý£©ªØ—ß ‘ –գ∫ µ—ÈÂ
¢Ò.ƒ≥ªØ—ß µ—È–°◊ÈÃΩæø – € ≥”√∞◊¥◊÷–¥◊À·µƒ◊º»∑≈®∂»£¨»°25.00mLƒ≥∆∑≈∆ ≥”√∞◊¥◊”⁄…’±≠÷–£¨œ° Õ≤¢◊™“∆÷¡250mL»ð¡ø∆ø÷–£¨∂®»ð£¨“°‘»°£»°œ° Õ“∫25.00mL”√≈®∂»Œ™cb mol/Lµƒ±Í◊ºNaOH»Ð“∫∂‘∆‰Ω¯––µŒ∂®°£
£®1£©∏√–°◊È”√∑”Ù ‘“∫◊˜÷∏ 溡£¨≈–∂œµΩ¥ÔµŒ∂®÷’µ„µƒ µ—Èœ÷œÛ «£∫ °°°£
£®2£©”“Õº±Ì æ50mLµŒ∂®πÐ÷–“∫√ʵƒŒª÷√£¨»ÙA”ÎCøÃ∂»º‰œý≤Ól mL£¨A¥¶µƒøÃ∂»Œ™25£¨µŒ∂®πÐ÷–“∫√Ê∂¡ ˝”¶Œ™ mL°£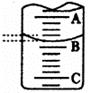
£®3£©Œ™¡Àºı–° µ—ÈŒÛ≤Ó£¨∏√Õ¨—ß“ªπ≤Ω¯––¡À»˝¥Œ µ—È£¨ºŸ…Ë√ø¥ŒÀ˘»°∞◊¥◊ê˝æ˘Œ™25.00mL£¨NaOH±Í◊º“∫≈®∂»Œ™cb mo1/L£¨»˝¥Œ µ—ÈΩ·π˚º«¬º»Áœ¬£∫
| µ—È¥Œ ˝ | µ⁄“ª¥Œ | µ⁄∂˛¥Œ | µ⁄»˝¥Œ |
| œ˚∫ƒNaOH»Ð“∫ê˝/mL | 26.32 | 25.34 | 25.30 |
| A£ÆµŒ∂®«∞µŒ∂®πк‚◊Ï”–∆¯≈𣨵Œ∂®Ω· ¯ŒÞ∆¯≈ð |
| B£Æ ¢◊∞±Í◊º“∫µƒµŒ∂®πÐ◊∞“∫«∞”√’Ù¡ÛÀÆœ¥∫Û£¨Œ¥”√±Í◊º“∫»Ûœ¥ |
| C£Æµ⁄“ª¥ŒµŒ∂®”√µƒ◊∂–Œ∆ø”√∞◊¥◊»Ûœ¥ |
D£Æ∏√NaOH±Í◊º“∫±£¥Ê ±º‰π˝≥§£¨”–≤ø∑÷±‰÷ £¨≈® ∂»ΩµµÕ ∂»ΩµµÕ |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2010ƒÍ’„Ω≠ °∏þ∂˛µ⁄∂˛—ß∆⁄∆⁄÷–øº ‘£®∆’Õ®∞ý£©ªØ—ß ‘ –գ∫ µ—ÈÂ
¢Ò.ƒ≥ªØ—ß µ—È–°◊ÈÃΩæø – € ≥”√∞◊¥◊÷–¥◊À·µƒ◊º»∑≈®∂»£¨»°25.00mLƒ≥∆∑≈∆ ≥”√∞◊¥◊”⁄…’±≠÷–£¨œ° Õ≤¢◊™“∆÷¡250mL»ð¡ø∆ø÷–£¨∂®»ð£¨“°‘»°£»°œ° Õ“∫25.00mL”√≈®∂»Œ™cb mol/Lµƒ±Í◊ºNaOH»Ð“∫∂‘∆‰Ω¯––µŒ∂®°£
£®1£©∏√–°◊È”√∑”Ù ‘“∫◊˜÷∏ 溡£¨≈–∂œµΩ¥ÔµŒ∂®÷’µ„µƒ µ—Èœ÷œÛ «£∫ °°°£
£®2£©”“Õº±Ì æ50mLµŒ∂®πÐ÷–“∫√ʵƒŒª÷√£¨»ÙA”ÎCøÃ∂»º‰œý≤Ól mL£¨A¥¶µƒøÃ∂»Œ™25£¨µŒ∂®πÐ÷–“∫√Ê∂¡ ˝”¶Œ™ mL°£
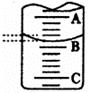
£®3£©Œ™¡Àºı–° µ—ÈŒÛ≤Ó£¨∏√Õ¨—ß“ªπ≤Ω¯––¡À»˝¥Œ µ—È£¨ºŸ…Ë√ø¥ŒÀ˘»°∞◊¥◊ê˝æ˘Œ™25.00mL£¨NaOH±Í◊º“∫≈®∂»Œ™cb mo1/L£¨»˝¥Œ µ—ÈΩ·π˚º«¬º»Áœ¬£∫
|
µ—È¥Œ ˝ |
µ⁄“ª¥Œ |
µ⁄∂˛¥Œ |
µ⁄»˝¥Œ |
|
œ˚∫ƒNaOH»Ð“∫ê˝/mL |
26.32 |
25.34 |
25.30 |
¥”…œ±Ìø…“‘ø¥≥ˆ£¨µ⁄“ª¥Œ µ—È÷–º«¬ºœ˚∫ƒNaOH»Ð“∫µƒÃª˝√˜œ‘∂ý”⁄∫Û¡Ω¥Œ£¨∆‰‘≠“Úø…ƒÐ « °£
A£ÆµŒ∂®«∞µŒ∂®πк‚◊Ï”–∆¯≈𣨵Œ∂®Ω· ¯ŒÞ∆¯≈ð
B£Æ ¢◊∞±Í◊º“∫µƒµŒ∂®πÐ◊∞“∫«∞”√’Ù¡ÛÀÆœ¥∫Û£¨Œ¥”√±Í◊º“∫»Ûœ¥
C£Æµ⁄“ª¥ŒµŒ∂®”√µƒ◊∂–Œ∆ø”√∞◊¥◊»Ûœ¥
D£Æ∏√NaOH±Í◊º“∫±£¥Ê ±º‰π˝≥§£¨”–≤ø∑÷±‰÷ £¨≈®∂»ΩµµÕ
£®4£©∏˘æðÀ˘∏¯ ˝æ𣨖¥≥ˆº∆À„∏√∞◊¥◊÷–¥◊À·µƒŒÔ÷ µƒ¡ø≈®∂»µƒ±Ì¥Ô Ω(≤ª±ÿªØºÚ)£∫
c£Ω °£
¢Ú. ”√÷–∫ÕµŒ∂®∑®≤‚∂®NaOH∫ÕNa2CO3ªÏ∫œ»Ð“∫÷–µƒNaOHµƒ÷ ¡ø∑÷ ˝ ±£¨ø…œ»‘⁄ªÏ∫œ»Ð“∫÷–º”»Îπ˝¡øµƒBaCl2»Ð“∫£¨ πNa2CO3ÕÍ»´±‰≥…BaCO3≥¡µÌ£¨»ª∫Û”√±Í◊º—ŒÀ·µŒ∂®£®”√∑”Ù◊ˆŒ™÷∏ 溡£©°£ ‘ªÿ¥£∫
£®1£©œÚªÏ”–BaCO3≥¡µÌµƒNaOH»Ð“∫¿ÔµŒº”—ŒÀ·£¨Œ™ ≤√¥≤ªª· πBaCO3»ÐΩ‚∂¯ƒÐ≤‚∂®NaOH»Ð“∫µƒ÷ ¡ø∑÷ ˝£ø
£®2£©∑÷Œˆ‘⁄µŒ∂®π˝≥Ã÷–≤ª∂œ’Òµ¥◊∂–Œ∆øµƒ‘≠“Ú£ø
£®3£©µŒ∂®÷’µ„ ±»Ð“∫—’…´»Á∫Œ±‰ªØ£ø
£®4£©ƒÐ∑Ò∏ƒ”√º◊ª˘≥»◊˜÷∏ 溡£ø≤¢Àµ√˜¿Ì”…°£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫ µ—ÈÂ

| µ—È¥Œ ˝ | µ⁄“ª¥Œ | µ⁄∂˛¥Œ | µ⁄»˝¥Œ |
| œ˚∫ƒNaOH»Ð“∫ê˝/mL | 26.32 | 25.34 | 25.30 |
| A£ÆµŒ∂®«∞µŒ∂®πк‚◊Ï”–∆¯≈𣨵Œ∂®Ω· ¯ŒÞ∆¯≈ð |
| B£Æ ¢◊∞±Í◊º“∫µƒµŒ∂®πÐ◊∞“∫«∞”√’Ù¡ÛÀÆœ¥∫Û£¨Œ¥”√±Í◊º“∫»Ûœ¥ |
| C£Æµ⁄“ª¥ŒµŒ∂®”√µƒ◊∂–Œ∆ø”√∞◊¥◊»Ûœ¥ |
D£Æ∏√NaOH±Í◊º“∫±£¥Ê ±º‰π˝≥§£¨”–≤ø∑÷±‰÷ £¨≈® ∂»ΩµµÕ ∂»ΩµµÕ |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫

π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com