
对于常温下pH为12的氢氧化钠溶液,叙述正确的是( )
|
科目:高中化学 来源:不详 题型:单选题
| A.c(OH-)=c(H+)+c(Na+) |
| B.与等体积pH=2乙酸混合后所得溶液显碱性 |
| C.由H2O电离出的c(H+)=1.0×10-2mol?L-1 |
| D.与等体积0.01 mol?L-1氯化铵溶液混合后所得溶液中:c(Na+)=c(NH4+) |
科目:高中化学 来源:2012-2013学年江西省上饶市横峰中学高二(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源:2014届湖北武汉部分重点中学高二上学期期末考试化学试卷(解析版) 题型:选择题
下列对溶液叙述正确的是
A.向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小
B.对于物质的量浓度相同的氢氧化钠和氨水,加水稀释至m倍、n倍后,若稀释后溶液的PH相等,则m<n
C.常温下,5ml0.02mol/LHCl溶液与5ml0.02mol/LBa(OH)2溶液混合,经充分反应后,如果溶液体积为10mL,则溶液的PH=12
D.常温下将稀NaOH溶液与醋酸溶液混合,可能出现PH>7的情况,且c(OH-)>c(Na+)>c(CH3COO-)>c(H+)
科目:高中化学 来源:广东省中山一中2012届高三上学期第三次统测化学试题 题型:058
2011年8月12日,网上传云南曲靖市越州镇有总量5000余吨的重毒化工废料铬渣由于非法丢放,毒水被直接排放南盘江中.
Ⅰ:某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
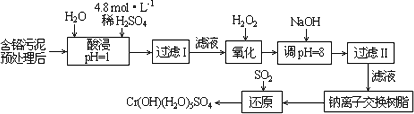
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
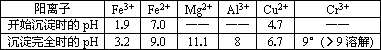
(1)实验室用18.4 mol·L-1的浓硫酸配制250 mL 4.8 mol·L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需________.
(2)酸浸时,为了提高浸取率可采取的措施是________(至少答一点).
(3)加入H2O2的作用是________.
调节溶液的pH=8是为了除去________离子.
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的的杂质离子是________.
(5)还原过程发生以下反应(请配平):
________Na2Cr2O7+________SO2+________=________Cr(OH)(H2O)5SO4+________Na2SO4;
Ⅱ:
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理.其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀.阳极的电极反应式为________.在阴极附近溶液pH升高的原因是(用电极反应方程式解释)________.科目:高中化学 来源:湖北省模拟题 题型:填空题
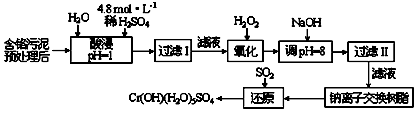
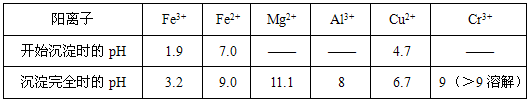
科目:高中化学 来源:福建省月考题 题型:填空题


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com