
已知结构为正四面体型的离子A和直线型离子B反应,生成三角锥形分子C和V形分子D(A、B、C、D均为10电子微粒,组成它们的元素原子序数均小于10),下列说法正确的是( )
|
科目:高中化学 来源: 题型:
已知结构为正四面体型的离子A和直线型离子B反应,生成三角锥形分子C和V形分子D(组成A、B、C、D微粒的元素原子序数均小于10),下列说法正确的是
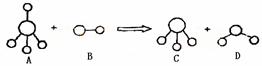
A.分子C与D不能发生化学反应
B.微粒A的空间结构与CH4相似,它们均为正四面体,所以它是非极性分子
C.固态D的熔沸点明显高于固态H2S的原因在于D分子中的共价键强于S-H键
D.在25℃时,含有A的盐酸盐溶液的pH小于7
科目:高中化学 来源: 题型:
科目:高中化学 来源: 题型:
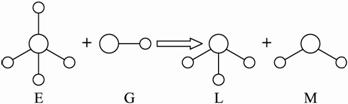
A.E、G、L、M都是10e-微粒?
B.L、M都是极性分子?
C.L能使紫色石蕊试液变蓝色?
D.E离子中质子数一定大于中子数
科目:高中化学 来源: 题型:
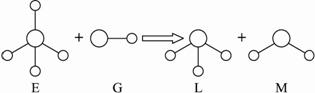
A.E、G、L、M都是10e-微粒?
B.L、M都是极性分子?
C.L能使紫色石蕊试液变蓝色?
D.E离子中质子数一定大于中子数
科目:高中化学 来源: 题型:
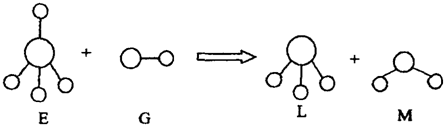
已知结构为正四面体型的离子E和直线型离子G反应,生成三角锥分子L和V形分子M(组成E、G、L、M微粒的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是 ( )
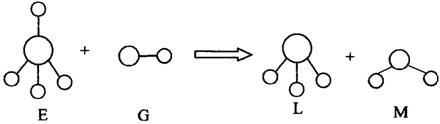
A.E、G、L、M都是10e![]() 微粒 B.L、M都是极性分子
微粒 B.L、M都是极性分子
C.L能使紫色石蕊试液变蓝色 D.E离子中,质子数一定大于中子数
科目:高中化学 来源:2006-2007学年山东省聊城市高三(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题
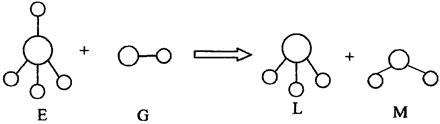
A.E、G、L、M都是10e 微粒 微粒 | B.L、M都是极性分子 |
| C.L能使紫色石蕊试液变蓝色 | D.E离子中,质子数一定大于中子数 |
科目:高中化学 来源:山东省聊城市2006-2007学年度第一学期高三年级期中考试、化学试题 题型:013
|
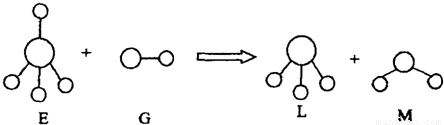
已知结构为正四面体型的离子E和直线型离子G反应,生成三角锥型分子L和V形分子M(组成E、G、L、M微粒的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是
| |
| [ ] | |
A. |
E、G、L、M都是10e-微粒 |
B. |
L、M都是极性分子 |
C. |
L能使紫色石蕊试液变蓝色 |
D. |
E离子中,质子数一定大于中子数 |
科目:高中化学 来源:闸北区一模 题型:单选题
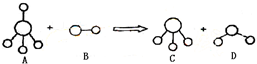
| A.分子C与D不能发生化学反应 |
| B.微粒A的空间结构与CH4相似,它们均为正四面体,所以A是非极性分子 |
| C.固态D的熔沸点明显高于固态H2S的原因在于D分子中的共价键强于S-H键 |
| D.在25℃时,A的盐酸盐溶液的pH小于7 |
科目:高中化学 来源:2012年上海市闸北区高考化学一模试卷(解析版) 题型:选择题

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com