
现有浓度均为2mol?L的盐酸和硫酸溶液各100mL,分别加入等质量的铁粉,反应结束后,测得生成的气体的质量比为2:3,则加入铁粉的质量可能是( )
|
科目:高中化学 来源:郑州一模 题型:单选题
| A.2.8 g | B.5.6 g | C.8.4 g | D.16.8 g |
科目:高中化学 来源:2010年河南省郑州市高考化学一模试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:
科目:高中化学 来源:北京期中题 题型:单选题
科目:高中化学 来源:2013-2014学年河北省高三下学期一调考试理综化学试卷(解析版) 题型:填空题
I? “套管实验”是将一支较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要更多仪器进行的实验。因其具有许多优点,被广泛应用于化学实验中,如图实验为“套管实验”,小试管内塞有沾有无水硫酸铜粉末的棉花球。请观察实验装置,分析实验原理,回答下列问题:
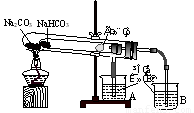 ???
???
(1)该实验的目的是_____________________
(2)实验开始前微热试管,说明装置不漏气的现象是???????????????????????????????
(3)一段时间后结束实验,待装置冷却,取出小试管中固体溶于水,然后滴加1mol/L盐酸,产生CO2的量与盐酸的量的关系如图所示。其中合理的是________________
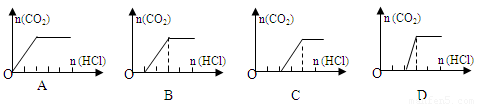
II燃料电池是一种连续的将燃料和氧化剂的化学能直接转化为电能的化学电池。氢气、烃、肼、甲醇等液体或气体,均可以作燃料电池的燃料。请回答下列问题:
(1)以甲烷和氧气为原料,氢氧化钠溶液为电解质溶液构成电池。写出其正极反应式???
(2)以上述电池为电源,石墨为电极电解1L 0. 1mol/L的氯化钾溶液。回答下列问题:
写出电解总反应的离子方程式????????????????????? ???????????????
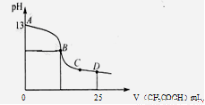
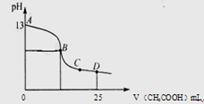
(3)室温时,电解一段时间后,取25mL上述电解后溶液,滴加0.2mol/L醋酸,加入醋酸的体积与溶液的pH的关系如图所示(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)
????????????? ①计算消耗标准状况下甲烷???????? mL
????????????? ②若图中的B点pH=7,则酸碱恰好完全反应的点在??????? 区间(填“AB”、“BC”或“CD”)
????????????? ③AB区间溶液中各离子浓度大小关系中可能正确的是?????????????????
A. c(K+)>c(OH-)>c (CH3COO-) >c(H+)???
B. c(K+)>c(CH3COO-)>c(OH-) >c(H+)
C. c(K+)>c(CH3COO-)=c(OH-) >c(H+)
科目:高中化学 来源: 题型:填空题
I “套管实验”是将一支较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要更多仪器进行的实验。因其具有许多优点,被广泛应用于化学实验中,如图实验为“套管实验”,小试管内塞有沾有无水硫酸铜粉末的棉花球。请观察实验装置,分析实验原理,回答下列问题: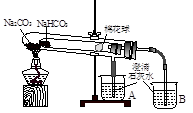
(1)该实验的目的是_____________________
(2)实验开始前微热试管,说明装置不漏气的现象是
(3)一段时间后结束实验,待装置冷却,取出小试管中固体溶于水,然后滴加1mol/L盐酸,产生CO2的量与盐酸的量的关系如图所示。其中合理的是________________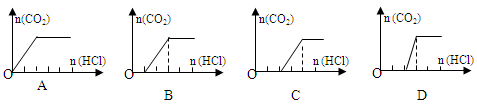
II燃料电池是一种连续的将燃料和氧化剂的化学能直接转化为电能的化学电池。氢气、烃、肼、甲醇等液体或气体,均可以作燃料电池的燃料。请回答下列问题:
(1)以甲烷和氧气为原料,氢氧化钠溶液为电解质溶液构成电池。写出其正极反应式
(2)以上述电池为电源,石墨为电极电解1L0. 1mol/L的氯化钾溶液。回答下列问题:
写出电解总反应的离子方程式 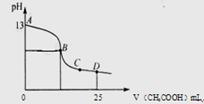
(3)室温时,电解一段时间后,取25mL上述电解后溶液,滴加0.2mol/L醋酸,加入醋酸的体积与溶液的pH的关系如图所示(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)
①计算消耗标准状况下甲烷 mL
②若图中的B点pH=7,则酸碱恰好完全反应的点在 区间(填“AB”、“BC”或“CD”)
③AB区间溶液中各离子浓度大小关系中可能正确的是
A. c(K+)>c(OH-)>c (CH3COO-) >c(H+)
B. c(K+)>c(CH3COO-)>c(OH-) >c(H+)
C. c(K+)>c(CH3COO-)=c(OH-) >c(H+)
科目:高中化学 来源:不详 题型:填空题


科目:高中化学 来源: 题型:阅读理解
MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果。某兴趣小组通过实验研究MnO2的性质![]()
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是 。
A、把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B、把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C、把MnO2固体加入到Na2SO3溶液中,再加入BaCl2观察是否有白色沉淀生成
D、把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比试验。
| 实验 | 酸或碱 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸溶液 | 迅速变棕褐色 |
该小组从上述对比实验中,可以得出的结论是 。
写出在酸性条件下,MnO2氧化I-的离子方程式 。
(3)欲探究MnO2的催化效果,需要用30%的H2O2溶液(密度近似为1g/cm3)配制浓度3%的H2O2溶液(密度近似为1g/cm3)100mL。其配制方法是:用量筒量取 mL30%H2O2溶液放入 (填仪器名称)中,再加入一定量的水,搅拌均匀。
(4)在实验时,某同学把1滴KI溶液误滴入到过量的5mL3%的H2O2溶液中,发现产生了大量气泡。该小组查阅到KI与H2O2可发生如下反应:2KI+H2O2=KOH+I2,认为有可能是反应产物I2起了催化H2O2分解的作用。请设计一个简单实验证明该假设是否正确。
。
(5)实验室用二氧化锰和浓盐酸制取氯气,下列仪器可作为该反应的反应容器的是 (填序号)。
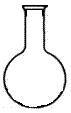

![]()
A B C D
(6)二氧化锰可用于制作干电池,电池总反应为:Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O,则其正极的电极反应式为 。
科目:高中化学 来源: 题型:阅读理解
科目:高中化学 来源: 题型:阅读理解
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加入KSCN溶液 | 溶液变血红色 溶液变血红色 |
固体物质中有FeCl3 |
| 在酸性KMnO4溶液中加入少量A | KMnO4溶液颜色无明显变化 | 固体物质中不含 FeCl2 FeCl2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com