
在下列的各种叙述中,正确的是( )
|
科目:高中化学 来源:2012-2013学年湖南省长沙市天心一中高二(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题
| A.在任何条件下,纯水的pH=7 |
| B.在任何条件下,纯水都呈中性 |
| C.在100℃时,纯水的pH>7 |
| D.在100℃时,纯水中c(H+)<10-7mol/L |
科目:高中化学 来源:2015届江西省四校高一零班第一次月考化学试卷(解析版) 题型:选择题
下列有关气体体积的叙述中,正确的是 ( )
A.一定温度和压强下,各种气态物质的体积大小,由构成气体的分子大小决定
B.一定温度和压强下,各种气态物质的体积大小由构成气体的分子数决定
C.非标准状况下,1 mol任何气体的体积不可能为22.4 L
D.将0.5mol气体A和0.5mol气体B混合,在标准状况下的体积一定约为22.4 L
科目:高中化学 来源:不详 题型:单选题
| A.一定温度和压强下,各种气态物质的体积大小,由构成气体的分子大小决定 |
| B.一定温度和压强下,各种气态物质的体积大小由构成气体的分子数决定 |
| C.非标准状况下,1 mol任何气体的体积不可能为22.4 L |
| D.将0.5mol气体A和0.5mol气体B混合,在标准状况下的体积一定约为22.4 L |
科目:高中化学 来源: 题型:
下列各项中前后两个叙述都正确的是( )
A.单质分子中一定存在共价键;塑料、合成橡胶和合成纤维二大合成材料都是以石
油、煤和天然气为原料生产的
B.诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别指蛋白质和烃;质子数相同的粒子不…定属丁同种元素
C.同位素的化学性质儿乎完全相同;任何原子的原子核都是由质子和中子构成的
D. PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构;乙烯的结构式CH2=CH2
科目:高中化学 来源: 题型:
下列各项中前后两个叙述都正确的是( )
A.单质分子中一定存在共价键;塑料、合成橡胶和合成纤维二大合成材料都是以石
油、煤和天然气为原料生产的
B.诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别指蛋白质和烃;质子数相同的粒子不…定属丁同种元素
C.同位素的化学性质儿乎完全相同;任何原子的原子核都是由质子和中子构成的
D. PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构;乙烯的结构式CH2=CH2
科目:高中化学 来源:2012-2013学年江西省四校高一零班第一次月考化学试卷(带解析) 题型:单选题
下列有关气体体积的叙述中,正确的是 ( )
| A.一定温度和压强下,各种气态物质的体积大小,由构成气体的分子大小决定 |
| B.一定温度和压强下,各种气态物质的体积大小由构成气体的分子数决定 |
| C.非标准状况下,1 mol任何气体的体积不可能为22.4 L |
| D.将0.5mol气体A和0.5mol气体B混合,在标准状况下的体积一定约为22.4 L |
科目:高中化学 来源: 题型:
(10分)工业上通常把溶液中存在的CO32- 和HCO3-的总浓度称为总碱度。水中碱度的控制成为碳酸钠软化水处理法的关键。碳酸在水中一般以3种形态存在,即H2CO3(CO2)、CO32- 和HCO3-。当溶液的pH发生变化时,其中任一种形态的物质的量占三种形态总物质的量的分数δ也可能发生变化,下图是碳酸溶液中碳酸的各种形态的δ随pH的变化曲线。
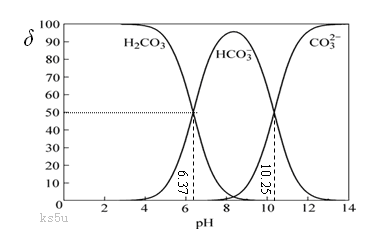
(1)从图中推断NaHCO3溶液呈 (填“酸”、“碱”、或“中”)性,其原因是
(用离子方程式表示)。
(2)正常情况下,人体血液的pH维持在7.35~7.45之间,则溶于血液中的二氧化碳的主要存在形式是 。(填写微粒化学式)
(3)根据上图,下列叙述中正确的是 。
A.HCO3-既能与强酸反应又能与强碱反应。
 B.盐酸逐滴滴入碳酸钠溶液至恰好完全反应时溶液呈中性
B.盐酸逐滴滴入碳酸钠溶液至恰好完全反应时溶液呈中性
C.pH小于7的雨水称为酸雨
D.在pH为6.37时,溶液中的c (H2CO3)= c (HCO3-)
(4)工业用循环冷却水中常含有Ca2+等杂质离子,在循环过程中易结垢,可通过控制溶液的总碱度使Ca2+等离子形成沉渣除去。已知某温度下Ksp(CaCO3)=3.03×10-9,当水中的c(Ca2+)≤3×10-4 mol·L-1时,不会出现结垢现象,则该水中的c(CO32-)应至少为 mol·L-1。
科目:高中化学 来源:同步题 题型:填空题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com