
¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al-AgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∆‰‘≠¿Ì»ÁÕºÀ˘ æ£Æ∏√µÁ≥ÿ∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™£∫2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O£¨œ¬¡–Àµ∑®’˝»∑µƒ «£®°°°°£©
 |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
 ¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al-AgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∆‰‘≠¿Ì»ÁÕºÀ˘ æ£Æ∏√µÁ≥ÿ∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™£∫2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O£¨œ¬¡–Àµ∑®’˝»∑µƒ «£®°°°°£©
¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al-AgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∆‰‘≠¿Ì»ÁÕºÀ˘ æ£Æ∏√µÁ≥ÿ∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™£∫2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O£¨œ¬¡–Àµ∑®’˝»∑µƒ «£®°°°°£©ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£Æ∏√∏Ùƒ§ «—Ù¿Î◊”Ωªªªƒ§ |
| B£Æµ±µÁº´…œŒˆ≥ˆ1.08 g Ag ±£¨µÁ¬∑÷–◊™“∆µƒµÁ◊”Œ™0.01 mol |
| C£ÆAlµÁº´µƒ∑¥”¶ ΩŒ™£∫Al-3e-+4OH-=AlO2-+2H2O |
| D£Æ’˝º´µƒµÁº´∑¥”¶ ΩŒ™£∫O2+2H2O+4e-=4OH- |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2012-2013—߃͡…ƒ˛ µ—È÷–—ß∏þ∂˛£®…œ£©∆⁄ƒ©ªØ—ß ‘æÌ£®Ω‚Œˆ∞Ê£© –գ∫—°‘ÒÂ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
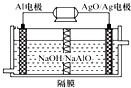
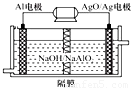
¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al-AgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∆‰‘≠¿Ì»ÁÕºÀ˘ æ°£
∏√µÁ≥ÿ∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™£∫2Al£´3AgO£´2NaOH=2NaAlO2£´3Ag£´H2O£¨
‘Úœ¬¡–Àµ∑®’˝»∑µƒ «
A£Æ∏√∏Ùƒ§ «—Ù¿Î◊”Ωªªªƒ§![]()
B£Æµ±µÁº´…œŒˆ≥ˆ0.54 g Ag ±£¨µÁ¬∑÷–◊™“∆µƒµÁ◊”Œ™0.005 mol
C£ÆAlµÁº´µƒ∑¥”¶ ΩŒ™£∫Al-3e£≠+4OH£≠= ![]() +2H2O
+2H2O
D£Æ’˝º´µƒµÁº´∑¥”¶ ΩŒ™£∫O2+2H2O+4e£≠=4OH£≠
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
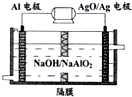 ¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al-AgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∆‰‘≠¿Ì»ÁÕº£Æœ¬¡–Àµ∑®≤ª’˝»∑µƒ «£®°°°°£©
¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al-AgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∆‰‘≠¿Ì»ÁÕº£Æœ¬¡–Àµ∑®≤ª’˝»∑µƒ «£®°°°°£©ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
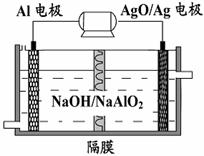
¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al ®CAgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∆‰‘≠¿Ì
»Á”“ÕºÀ˘ æ°£œ¬¡–Àµ∑®≤ª’˝»∑µƒ «
A£Æ‘⁄’˝º´∑¢…˙µƒµÁº´∑¥”¶Œ™£∫AgO+2e-+H2O=Ag+2OH-
B£Æ‘⁄’˝º´«¯H+≈®∂»‘ˆ¥Û£¨‘⁄∏∫º´«¯H+≈®∂»ºı…Ÿ
C£Æ∏√µÁ≥ÿ◊Ð∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫
![]()
D£Æµ±µÁ≥ÿ∏∫º´µƒ÷ ¡ø±‰ªØ10.8g£¨‘Úπ˝≥Ã÷–µÁ≥ÿ¡˜∂صƒµÁ◊”ŒÔ÷ µƒ¡øŒ™1.2NA
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
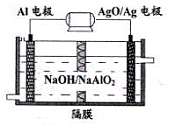
¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al ®CAgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∆‰‘≠¿Ì
»Á”“ÕºÀ˘ æ°£œ¬¡–Àµ∑®≤ª’˝»∑µƒ «
A£Æ‘⁄’˝º´∑¢…˙µƒµÁº´∑¥”¶Œ™£∫AgO+2e-+H2O=Ag+2OH-
B£Æ‘⁄’˝º´«¯H+≈®∂»‘ˆ¥Û£¨‘⁄∏∫º´«¯H+≈®∂»ºı…Ÿ
C£Æ∏√µÁ≥ÿ◊Ð∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫
2Al + 3AgO + 2NaOH= 2NaAlO2 + 3Ag+ H2O
D£Æµ±µÁ≥ÿ∏∫º´µƒ÷ ¡ø±‰ªØ10.8g£¨‘Úπ˝≥Ã÷–µÁ≥ÿ¡˜∂صƒµÁ◊”ŒÔ÷ µƒ¡øŒ™1.2 mol
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2012-2013—߃ÍΩ≠À’ °ƒœÕ® –∫£∞≤œÿ∏þ∂˛…œ—ß∆⁄∆⁄ƒ©øº ‘ªØ—ß ‘æÌ£®¥¯Ω‚Œˆ£© –գ∫ÃÓø’Â
£®14∑÷£©µÁªØ—ß‘≠¿Ì‘⁄œ÷¥˙…˙≤˙…˙ªÓ÷–”–◊≈÷ÿ“™”¶”√°£
¢≈»º¡œµÁ≥ÿ «ƒø«∞∑¢’π ∆Õ∑«ø梵ƒ”≈–„¬Ã…´ª∑±£µÁ≥ÿ°£ƒ≥–¬–Õ«‚—ı»º¡œµÁ≥ÿ“‘H2Œ™»º¡œ£¨O2Œ™—ıªØº¡£¨H2SO4»Ð“∫Œ™µÁΩ‚“∫£©£¨–¥≥ˆ∏√µÁ≥ÿµƒ◊Ð∑¥”¶∑Ω≥Ã Ω£∫ °£
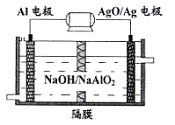
¢∆¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al°™AgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∏√µÁ≥ÿ∑¥”¶µƒ‘≠¿ÌŒ™£∫
Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O°£
¢Ÿ∏√µÁ≥ÿ∑¥”¶µƒ∏∫º´µÁº´∑¥”¶ Ω °£
¢⁄Õº÷–∏Ùƒ§Œ™“ı¿Î◊”Ωªªªƒ§£¨»Ð“∫÷–OH£≠Õ®π˝œÚ º´“∆∂Ø£®—°ÃÓ°∞’˝°±ªÚ°∞∏∫°±£©°£
”√Al°™AgOµÁ≥ÿ◊˜Œ™µÁ‘¥£¨ π”√PtµÁº´µÁΩ‚500mL±•∫ÕNaCl»Ð“∫£¨µÁΩ‚“ª∂Œ ±º‰∫Û£¨ª÷∏¥÷¡ “Œ¬£¨À˘µ√»Ð“∫pH=13£®ºŸ…ËNaCl»Ð“∫◊„¡ø«“µÁΩ‚«∞∫Ûê˝≤ª±‰£©°£
¢€ π”√PtµÁº´µÁΩ‚NaCl»Ð“∫µƒ¿Î◊”∑Ω≥Ã Ω £ª
µÁΩ‚π˝≥Ã÷–∑≈≥ˆ«‚∆¯µƒÃª˝£®±Í◊º◊¥øˆœ¬£©Œ™ L°£
¢Ð»ÙµÁ≥ÿµƒ–߬ Œ™50%£¨∏√π˝≥Ã÷–œ˚∫ƒΩ Ù¬¡µƒ÷ ¡øŒ™ g°£
¢«”√µÁΩ‚∑®÷∆»°√æ ±£¨»Ù‘≠¡œ¬»ªØ√æ∫¨”–ÀÆ ±£¨‘⁄µÁΩ‚Œ¬∂»œ¬£¨‘≠¡œª·–Œ≥…Mg(OH)Cl£¨≤¢∑¢…˙µÁ¿Î£∫Mg(OH)C1 £Ω Mg(OH)£´ £´ C1“ª°£
µÁΩ‚ ±‘⁄“ıº´±Ì√ʪ·≤˙…˙—ıªØ√æ∂€ªØƒ§£¨¥À ±“ıº´µƒ∑¥”¶ ΩŒ™ °£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2014ΩÏΩ≠À’ °ƒœÕ® –∫£∞≤œÿ∏þ∂˛…œ—ß∆⁄∆⁄ƒ©øº ‘ªØ—ß ‘æÌ£®Ω‚Œˆ∞Ê£© –գ∫ÃÓø’Â
£®14∑÷£©µÁªØ—ß‘≠¿Ì‘⁄œ÷¥˙…˙≤˙…˙ªÓ÷–”–◊≈÷ÿ“™”¶”√°£
¢≈»º¡œµÁ≥ÿ «ƒø«∞∑¢’π ∆Õ∑«ø梵ƒ”≈–„¬Ã…´ª∑±£µÁ≥ÿ°£ƒ≥–¬–Õ«‚—ı»º¡œµÁ≥ÿ“‘H2Œ™»º¡œ£¨O2Œ™—ıªØº¡£¨H2SO4»Ð“∫Œ™µÁΩ‚“∫£©£¨–¥≥ˆ∏√µÁ≥ÿµƒ◊Ð∑¥”¶∑Ω≥Ã Ω£∫ °£
¢∆¬¡µÁ≥ÿ–‘ƒÐ”≈‘Ω£¨Al°™AgOµÁ≥ÿø…”√◊˜ÀÆœ¬∂Ø¡¶µÁ‘¥£¨∏√µÁ≥ÿ∑¥”¶µƒ‘≠¿ÌŒ™£∫
Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O°£

¢Ÿ∏√µÁ≥ÿ∑¥”¶µƒ∏∫º´µÁº´∑¥”¶ Ω °£
¢⁄Õº÷–∏Ùƒ§Œ™“ı¿Î◊”Ωªªªƒ§£¨»Ð“∫÷–OH£≠Õ®π˝œÚ º´“∆∂Ø£®—°ÃÓ°∞’˝°±ªÚ°∞∏∫°±£©°£
”√Al°™AgOµÁ≥ÿ◊˜Œ™µÁ‘¥£¨ π”√PtµÁº´µÁΩ‚500mL±•∫ÕNaCl»Ð“∫£¨µÁΩ‚“ª∂Œ ±º‰∫Û£¨ª÷∏¥÷¡ “Œ¬£¨À˘µ√»Ð“∫pH=13£®ºŸ…ËNaCl»Ð“∫◊„¡ø«“µÁΩ‚«∞∫Ûê˝≤ª±‰£©°£
¢€ π”√PtµÁº´µÁΩ‚NaCl»Ð“∫µƒ¿Î◊”∑Ω≥Ã Ω £ª
µÁΩ‚π˝≥Ã÷–∑≈≥ˆ«‚∆¯µƒÃª˝£®±Í◊º◊¥øˆœ¬£©Œ™ L°£
¢Ð»ÙµÁ≥ÿµƒ–߬ Œ™50%£¨∏√π˝≥Ã÷–œ˚∫ƒΩ Ù¬¡µƒ÷ ¡øŒ™ g°£
¢«”√µÁΩ‚∑®÷∆»°√æ ±£¨»Ù‘≠¡œ¬»ªØ√æ∫¨”–ÀÆ ±£¨‘⁄µÁΩ‚Œ¬∂»œ¬£¨‘≠¡œª·–Œ≥…Mg(OH)Cl£¨≤¢∑¢…˙µÁ¿Î£∫Mg(OH)C1 £Ω Mg(OH)£´ £´ C1“ª°£
µÁΩ‚ ±‘⁄“ıº´±Ì√ʪ·≤˙…˙—ıªØ√æ∂€ªØƒ§£¨¥À ±“ıº´µƒ∑¥”¶ ΩŒ™ °£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫ÃÓø’Â

π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com