
下列离子方程式表示错误的是( )
|
科目:高中化学 来源:2010-2011学年山西省阳泉十五中高一(上)期末化学试卷(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题
| A.等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合: HCO3-+Ba2++OH-═BaCO3↓+H2O |
| B.Fe2O3溶于过量氢碘酸溶液中: Fe2O3+6H++2I-═2Fe2++I2+3H2O |
| C.铜片加入稀硝酸中: 3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O |
| D.三氯化铁浓溶液滴入沸水中,制取氢氧化铁胶体: Fe3++3H2O=Fe(OH)3↓+3H+ |
科目:高中化学 来源: 题型:
关于下列各图的叙述错误的是 ( )
 |

| 化学方程式 | 平衡常数K |
| F2+H2 | 6.5×1095 |
| Cl2+H2 | 2.6×1033 |
| Br2+H2 | 1.9×1019 |
| I2 + H2 | 8.7×102 |
图 甲 表 乙 图 丙
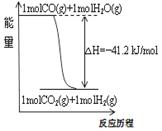
A.已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);ΔH= - 483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B.常温下0.4 mol·L-1 HB溶液和0.2 mol·L-1NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(B-)> c(Na+)>c(H+)>c(OH-)
C.常温下,X2(g)和H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐减小,且HX的还原性逐渐减弱
D.图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,![]() 的变化情况
的变化情况
科目:高中化学 来源:河北省2010届高三一模模拟(三)理综化学部分 题型:选择题
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用下图简单表示(“—”表示铁各种价态的变化,用“—·—”表示碘各种形态的变化)。

下列结论错误的是( )
A.Cl2、I2、IO3-、Fe3+的氧化性依次减小
B.当n(Cl2)/n(FeI2)=1.2时,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl-
C.当n(Cl2)/n(FeI2)=6.5时,溶液中n(Cl-)/n(IO3-)=6.5
D.若溶液的体积不变,则溶液的pH减小
科目:高中化学 来源: 题型:
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用下图简单表示(“—”表示铁各种价态的变化,用“—·—”表示碘各种形态的变化)。

下列结论错误的是( )
A.Cl2、I2、IO3-、Fe3+的氧化性依次减小
B.当n(Cl2)/n(FeI2)=1.2时,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl-
C.当n(Cl2)/n(FeI2)=6.5时,溶液中n(Cl-)/n(IO3-)=6.5
D.若溶液的体积不变,则溶液的pH减小
科目:高中化学 来源: 题型:
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用下图简单表示(“—”表示铁各种价态的变化,用“—·—”表示碘各种形态的变化)。
下列结论错误的是( )
A.Cl2、I2、IO3-、Fe3+的氧化性依次减小
B.当n(Cl2)/n(FeI2)=1.2时,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl-
C.当n(Cl2)/n(FeI2)=6.5时,溶液中n(Cl-)/n(IO3-)=6.5
D.若溶液的体积不变,则溶液的pH减小
科目:高中化学 来源:河北省正定中学2010届高三一模模拟(三)理综化学部分 题型:单选题
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用下图简单表示(“—”表示铁各种价态的变化,用“—·—”表示碘各种形态的变化)。
下列结论错误的是( )
| A.Cl2、I2、IO3-、Fe3+的氧化性依次减小 |
| B.当n(Cl2)/n(FeI2)=1.2时,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl- |
| C.当n(Cl2)/n(FeI2)=6.5时,溶液中n(Cl-)/n(IO3-)=6.5 |
| D.若溶液的体积不变,则溶液的pH减小 |
科目:高中化学 来源:不详 题型:单选题

| A.Cl2、I2、IO3-、Fe3+的氧化性依次减小 |
| B.当n(Cl2)/n(FeI2)=1.2时,反应的离子方程式为2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl- |
| C.当n(Cl2)/n(FeI2)=6.5时,溶液中n(Cl-)/n(IO3-)=6.5 |
| D.若溶液的体积不变,则溶液的pH减小 |
科目:高中化学 来源:不详 题型:单选题

| A.I-、Fe2+、I2的还原性和Cl2、Fe3+、I2的氧化性都依次减小 |
| B.当n(Cl2)/n(FeI2)==1.2时,离子方程式为2Fe2++10I-+6Cl2==5I2+2Fe3++12Cl- |
| C.当n(Cl2)/n(FeI2)==6.5时,溶液中n(Cl-)/n(IO3-)==6.5 |
| D.若溶液体积不变,溶液的pH始终不变 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com