
在C(HCO3-)=0.1mol?L-1的溶液中,可以大量共存的离子组是( )
|
科目:高中化学 来源:不详 题型:单选题
| A.Ca2+、NO3-、NH4+、Cl- | B.Na+、SO42-、C1-、Ca2+ |
| C.H+、Ba2+、Cl-、NO3- | D.Cl-、CO32-、Na+、OH- |
科目:高中化学 来源:2011-2012学年江西省吉安一中高一(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源:2013届江西省高二第二次月考化学试卷 题型:填空题
(10分)
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3-)变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①分别用0.1 mol/L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
②与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快 B.H2SO4最快 C.CH3COOH最快 D.一样快
(3)某温度下,纯水中c(H+)=2×10-7 mol/L,则此时0.02mol/LBa(OH)2溶液的pH =
(4)有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
科目:高中化学 来源: 题型:
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3-)变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①分别用0.1 mol/L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
②与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快 B.H2SO4最快 C.CH3COOH最快 D.一样快
(3)某温度下,纯水中c(H+)=2×10-7 mol/L,则此时0.02mol/LBa(OH)2溶液的pH =
(4)有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
科目:高中化学 来源: 题型:
(10分)
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3-)变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①分别用0.1 mol/L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
②与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快 B.H2SO4最快 C.CH3COOH最快 D.一样快
(3)某温度下,纯水中c(H+)=2×10-7 mol/L,则此时0.02mol/LBa(OH)2溶液的pH =
(4)有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
科目:高中化学 来源:2011-2012学年江西省安福二中高二第二次月考化学试卷 题型:填空题
(10分)
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3-)变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①分别用0.1 mol /L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
/L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
②与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快 B.H2SO4最快 C.CH3COOH最快 D. 一样快
一样快
(3)某温度下,纯水中c(H+)=2×10-7 mol/L,则此时0.02mol/LBa(OH)2溶液的pH =
(4)有四种一元酸HA、HB、HC、H D,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质
D,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质 的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
科目:高中化学 来源:0111 模拟题 题型:填空题

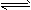 H++HA- HA-
H++HA- HA-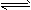 H++A2-
H++A2-科目:高中化学 来源: 题型:
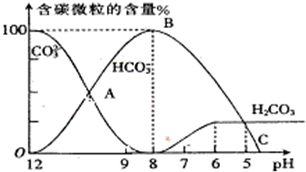 I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:
I.常温下在20mL0.1mol?L-1Na2CO3溶液中逐滴加入0.1mol?L-1 HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.回答下列问题:c(
| ||
c(
|
 H++HA- HA-
H++HA- HA- H++A2-
H++A2-湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com