
下列反应的离子方程式正确的是( )
|
科目:高中化学 来源:2012-2013学年江苏省南通一中高一(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源:2014届湖北省武汉市五校高一上学期期中统考化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是( )
A.Fe与稀H2SO4反应:2Fe + 6H+ == 2Fe3+ + 3H2↑
B.硫酸铜溶液与氢氧化钡溶液反应 :Ba2++ SO42― == BaSO4↓
C.氧化铜溶于硫酸:O2―+2H+ == H2O
D.NaCl溶液与AgNO3溶液反应:Ag++Cl―== AgCl↓
科目:高中化学 来源:2010-2011学年云南省昆明市高三复习教学质量检测(理综)化学部分 题型:选择题
下列反应的离子方程式正确的是 ( )
A.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应:
CH3OH+6OH--6e-=CO2↑+5H2O[来源:学_科_网]
B.在NaHSO4溶液中加Ba(OH)2溶液至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
C.过量氨水与AlCl3溶液反应:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D.向饱和NaCl溶液中通入足量氨气和CO2后有晶体析出:
Na++NH3+CO2+H2O=NaHCO3↓+NH4+
科目:高中化学 来源:不详 题型:单选题
| A.Fe与稀H2SO4反应:2Fe + 6H+ ="=" 2Fe3+ + 3H2↑ |
| B.硫酸铜溶液与氢氧化钡溶液反应:Ba2++ SO42― ="=" BaSO4↓ |
| C.氧化铜溶于硫酸:O2―+2H+ ="=" H2O |
| D.NaCl溶液与AgNO3溶液反应:Ag++Cl―="=" AgCl↓ |
科目:高中化学 来源:2011-2012学年湖北省武汉市五校高一上学期期中统考化学试卷(带解析) 题型:单选题
下列反应的离子方程式正确的是( )
| A.Fe与稀H2SO4反应:2Fe + 6H+ ="=" 2Fe3+ + 3H2↑ |
| B.硫酸铜溶液与氢氧化钡溶液反应:Ba2++ SO42― ="=" BaSO4↓ |
| C.氧化铜溶于硫酸:O2―+2H+ ="=" H2O |
| D.NaCl溶液与AgNO3溶液反应:Ag++Cl―="=" AgCl↓ |
科目:高中化学 来源: 题型:阅读理解
A.《物质结构与性质》
(1)前三周期元素中第一电离能最小的是 _______ (填元素符号),其基态原子的电子排布式为 _______ 。第二周期非金属元素形成的氢化物中化学键极性最大的是 _______
(填分子式),该物质在CCl4中的溶解度比在水中的溶解度 _______ (填“大”或“小”)。
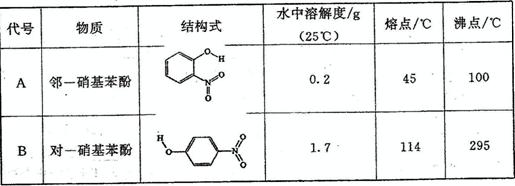 |
(3)晶格能的大小:MgO _______ NaCl,键能的大小:HBr _______ HI。(填“>”、“=”或“<”)
(4)下列物质的熔点高低顺序,正确的是 _______
A.金刚石>晶体硅>二氧化硅>碳化硅
B.CI4 > CBr4 > CCl4 > CH4
C.SiF4 > NaF > NaCl > NaBr
B《实验化学》
七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
表2 两种盐的溶解度(单位为g/100g水)
| 温度 / ℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
硼镁泥制取七水硫酸镁的工艺流程如下:

根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为 _______ 。加热煮沸的主要目的是_ _______ 。
(2)沉淀B中除MnO2、SiO2外还含有 _______ (填化学式)等物质。
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是 _______ ;
(4)沉淀C的化学式是 _______ 。过滤II需趁热过滤的理由是 _______
科目:高中化学 来源:2011-2012学年黑龙江省哈尔滨市高三上学期期末考试化学试卷 题型:选择题
下列说法正确的是( )
A.25℃时NH4Cl溶液的KW大于100℃时NaCl溶液的KW
B. SO2通入碘水中,反应的离子方程式为SO2 + I2 + 2H2O = SO42- + 2I- + 4H+
C. 加入铝粉能产生H2的溶液中,可能存在大量的Na+ 、HCO3-、AlO2— 、NO3—
D. 100℃时,将 pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
科目:高中化学 来源:2012届黑龙江哈尔滨市高三上学期期末考试化学试卷 题型:选择题
下列说法正确的是( )
A.25℃时NH4Cl溶液的KW大于100℃时NaCl溶液的KW
B. SO2通入碘水中,反应的离子方程式为SO2 + I2 + 2H2O = SO42- + 2I- + 4H+
C. 加入铝粉能产生H2的溶液中,可能存在大量的Na+ 、HCO3-、AlO2— 、NO3—
D. 100℃时,将 pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
科目:高中化学 来源:不详 题型:单选题
| A.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O | ||||
| B.亚硫酸氢钠水HSO3-+H2O?SO32-+H3O+ | ||||
| C.氧化铁溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O | ||||
D.用石墨电极电解NaCl溶液:2Cl-+2H2O
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com