
某溶液经分析除含大量H+外,还有Ba2+和Fe2+,则该溶液中还可能大量存在的离子是( )
|
科目:高中化学 来源:2012-2013学年广西桂林十八中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
科目:高中化学 来源: 题型:
(16分)为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下:
合成塔中反应的化学方程式为 ;△H<0。从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了 。
从合成塔分离出甲醇的原理与下列 操作的原理比较相符(填字母)。
A.过滤 B.分液 C.蒸馏 D.结晶
(3)工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施。“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括 。
(4)在体积为2L的合成塔中,充入2 mol CO2和6 mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,v(H2) =______________;能使平衡体系中n(CH3OH)/n(CO2)增大的措施有 。
(5)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
巳知CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3kJ/mol
H2 (g)+ O2(g)=H2O(l) ΔH2=-285.8kJ/mol
写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式________________。
科目:高中化学 来源:2012届安徽省安师大附中高三上学期第四次模拟考试化学试卷 题型:填空题
(16分)为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下: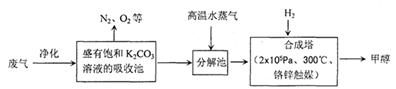
合成塔中反应的化学方程式为 ;△H<0。从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考 虑温度对反应速率的影响外,还主要考虑了 。
虑温度对反应速率的影响外,还主要考虑了 。
从合成塔分离出甲醇的原理与下列 操作的原理比较相符(填字母)。
| A.过滤 | B.分液 | C.蒸馏 | D.结晶 |
科目:高中化学 来源:2011-2012学年安徽省高三上学期第四次模拟考试化学试卷 题型:填空题
(16分)为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下:
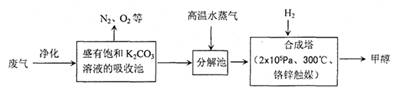
合成塔中反应的化学方程式为 ;△H<0。从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了 。
从合成塔分离出甲醇的原理与下列 操作的原理比较相符(填字母)。
A.过滤 B.分液 C.蒸馏 D.结晶
(3)工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施。“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括 。
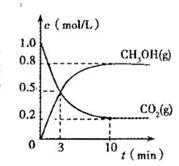
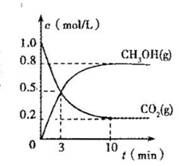
(4)在体积为2L的合成塔中,充入2 mol CO2和6 mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,v(H2) =______________;能使平衡体系中n(CH3OH)/n(CO2)增大的措施有 。
(5)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
巳知CH4(g)+2O2(g)= CO2(g)+2H2O(l) ΔH1=-890.3kJ/mol
H2 (g)+ O2(g)= H2O(l) ΔH2=-285.8kJ/mol
写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式________________。
科目:高中化学 来源:不详 题型:填空题

 虑温度对反应速率的影响外,还主要考虑了 。
虑温度对反应速率的影响外,还主要考虑了 。| A.过滤 | B.分液 | C.蒸馏 | D.结晶 |

科目:高中化学 来源: 题型:
(12分)为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下
(1)合成塔中反应的化学方程式为 ;△H<0。从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了 。
(2)从合成塔分离出甲醇的原理与下列 操作的原理比较相符(填字母)
A.过滤 B.分液 C.蒸馏 D.结晶
工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施。“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括 .
(3)在体积为2L的合成塔中,充人2 mol CO2和6 mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
从反应开始到平衡,V(H2) =______________;能使平衡体系中nCH3OH)/n(CO2)增大的措施有______ __。
(4) 如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
巳知
写出C02(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式________________。
科目:高中化学 来源:2012届浙江省杭州市学军中学高三上学期第一次月考化学试卷 题型:计算题
(12分)为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇。“绿色自由”构想的部分技术流程如下
(1)合成塔中反应的化学方程式为 ;△H<0。从平衡移动原理分析,低温有利于提高原料气的平衡转化率。而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了 。
(2)从合成塔分离出甲醇的原理与下列 操作的原理比较相符(填字母)
| A.过滤 | B.分液 | C.蒸馏 | D.结晶 |
 2和6 mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
2和6 mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
 __。
__。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com