
下列反应最终无沉淀产生的是( )
|
科目:高中化学 来源:2012-2013学年江苏省南通市启东中学高二(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源:2010-2011学年广东省汕头市潮南区胪溪中学高二(上)期末化学试卷(文科)(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题
| A.过量的CO2通入Na2SiO3溶液中 |
| B.向AlCl3溶液中滴加稀氨水至过量 |
| C.少量的CO2通入BaCl2溶液中 |
| D.向MgCl2溶液中滴加NaOH溶液至过量 |
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②④ | C.②③ | D.①④ |
科目:高中化学 来源: 题型:
科目:高中化学 来源:菏泽二模 题型:单选题
| A.某钠盐溶液中加入硝酸无明显现象,再加入氯化钡溶液有白色沉淀,该钠盐一定是硫酸钠 |
| B.在硫酸钡中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
| C.新制氯水中加入碳酸钙粉末搅拌,过滤、滤液中c(HClO)将增大 |
| D.相同质量的两份锌粒分别加入足量稀硫酸,在一份中加入少量CuSO4?5H2O,其反应速率将加快,且最终产生的H2与另一份相同 |
科目:高中化学 来源: 题型:
| A、上述过程中,最终被还原的是NO3- | B、从上述反应可以得出结论,氧化性:HNO3>Fe3+>稀硫酸 | C、上述过程中,会产生一种无色难溶于水的气体 | D、假设通SO2完全反应,同温同压下,SO2和逸出气体的体积比为1:1 |
科目:高中化学 来源: 题型:
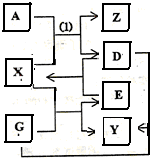 (2011?咸阳模拟)A、D、E、G四种单质和X、Y、Z三种化合物均是中学化学中的重要物质,他们之间有如图所示的转化关系.常温常压下,X是无色无味的液体,Y是黑色晶体,Z的水溶液是一种弱酸,反应(1)不能在玻璃仪器中进行.请回答下列问题:
(2011?咸阳模拟)A、D、E、G四种单质和X、Y、Z三种化合物均是中学化学中的重要物质,他们之间有如图所示的转化关系.常温常压下,X是无色无味的液体,Y是黑色晶体,Z的水溶液是一种弱酸,反应(1)不能在玻璃仪器中进行.请回答下列问题: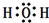
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com