
下列反应中生成H2的速率最快的是( )
|
科目:高中化学 来源:2010-2011学年福建省泉州市安溪一中、养正中学联考高一(下)期末化学试卷(理科)(解析版) 题型:选择题
| 金属 | 酸溶液 | 温度 | |
| ① | Mg | 0.5mol?L-1 H2SO4 | 20℃ |
| ② | Fe | 1mol?L-1 HCl | 20℃ |
| ③ | Mg | 2mol?L-1 HCl | 20℃ |
| ④ | Mg | 1mol?L-1 H2SO4 | 30℃ |
科目:高中化学 来源:2010-2011学年湖北省黄冈市英山一中高一(下)期中化学试卷(解析版) 题型:选择题
| 金属 | 酸溶液 | 温度 | |
| A | Zn | 0.5mol?L-1 H2SO4 | 20℃ |
| B | Fe | 1mol?L-1HCl | 20℃ |
| C | Al | 2mol?L-1HCl | 30℃ |
| D | Mg | 2mol?L-1H2SO4 | 30℃ |
科目:高中化学 来源: 题型:
下列反应中生成H2的速率最快的是( )
| 金属 | 酸溶液 | 温度 | |
| A | Mg | 0.5mol??L-1 H2SO4 | 20℃ |
| B | Fe | 1 mol??L-1 HCl | 20℃ |
| C | Mg | 2 mol??L-1 HCl | 20℃ |
| D | Mg | 1 mol??L-1 H2SO4 | 30℃ |
科目:高中化学 来源:2010年福建省季延中学高一下学期期末考试化学试题 题型:单选题
下列反应中生成H2的速率最快的是( )
| | 金属 | 酸溶液 | 温度 |
| A | Mg | 0.5mol?L-1 H2SO4 | 20℃ |
| B | Fe | 1 mol?L-1 HCl | 20℃ |
| C | Mg | 2 mol?L-1 HCl | 20℃ |
| D | Mg | 1 mol?L-1 H2SO4 | 30℃ |
科目:高中化学 来源: 题型:
下列反应中生成H2的速率最快的是( )
|
科目:高中化学 来源: 题型:
下列反应中生成H2的速率最快的是( )
|
科目:高中化学 来源:不详 题型:单选题
| 金属 | 酸溶液 | 温度 | |
| A | Zn | 0.5mol?L-1 H2SO4 | 20℃ |
| B | Fe | 1mol?L-1HCl | 20℃ |
| C | Al | 2mol?L-1HCl | 30℃ |
| D | Mg | 2mol?L-1H2SO4 | 30℃ |
| A.A | B.B | C.C | D.D |
科目:高中化学 来源:不详 题型:问答题
| 金属 | 酸溶液 | 温度 | |
| ① | Mg | 0.5mol?L-1 H2SO4 | 20℃ |
| ② | Fe | 1mol?L-1 HCl | 20℃ |
| ③ | Mg | 2mol?L-1 HCl | 20℃ |
| ④ | Mg | 1mol?L-1 H2SO4 | 30℃ |
| A.① | B.② | C.③ | D.④ |
科目:高中化学 来源: 题型:阅读理解
 铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:科目:高中化学 来源: 题型:
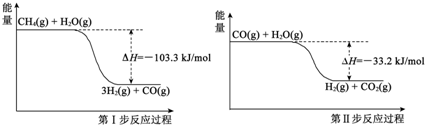 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.| 储氢 | 释氢 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com