
下列有关水溶液中的离子问题的叙述中正确的是( )
|
科目:高中化学 来源:昌平区二模 题型:单选题
| A.pH=12的氨水和pH=2的盐酸溶液等体积混合,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.将pH=11的氨水溶液稀释后,恢复至原温度,pH和Kw均减小 |
| C.向一定量的醋酸溶液中逐滴加入物质的量浓度相同的氢氧化钠溶液,直至氢氧化钠过量,在实验过程中水的电离程度的变化趋势是先小后大 |
| D.在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降 |
科目:高中化学 来源:2011年北京市昌平区高考化学二模试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源:北京市昌平区2011届高三二模理综化学试题 题型:013
|
下列有关水溶液中的离子问题的叙述中正确的是 | |
| [ ] | |
A. |
pH=12的氨水和pH=2的盐酸溶液等体积混合,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
B. |
将pH=11的氨水溶液稀释后,恢复至原温度,pH和Kw均减小 |
C. |
向一定量的醋酸溶液中逐滴加入物质的量浓度相同的氢氧化钠溶液,直至氢氧化钠过量,在实验过程中水的电离程度的变化趋势是先小后大 |
D. |
在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降 |
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源:安徽省合肥润安公学2008-2009学年高三第一学期月考试题化学 题型:013
|
生活中遇到的某些问题,常常涉及到化学,下列叙述正确的是 | |
| [ ] | |
A. |
废旧电池必须进行集中处理的主要原因是回收其中的石墨电极 |
B. |
“雨后彩虹”和“海市蜃楼”现象的出现与胶体的性质有关 |
C. |
被蜂蚁蜇咬会感觉痛痒难忍,若在患处涂抹稀氨水或氢氧化钠溶液,能减轻症状 |
D. |
“加碘食盐”“含氟牙膏”“富硒营养品”“高钙牛奶”“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子 |
科目:高中化学 来源:模拟题 题型:填空题
科目:高中化学 来源: 题型:阅读理解
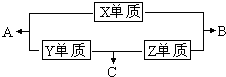 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
| ||
| △ |
| ||
| △ |
| 加热 |
| 加热 |
科目:高中化学 来源:黑龙江省鹤岗一中2011-2012学年高一上学期期末考试化学试题 题型:022
| |||||||||||||||||||||||||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com