
下列离子反应方程式正确的是( )
|
科目:高中化学 来源:2011年四川省绵阳中学高考化学二模试卷(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题
| A.用铁棒电极电解饱和食盐水:2Cl-+2H2O═2OH-+H2↑+Cl2↑ |
| B.工业制漂白粉:Cl2+2OH-=Cl-+ClO-+H2O |
| C.向饱和Na2CO3溶液中通入CO2:2Na++CO32-+CO2+H2O═2NaHCO3↓ |
| D.Ba(OH)2溶液中滴入NaHSO4溶液至恰好呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中正确的是( )
A.氢氧燃料电池在碱性介质中的负极反应式:H2一2e-=2H+
B.用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:
2C1— + 2H2O![]() H2↑ + Cl2↑ + 2OH—
H2↑ + Cl2↑ + 2OH—
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu一2e-=Cu2+
D.用镀层金属作阳极、镀件作阴极,进行电镀
科目:高中化学 来源: 题型:
科目:高中化学 来源: 题型:
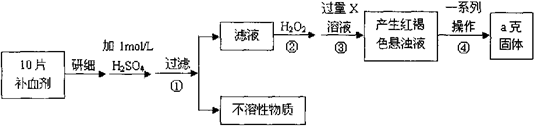
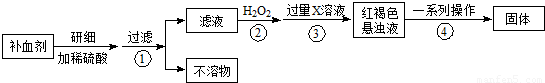
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
请回答下列问题:
(1)步骤②加入过量H2O2的目的:
(2)步骤③中反应的离子方程式:
(3)步骤④中一系列处理的操作步骤:过滤、 、灼烧、 、称量。
(4)若实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)
 (5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+ = 5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是 。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
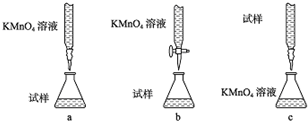
③某同学设计的下列滴定方式中,最合理的是 (夹持部分略去)(填字母序号)

(6)正常人每天应补充14mg左右的铁。其中绝大部分来自于食物。如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含 mg
FeSO4·7H2O的片剂。
科目:高中化学 来源:2010学年广东省汕头市金平区高考化学模拟试卷(解析版) 题型:解答题
科目:高中化学 来源: 题型:解答题

科目:高中化学 来源:2013-2014学年湖北省荆门市高三元月调考理综化学试卷(解析版) 题型:实验题
绿矾晶体(FeSO4·7H2O,M=278g/mol)是治疗缺铁性贫血药品的重要成分。实验室利用硫酸厂的烧渣(主要成分为Fe2O3及少量FeS、SiO2),制备绿矾的过程如下:

试回答:
(1)操作I为 ???????????? (填写操作名称)。
(2)试剂Y与溶液X反应的离子方程式为?????????????????????????????????? 。
(3)操作III的顺序依次为:????????????? 、冷却结晶、过滤、 ????????? 、干燥。
(4)某同学用酸性KMnO4溶液测定绿矾产品中Fe2+含量:
a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。①步骤a配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需???????????????? 。②该同学设计的下列滴定方式,最合理的是?????? (夹持部分略去)(填字母序号)。
③滴定时发生反应的离子方程式为: 。
④判断此滴定实验达到终点的方法是????????????? ;若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,其它操作均正确,则使测定结果???????? (填“偏高”“偏低”“无影响”)。
⑤计算上述样品中FeSO4·7H2O的质量分数为???????????????? 。

科目:高中化学 来源: 题型:实验题
绿矾晶体(FeSO4·7H2O,M=278g/mol)是治疗缺铁性贫血药品的重要成分。实验室利用硫酸厂的烧渣(主要成分为Fe2O3及少量FeS、SiO2),制备绿矾的过程如下: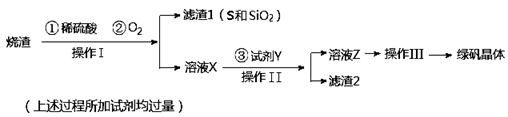
试回答:
(1)操作I为 (填写操作名称)。
(2)试剂Y与溶液X反应的离子方程式为 。
(3)操作III的顺序依次为: 、冷却结晶、过滤、 、干燥。
(4)某同学用酸性KMnO4溶液测定绿矾产品中Fe2+含量:
a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。①步骤a配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需 。②该同学设计的下列滴定方式,最合理的是 (夹持部分略去)(填字母序号)。
③滴定时发生反应的离子方程式为: 。
④判断此滴定实验达到终点的方法是 ;若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,其它操作均正确,则使测定结果 (填“偏高”“偏低”“无影响”)。
⑤计算上述样品中FeSO4·7H2O的质量分数为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com