
物质的量浓度相同(0.1mol?L-1)的弱酸HX与NaX溶液等体积混合后,溶液中粒子浓度关系错误的是( )
|
科目:高中化学 来源:不详 题型:单选题
| A.c(Na+)+c(H+)=c(X-)+c(OH-) |
| B.c(HX)+c(X-)=2c(Na+)? |
| C.若混合液呈酸性则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) |
| D.若混合液呈碱性则c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+) |
科目:高中化学 来源: 题型:
物质的量浓度相同(0.1mol·L-1)的酸HX与NaX溶液等体积混合后,溶液中离子浓度关系错误的是
A、c(Na+)+c(H+)=c(X-)+c(OH-) B、c(HX)+c(X-)=2c(Na+)
C、若混合液呈酸性,则:c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
D、若混合液呈碱性,则:c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+)
科目:高中化学 来源:不详 题型:填空题
科目:高中化学 来源:2010-2011学年江苏省姜堰市高二(下)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源:2010年天津市耀华中学高三暑期验收化学试卷(一)(解析版) 题型:填空题
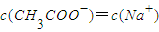 ,则混合后溶液呈 (填“酸“‘碱”或“中”)性,醋酸与氢氧化钠溶液体积大小关系是V(CH3COOH) V(NaOH)(填“>”“=”或“<”).
,则混合后溶液呈 (填“酸“‘碱”或“中”)性,醋酸与氢氧化钠溶液体积大小关系是V(CH3COOH) V(NaOH)(填“>”“=”或“<”).科目:高中化学 来源: 题型:
(8分)物质的量相同的NaHCO3和KHCO3固体混合物9.20g与100mL盐酸反应。
(1)欲求标准状况下生成CO2的体积,还需要什么数据__________________。(讨论(2)的问题中,该数据用a表示)
(2)讨论a值的变化时,产生CO2的体积(标准状况)
| a | 生成CO2的体积(L) |
|
|
|
|
|
|
【解析】(1)物质的量相同的NaHCO3和KHCO3固体混合物是9.20g所以二者的物质的量分别为![]() 。所以要想计算生成CO2的体积,还缺少盐酸的物质的量,即还需要知道盐酸的浓度。
。所以要想计算生成CO2的体积,还缺少盐酸的物质的量,即还需要知道盐酸的浓度。
(2)反应的离子方程式为HCO3-+H+=H2O+CO2↑,HCO3-一共是0.1mol,若和盐酸恰好反应,则盐酸的物质的量是0.1mol,其浓度是1.0mol/L,生成CO2的体积是2.24L。若盐酸不足,即a<1.0mol/L时,生成的CO2的体积为2.24aL。若盐酸过量,即a>1.0mol/L时,生成的CO2是2.24L。
科目:高中化学 来源:2014届山西省高一下学期期中考试理科化学试卷(解析版) 题型:计算题
(8分)物质的量相同的NaHCO3和KHCO3固体混合物9.20g与100mL盐酸反应。
(1)欲求标准状况下生成CO2的体积,还需要什么数据__________________。(讨论(2)的问题中,该数据用a表示)
(2)讨论a值的变化时,产生CO2的体积(标准状况)
|
a |
生成CO2的体积(L) |
|
|
|
|
|
|
【解析】(1)物质的量相同的NaHCO3和KHCO3固体混合物是9.20g所以二者的物质的量分别为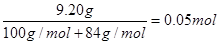 。所以要想计算生成CO2的体积,还缺少盐酸的物质的量,即还需要知道盐酸的浓度。
。所以要想计算生成CO2的体积,还缺少盐酸的物质的量,即还需要知道盐酸的浓度。
(2)反应的离子方程式为HCO3-+H+=H2O+CO2↑,HCO3-一共是0.1mol,若和盐酸恰好反应,则盐酸的物质的量是0.1mol,其浓度是1.0mol/L,生成CO2的体积是2.24L。若盐酸不足,即a<1.0mol/L时,生成的CO2的体积为2.24aL。若盐酸过量,即a>1.0mol/L时,生成的CO2是2.24L。
科目:高中化学 来源: 题型:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com