
œ¬¡–∂‘∏˜÷÷ÃÂœµµƒ– ˆ÷–£¨≤ª’˝»∑µƒ «£®°°°°£©
|
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2012-2013—߃ͅΩ∂´ °º√ƒ˛ –∏þ»˝£®…œ£©∆⁄ƒ©ªØ—ß ‘æÌ£®Ω‚Œˆ∞Ê£© –գ∫—°‘ÒÂ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£Æ‘⁄∫¨FeCl2‘”÷ µƒFeCl3»Ð“∫÷–Õ®»Î◊„¡øC12∫Û£¨≥‰∑÷º”»»≥˝»•π˝¡øCl2£¨µ√µΩΩœ¥ø檵ƒFeCl3»Ð“∫ |
| B£Æ“ª∂®≈®∂»µƒ¥◊À·ƒ∆»Ð“∫ø… π∑”Ù ‘“∫±‰∫Ï£¨∆‰‘≠“Ú «»Ð“∫÷–¥Ê‘⁄»Áœ¬∆Ω∫‚£∫CH3COO-+H2O?CH3COOH+OH-£¨ πµ√»Ð“∫÷–µƒc£®OH-£©£æc£®H+£© |
| C£Æ≥£Œ¬œ¬£¨‘⁄¥◊À·»Ð“∫÷–º”»Î…Ÿ¡øµƒCH3COONaπÃ㨪· π∆‰µÁ¿Î∆Ω∫‚ƒÊœÚ“∆∂Ø |
| D£Æ¥¶¿Ìπ¯¬ØÀÆπ∏÷–µƒCaSO4 ±£¨œ»”√±•∫ÕNa2CO3»Ð“∫¥¶¿Ì£¨‘Ÿº”»Î—ŒÀ·£¨ÀÆπ∏æÕª·»ÐΩ‚ |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2011-2012—߃ͅΩ∂´ °Û{»˝µ⁄“ª¥Œ’Ô∂œ–‘øº ‘ªØ—ß ‘æÌ Ã‚–Õ£∫—°‘ÒÂ
œ¬¡–∂‘∏˜÷÷∆Ω∫‚ÃÂœµµƒ– ˆ÷–£¨ÕÍ»´’˝»∑µƒ «“ª◊È « £® £©
 ¢Ÿ‘⁄¥◊À·»Ð“∫÷–¥Ê‘⁄µƒµÁ¿Î∆Ω∫‚£∫CH3COOH
CH3COO-+H+£¨º”ÀÆœ° Õ∫Û£¨»Ð“∫÷–À˘”–¿Î◊”≈®∂»æ˘ºı–°£ª
¢Ÿ‘⁄¥◊À·»Ð“∫÷–¥Ê‘⁄µƒµÁ¿Î∆Ω∫‚£∫CH3COOH
CH3COO-+H+£¨º”ÀÆœ° Õ∫Û£¨»Ð“∫÷–À˘”–¿Î◊”≈®∂»æ˘ºı–°£ª
¢⁄≥£Œ¬œ¬£¨‘⁄¥◊À·»Ð“∫÷–º”»Î…Ÿ¡øµƒCH3COONaπÃ㨪· π∆‰µÁ¿Î∆Ω∫‚ƒÊœÚ“∆∂Ø£ª
 ¢€ƒ≥Œ¬∂»œ¬£¨»ðª˝“ª∂®µƒ√б’»ð∆˜÷–Ω¯––ø…ƒÊ∑¥”¶£∫X(g)+Y(g)
2Z(g)+W(s); °˜H>0∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∏√ªØ—ß∆Ω∫‚’˝œÚ“∆∂Ø£ª
¢€ƒ≥Œ¬∂»œ¬£¨»ðª˝“ª∂®µƒ√б’»ð∆˜÷–Ω¯––ø…ƒÊ∑¥”¶£∫X(g)+Y(g)
2Z(g)+W(s); °˜H>0∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∏√ªØ—ß∆Ω∫‚’˝œÚ“∆∂Ø£ª
¢Ð‘⁄…œ ˆ¢€µƒø…ƒÊ∑¥”¶÷–£¨µ±»ð∆˜÷–∆¯Ã—π«ø≤ª±‰ ±£¨∑¥”¶¥ÔµΩ∆Ω∫‚£ª
¢ð“ª∂®≈®∂»µƒ¥◊À·ƒ∆»Ð“∫ø… π∑”Ù ‘“∫±‰∫Ï£¨∆‰‘≠“Ú «»Ð“∫÷–¥Ê‘⁄»Áœ¬∆Ω∫‚£∫
 CH3COO-+H2O
CH3COOH+OH- πµ√»Ð“∫÷–µƒc(OH-)>c(H+)
CH3COO-+H2O
CH3COOH+OH- πµ√»Ð“∫÷–µƒc(OH-)>c(H+)
¢Þ‘⁄úÀ·∏∆µƒ≥¡µÌ»ÐΩ‚∆Ω∫‚ÃÂœµ÷–£¨º”»Îœ°—ŒÀ·£¨∆Ω∫‚œÚ»ÐΩ‚µƒ∑ΩœÚ“∆∂Ø
¢þ‘⁄¬»ªØ“¯µƒ≥¡µÌ»ÐΩ‚∆Ω∫‚ÃÂœµ÷–£¨º”»Îµ‚ªØºÿπÃ㨬»ªØ“¯≥¡µÌø…◊™ªØŒ™µ‚ªØ“¯≥¡µÌ
A£Æ¢Ÿ¢⁄¢€¢Ð¢ð B£Æ¢⁄¢€¢Ð¢ð¢Þ C£Æ¢⁄¢€¢ð¢Þ¢þ D£Æ¢Ÿ¢⁄¢ð¢Þ¢þ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
œ¬¡–∂‘∏˜÷÷∆Ω∫‚ÃÂœµµƒ– ˆ÷–£¨ÕÍ»´’˝»∑µƒ «“ª◊È « £® £©
![]() ¢Ÿ‘⁄¥◊À·»Ð“∫÷–¥Ê‘⁄µƒµÁ¿Î∆Ω∫‚£∫CH3COOH CH3COO-+H+£¨º”ÀÆœ° Õ∫Û£¨»Ð“∫÷–À˘”–¿Î◊”≈®∂»æ˘ºı–°£ª
¢Ÿ‘⁄¥◊À·»Ð“∫÷–¥Ê‘⁄µƒµÁ¿Î∆Ω∫‚£∫CH3COOH CH3COO-+H+£¨º”ÀÆœ° Õ∫Û£¨»Ð“∫÷–À˘”–¿Î◊”≈®∂»æ˘ºı–°£ª
¢⁄≥£Œ¬œ¬£¨‘⁄¥◊À·»Ð“∫÷–º”»Î…Ÿ¡øµƒCH3COONaπÃ㨪· π∆‰µÁ¿Î∆Ω∫‚ƒÊœÚ“∆∂Ø£ª
![]() ¢€ƒ≥Œ¬∂»œ¬£¨»ðª˝“ª∂®µƒ√б’»ð∆˜÷–Ω¯––ø…ƒÊ∑¥”¶£∫X(g)+Y(g) 2Z(g)+W(s); °˜H>0∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∏√ªØ—ß∆Ω∫‚’˝œÚ“∆∂Ø£ª
¢€ƒ≥Œ¬∂»œ¬£¨»ðª˝“ª∂®µƒ√б’»ð∆˜÷–Ω¯––ø…ƒÊ∑¥”¶£∫X(g)+Y(g) 2Z(g)+W(s); °˜H>0∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∏√ªØ—ß∆Ω∫‚’˝œÚ“∆∂Ø£ª
¢Ð‘⁄…œ ˆ¢€µƒø…ƒÊ∑¥”¶÷–£¨µ±»ð∆˜÷–∆¯Ã—π«ø≤ª±‰ ±£¨∑¥”¶¥ÔµΩ∆Ω∫‚£ª
¢ð“ª∂®≈®∂»µƒ¥◊À·ƒ∆»Ð“∫ø… π∑”Ù ‘“∫±‰∫Ï£¨∆‰‘≠“Ú «»Ð“∫÷–¥Ê‘⁄»Áœ¬∆Ω∫‚£∫
![]() CH3COO-+H2O CH3COOH+OH- πµ√»Ð“∫÷–µƒc(OH-)>c(H+)
CH3COO-+H2O CH3COOH+OH- πµ√»Ð“∫÷–µƒc(OH-)>c(H+)
¢Þ‘⁄úÀ·∏∆µƒ≥¡µÌ»ÐΩ‚∆Ω∫‚ÃÂœµ÷–£¨º”»Îœ°—ŒÀ·£¨∆Ω∫‚œÚ»ÐΩ‚µƒ∑ΩœÚ“∆∂Ø
¢þ‘⁄¬»ªØ“¯µƒ≥¡µÌ»ÐΩ‚∆Ω∫‚ÃÂœµ÷–£¨º”»Îµ‚ªØºÿπÃ㨬»ªØ“¯≥¡µÌø…◊™ªØŒ™µ‚ªØ“¯≥¡µÌ
A£Æ¢Ÿ¢⁄¢€¢Ð¢ð B£Æ¢⁄¢€¢Ð¢ð¢Þ C£Æ¢⁄¢€¢ð¢Þ¢þ D£Æ¢Ÿ¢⁄¢ð¢Þ¢þ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
 CH3COO-+H+£¨º”ÀÆœ° Õ∫Û£¨»Ð“∫÷–À˘”–¿Î◊”≈®∂»æ˘ºı–°£ª
CH3COO-+H+£¨º”ÀÆœ° Õ∫Û£¨»Ð“∫÷–À˘”–¿Î◊”≈®∂»æ˘ºı–°£ª 2Z(g)+W(s); °˜H>0∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∏√ªØ—ß∆Ω∫‚’˝œÚ“∆∂Ø£ª
2Z(g)+W(s); °˜H>0∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∏√ªØ—ß∆Ω∫‚’˝œÚ“∆∂Ø£ª CH3COOH+OH- πµ√»Ð“∫÷–µƒc(OH-)>c(H+)
CH3COOH+OH- πµ√»Ð“∫÷–µƒc(OH-)>c(H+)| A£Æ¢Ÿ¢⁄¢€¢Ð¢ð | B£Æ¢⁄¢€¢Ð¢ð¢Þ | C£Æ¢⁄¢€¢ð¢Þ¢þ | D£Æ¢Ÿ¢⁄¢ð¢Þ¢þ |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2012ΩÏ…Ω∂´ ° µ—È÷–—ßÛ{»˝µ⁄“ª¥Œ’Ô∂œ–‘øº ‘ªØ—ß ‘æÌ Ã‚–Õ£∫µ•—°Ã‚
œ¬¡–∂‘∏˜÷÷∆Ω∫‚ÃÂœµµƒ– ˆ÷–£¨ÕÍ»´’˝»∑µƒ «“ª◊È « £® £©
¢Ÿ¥◊À·»Ð“∫÷–¥Ê‘⁄µƒµÁ¿Î∆Ω∫‚£∫CH3COOH CH3COO-+H+£¨º”ÀÆœ° Õ∫Û£¨»Ð“∫÷–À˘”–¿Î◊”≈®∂»æ˘ºı–°£ª
CH3COO-+H+£¨º”ÀÆœ° Õ∫Û£¨»Ð“∫÷–À˘”–¿Î◊”≈®∂»æ˘ºı–°£ª
¢⁄≥£Œ¬œ¬£¨‘⁄¥◊À·»Ð“∫÷–º”»Î…Ÿ¡øµƒCH3COONaπÃ㨪· π∆‰µÁ¿Î∆Ω∫‚ƒÊœÚ“∆∂Ø£ª
¢€ƒ≥Œ¬∂»œ¬£¨»ðª˝“ª∂®µƒ√б’»ð∆˜÷–Ω¯––ø…ƒÊ∑¥”¶£∫X(g)+Y(g) 2Z(g)+W(s); °˜H>0∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∏√ªØ—ß∆Ω∫‚’˝œÚ“∆∂Ø£ª
2Z(g)+W(s); °˜H>0∆Ω∫‚∫Û£¨…˝∏þŒ¬∂»£¨∏√ªØ—ß∆Ω∫‚’˝œÚ“∆∂Ø£ª
¢Ð‘⁄…œ ˆ¢€µƒø…ƒÊ∑¥”¶÷–£¨µ±»ð∆˜÷–∆¯Ã—π«ø≤ª±‰ ±£¨∑¥”¶¥ÔµΩ∆Ω∫‚£ª
¢ð“ª∂®≈®∂»µƒ¥◊À·ƒ∆»Ð“∫ø… π∑”Ù ‘“∫±‰∫Ï£¨∆‰‘≠“Ú «»Ð“∫÷–¥Ê‘⁄»Áœ¬∆Ω∫‚£∫
CH3COO-+H2O CH3COOH+OH- πµ√»Ð“∫÷–µƒc(OH-)>c(H+)
CH3COOH+OH- πµ√»Ð“∫÷–µƒc(OH-)>c(H+)
¢Þ‘⁄úÀ·∏∆µƒ≥¡µÌ»ÐΩ‚∆Ω∫‚ÃÂœµ÷–£¨º”»Îœ°—ŒÀ·£¨∆Ω∫‚œÚ»ÐΩ‚µƒ∑ΩœÚ“∆∂Ø
¢þ‘⁄¬»ªØ“¯µƒ≥¡µÌ»ÐΩ‚∆Ω∫‚ÃÂœµ÷–£¨º”»Îµ‚ªØºÿπÃ㨬»ªØ“¯≥¡µÌø…◊™ªØŒ™µ‚ªØ“¯≥¡µÌ
| A£Æ¢Ÿ¢⁄¢€¢Ð¢ð | B£Æ¢⁄¢€¢Ð¢ð¢Þ | C£Æ¢⁄¢€¢ð¢Þ¢þ | D£Æ¢Ÿ¢⁄¢ð¢Þ¢þ |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2012-2013—߃Í∫˛±± °Œ‰∫∫¡˘÷–∏þ»˝£®…œ£©11‘¬¡™øºªØ—߃£ƒ‚ ‘æÌ£®“ª£©£®Ω‚Œˆ∞Ê£© –գ∫ÃÓø’Â

ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
A°¢B°¢C°¢X «÷–—ߪؗß≥£º˚ŒÔ÷ £¨æ˘”…∂Ã÷Ð∆⁄‘™Àÿ◊È≥…£¨◊™ªØπÿœµ»ÁÕºÀ˘ æ°£
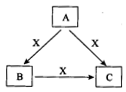
«Î’Î∂‘“‘œ¬≤ªÕ¨«Èøˆªÿ¥£∫
£®1£©»ÙA°¢B°¢Cµƒ—Ê…´∑¥”¶æ˘≥ ª∆…´£¨ÀƻГ∫æ˘Œ™ºÓ–‘°£
¢ŸA÷–À˘∫¨”–µƒªØ—ߺ¸ «_____________°£
¢⁄Ω´4.48 L£®±Í◊º◊¥øˆœ¬£©XÕ®»Î100mL3 mol£ØL AµƒÀƻГ∫∫Û£¨»Ð“∫÷–¿Î◊”≈®∂»”…¥ÛµΩ–°µƒÀ≥–ÚŒ™_______________________________________°£
¢€◊‘»ªΩÁ÷–¥Ê‘⁄B°¢C∫ÕH2O∞¥“ª∂®±»¿˝Ω·æß∂¯≥…µƒπÃ𣻰“ª∂®¡ø∏√πÃûД⁄ÀÆ≈‰≥…100mL»Ð“∫£¨≤‚µ√»Ð»Ð÷–Ω Ù—Ù¿Î◊”µƒ≈®∂»Œ™0.5 mol£ØL°£»Ù»°œýÕ¨÷ ¡øµƒπÃú”»»÷¡∫„÷ÿ£¨ £”ýπÃõƒ÷ ¡øŒ™__________°£
£®2£©»ÙAŒ™πÃè∑«Ω Ùµ•÷ £¨A”ÎXÕ¨÷Ð∆⁄£¨≥£Œ¬≥£—πœ¬CŒ™∞◊…´πÃã¨B∑÷◊”÷–∏˜‘≠◊”◊ÓÕ‚≤„æ˘Œ™8e![]() Ω·ππ°£
Ω·ππ°£
¢Ÿœ¬¡–”–πÿBŒÔ÷ µƒ– ˆ’˝»∑µƒ «
a°¢Bµƒ∑÷◊” ΩŒ™AX b°¢BŒ™π≤º€ªØ∫œŒÔ
c°¢B∑÷◊”≥ »˝Ω«◊∂–Œ d°¢B–‘÷ Œ»∂®£¨≤ª”Î≥˝XÕ‚µƒ»Œ∫ŒŒÔ÷ ∑¢…˙ªØ—ß∑¥”¶
¢⁄C”ÎÀÆæÁ¡“∑¥”¶£¨…˙≥…¡Ω÷÷≥£º˚À·£¨∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ °£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2012ΩÏ’„Ω≠ °…ЖÀ“ª÷–∏þ»˝…œ—ß∆⁄∆⁄÷–øº ‘ªØ—ß ‘æÌ Ã‚–Õ£∫ÃÓø’Â
A°¢B°¢C°¢X «÷–—ߪؗß≥£º˚ŒÔ÷ £¨æ˘”…∂Ã÷Ð∆⁄‘™Àÿ◊È≥…£¨◊™ªØπÿœµ»ÁÕºÀ˘ æ°£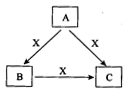
«Î’Î∂‘“‘œ¬≤ªÕ¨«Èøˆªÿ¥£∫
£®1£©»ÙA°¢B°¢Cµƒ—Ê…´∑¥”¶æ˘≥ ª∆…´£¨ÀƻГ∫æ˘Œ™ºÓ–‘°£
¢ŸA÷–À˘∫¨”–µƒªØ—ߺ¸ «_____________°£
¢⁄Ω´4.48 L£®±Í◊º◊¥øˆœ¬£©XÕ®»Î100mL 3 mol£ØL AµƒÀƻГ∫∫Û£¨»Ð“∫÷–¿Î◊”≈®∂»”…¥ÛµΩ–°µƒÀ≥–Ú Œ™_______________________________________°£
Œ™_______________________________________°£
¢€◊‘»ªΩÁ÷–¥Ê‘⁄B°¢C∫ÕH2O∞¥“ª∂®±»¿˝Ω·æß∂¯≥…µƒπÃ𣻰“ª∂®¡ø∏√πÃûД⁄ÀÆ≈‰≥…100mL»Ð“∫£¨≤‚µ√»Ð»Ð÷–Ω Ù—Ù¿Î◊”µƒ≈®∂»Œ™0.5 mol£ØL°£»Ù»°œýÕ¨÷ ¡øµƒπÃú”»»÷¡∫„÷ÿ£¨ £”ýπÃõƒ÷ ¡øŒ™__________°£
£®2£©»ÙAŒ™πÃè∑«Ω Ùµ•÷ £¨A”ÎXÕ¨÷Ð∆⁄£¨≥£Œ¬≥£—πœ¬CŒ™∞◊…´πÃã¨B∑÷◊”÷–∏˜‘≠◊”◊ÓÕ‚≤„æ˘Œ™8e Ω·ππ°£
Ω·ππ°£
¢Ÿœ¬¡–”–πÿBŒÔ÷ µƒ– ˆ’˝»∑µƒ «
a°¢Bµƒ∑÷◊” ΩŒ™AX b°¢BŒ™π≤º€ªØ∫œŒÔ
c°¢B∑÷◊”≥ »˝Ω«◊∂–Œ d°¢B–‘÷ Œ»∂®£¨≤ª”Î≥˝XÕ‚µƒ»Œ∫ŒŒÔ÷ ∑¢…˙ªØ—ß∑¥”¶
¢⁄C”ÎÀÆæÁ¡“∑¥”¶£¨…˙≥…¡Ω÷÷≥£º˚À·£¨∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ °£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com