
‘⁄“ª∂®Ãıº˛œ¬∑¢…˙œ¬¡–∑¥”¶£∫H2£®g£©+Br2£®g£©?2HBr£®g£©£¨∆ º ±£¨»ð∆˜ƒ⁄≥‰»ÎµƒH2£®g£©∫ÕBr2£®g£©∑÷±Œ™3mol∫Õ2mol£¨»ð∆˜µƒ»ðª˝Œ™2L£ª¥ÔµΩ∑¥”¶œÞ∂» ±£¨HBrµƒ≈®∂»Œ™1.56mol/L£Æ‘ÚBr2µƒ◊™ªØ¬ Œ™£®°°°°£©
|
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£Æ78% | B£Æ52% | C£Æ39% | D£Æ0.78% |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2009-2010—߃Í∫”ƒœ °‰∫” –¡ŸÚ£∂˛÷–∏þ“ª£®œ¬£©∆⁄÷–ªØ—ß ‘æÌ£®Ω‚Œˆ∞Ê£© –գ∫—°‘ÒÂ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫0113 ƒ£ƒ‚ –գ∫Õ∆∂œÃ‚
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2010-2011—߃Í∏£Ω® °Àƒµÿ¡˘–£∏þ»˝±œ“µ∞ýøº«∞ƒ£ƒ‚øº ‘£®¿Ì◊€£©ªØ—ß≤ø∑÷ –գ∫ÃÓø’Â
(13∑÷)
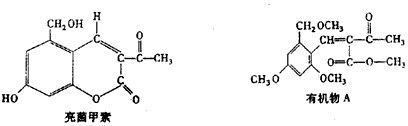
“ª∂®Ãıº˛œ¬£¨¿˚µ®Ω‚æ∑“©°∞¡¡æ˙º◊Àÿ°±∏˙(CH3)2SO4∑¥”¶…˙≥…A°£
∂˛’þµƒΩ·ππºÚ Ω»Áœ¬Õº°£ ‘ªÿ¥£∫

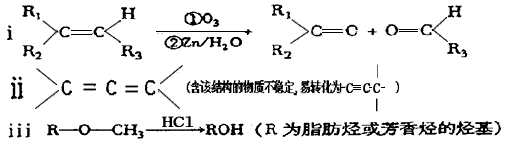
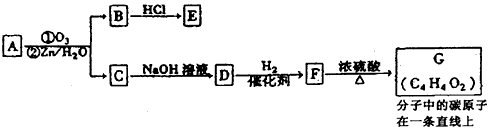
£®1£©°∞¡¡æ˙º◊Àÿ°±µƒ∑÷◊” ΩŒ™_____£¨1mol°∞¡¡æ˙º◊Àÿ°±∏˙≈®‰ÂÀÆ∑¥”¶ ±◊Ó∂ýœ˚∫ƒ____mol Br2£ª”–ª˙ŒÔA≤ªƒÐ∑¢…˙µƒªØ—ß∑¥”¶”–_______(ÃÓ–Ú∫≈)°£
¢Ÿº”≥…∑¥”¶ ¢⁄ı•ªØ∑¥”¶ ¢€ÀÆΩ‚∑¥”¶ ¢Ðœ˚»•∑¥”¶
£®2£©“—÷™£∫

”–ª˙ŒÔAƒÐ∑¢…˙»Áœ¬◊™ªØ£∫
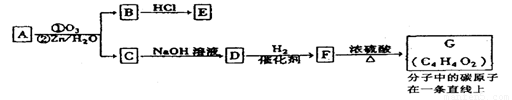
¢ŸC°˙DµƒªØ—ß∑Ω≥Ã ΩŒ™____________________________________°£
¢⁄1mol G∏˙1mol H2‘⁄“ª∂®Ãıº˛œ¬∑¥”¶£¨…˙≥…ŒÔµƒΩ·ππºÚ ΩŒ™___________°£
¢€∑˚∫œœ¬¡–Ãıº˛EµƒÕ¨∑÷“ÏππÔ–_____÷÷£¨–¥≥ˆ∆‰÷–»Œ“‚“ª÷÷µƒΩ·ππºÚ Ω________°£
a£Æ”ˆFeCl3»Ð“∫≥ ◊œ…´£ª b£Æ≤ªƒÐ∑¢…˙ÀÆΩ‚∑¥”¶£¨µ´ƒÐ∑¢…˙“¯æµ∑¥”¶£ª
c£Æ±Ωª∑…œµƒ“ª¬»»°¥˙ŒÔ÷ª”–“ª÷÷£¨«“∑÷◊”÷–ŒÞº◊ª˘°£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
(13∑÷)
“ª∂®Ãıº˛œ¬£¨¿˚µ®Ω‚æ∑“©°∞¡¡æ˙º◊Àÿ°±∏˙(CH3)2SO4∑¥”¶…˙≥…A°£
∂˛’þµƒΩ·ππºÚ Ω»Áœ¬Õº°£ ‘ªÿ¥£∫
£®1£©°∞¡¡æ˙º◊Àÿ°±µƒ∑÷◊” ΩŒ™_____£¨1mol°∞¡¡æ˙º◊Àÿ°±∏˙≈®‰ÂÀÆ∑¥”¶ ±◊Ó∂ýœ˚∫ƒ____mol Br2£ª”–ª˙ŒÔA≤ªƒÐ∑¢…˙µƒªØ—ß∑¥”¶”–_______(ÃÓ–Ú∫≈)°£
¢Ÿº”≥…∑¥”¶ ¢⁄ı•ªØ∑¥”¶ ¢€ÀÆΩ‚∑¥”¶ ¢Ðœ˚»•∑¥”¶
£®2£©“—÷™£∫
”–ª˙ŒÔAƒÐ∑¢…˙»Áœ¬◊™ªØ£∫
¢ŸC°˙DµƒªØ—ß∑Ω≥Ã ΩŒ™____________________________________°£
¢⁄1mol G∏˙1mol H2‘⁄“ª∂®Ãıº˛œ¬∑¥”¶£¨…˙≥…ŒÔµƒΩ·ππºÚ ΩŒ™___________°£
¢€∑˚∫œœ¬¡–Ãıº˛EµƒÕ¨∑÷“ÏππÔ–_____÷÷£¨–¥≥ˆ∆‰÷–»Œ“‚“ª÷÷µƒΩ·ππºÚ Ω________°£
a£Æ”ˆFeCl3»Ð“∫≥ ◊œ…´£ª b£Æ≤ªƒÐ∑¢…˙ÀÆΩ‚∑¥”¶£¨µ´ƒÐ∑¢…˙“¯æµ∑¥”¶£ª
c£Æ±Ωª∑…œµƒ“ª¬»»°¥˙ŒÔ÷ª”–“ª÷÷£¨«“∑÷◊”÷–ŒÞº◊ª˘°£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2011ΩÏ∏£Ω® °Àƒµÿ¡˘–£∏þ»˝±œ“µ∞ýøº«∞ƒ£ƒ‚øº ‘£®¿Ì◊€£©ªØ—ß≤ø∑÷ –գ∫ÃÓø’Â
(13∑÷)
“ª∂®Ãıº˛œ¬£¨¿˚µ®Ω‚æ∑“©°∞¡¡æ˙º◊Àÿ°±∏˙(CH3)2SO4∑¥”¶…˙≥…A°£
∂˛’þµƒΩ·ππºÚ Ω»Áœ¬Õº°£ ‘ªÿ¥£∫
£®1£©°∞¡¡æ˙º◊Àÿ°±µƒ∑÷◊” ΩŒ™_____£¨1mol°∞¡¡æ˙º◊Àÿ°±∏˙≈®‰ÂÀÆ∑¥”¶ ±◊Ó∂ýœ˚∫ƒ____mol Br2£ª”–ª˙ŒÔA≤ªƒÐ∑¢…˙µƒªØ—ß∑¥”¶”–_______(ÃÓ–Ú∫≈)°£
¢Ÿº”≥…∑¥”¶ ¢⁄ı•ªØ∑¥”¶ ¢€ÀÆΩ‚∑¥”¶ ¢Ðœ˚»•∑¥”¶
£®2£©“—÷™£∫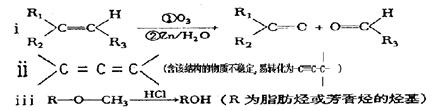
”–ª˙ŒÔAƒÐ∑¢…˙»Áœ¬◊™ªØ£∫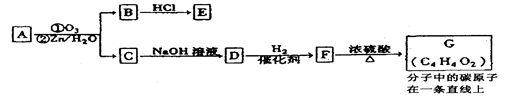
¢ŸC°˙DµƒªØ—ß∑Ω≥Ã ΩŒ™____________________________________°£
¢⁄1mol G∏˙1mol H2‘⁄“ª∂®Ãıº˛œ¬∑¥”¶£¨…˙≥…ŒÔµƒΩ·ππºÚ ΩŒ™___________°£
¢€∑˚∫œœ¬¡–Ãıº˛EµƒÕ¨∑÷“ÏππÔ–_____÷÷£¨–¥≥ˆ∆‰÷–»Œ“‚“ª÷÷µƒΩ·ππºÚ Ω________°£
a£Æ”ˆFeCl3»Ð“∫≥ ◊œ…´£ª b£Æ≤ªƒÐ∑¢…˙ÀÆΩ‚∑¥”¶£¨µ´ƒÐ∑¢…˙“¯æµ∑¥”¶£ª
c£Æ±Ωª∑…œµƒ“ª¬»»°¥˙ŒÔ÷ª”–“ª÷÷£¨«“∑÷◊”÷–ŒÞº◊ª˘°£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫ÃÓø’Â



ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2009-2010—߃Í∫”±±ºΩ÷ð÷–—ß∏þ“ªœ¬—ß∆⁄∆⁄÷–øº ‘ªØ—ßæÌ Ã‚–Õ£∫ÃÓø’Â
ÃÓø’Â
£®1£©œ¬¡–Àµ∑®÷–’˝»∑µƒ «
¢Ÿ√≈Ωð¡–∑ÚªÊ÷∆≥ˆ¡Àµ⁄“ª’≈Œ“√«œ÷‘⁄≥£”√µƒ‘™Àÿ÷Ð∆⁄±Ì°£¢⁄ÃÏ»ª¥Ê‘⁄µƒÕ¨ŒªÀÿ£¨œýª•º‰±£≥÷“ª∂®µƒ±»¬ °£¢€‘™Àÿµƒ–‘÷ ÀÊ◊≈‘≠◊”¡øµƒµð‘ˆ∂¯≥ ÷Ð∆⁄–‘±‰ªØµƒπʬ…Ω–◊ˆ‘™Àÿ÷Ð∆⁄¬…°£¢Ð»º¡œµÁ≥ÿ”Î∏…µÁ≥ÿµƒ÷˜“™≤Ó±‘⁄”⁄∑¥”¶ŒÔ≤ªÕ¨°£¢ðÕ¨œµŒÔ÷ƺ‰∑÷◊”¡øœý≤Ó14°£¢Þ”…”⁄¥Ê‘⁄ªØ—ß∑¥”¶µƒœÞ∂»£¨À˘“‘“ª∏ˆªØ—ß∑¥”¶‘⁄ µº Ω¯–– ±≤ª“ª∂®∞¥’’ªØ—ß∑Ω≥Ã Ωµƒº∆¡øπÿœµΩ¯––°£¢þ∏˜÷÷ŒÔ÷ ∂º¥¢¥Ê”–ªØ—߃а£¢ýº◊ÕÈ∫Õ¬»ÀÆ‘⁄π‚’’Ãıº˛œ¬∑¢…˙»°¥˙∑¥”¶£¨≤˙ŒÔŒ™ªÏ∫œŒÔ°£
£®2£©”√–ø∆¨°¢Õ≠∆¨¡¨Ω”∫ÛΩ˛»Îœ°¡ÚÀ·»Ð“∫÷–£¨ππ≥…¡À‘≠µÁ≥ÿ£¨π§◊˜“ª∂Œ ±º‰£¨–ø∆¨
µƒ÷ ¡øºı…Ÿ¡À3.25øÀ£¨Õ≠±Ì√ÊŒˆ≥ˆ¡À«‚∆¯ L£®±Í◊º◊¥øˆœ¬£©£¨µºœþ÷–Õ®π˝ molµÁ◊”°£
£®3£©‘⁄25°Ê ±£¨œÚ100 mL∫¨¬»ªØ«‚14.6 gµƒ—ŒÀ·»Ð“∫¿Ô∑≈»Î5.60 g¥øÃ˙∑€£®≤ªøº¬«∑¥”¶«∞∫ۻГ∫ê˝µƒ±‰ªØ£©£¨∑¥”¶ø™ º÷¡2 minƒ©£¨ ’ºØµΩ1.12 L£®±Í◊º◊¥øˆ£©«‚∆¯°£‘⁄¥À÷Æ∫Û£¨”÷æ≠π˝4 min£¨Ã˙∑€ÕÍ»´»ÐΩ‚°£‘Ú£∫ «∞2 min”Î∫Û4 minœý±»£¨∑¥”¶ÀŸ¬ Ωœøϵƒ « £¨∆‰‘≠“Ú «
£®4£©“—÷™œ¬¡–‘≠µÁ≥ÿµƒ◊Ð∑¥”¶ Ω£∫Cu+2FeCl3==CuCl2+2FeCl2£¨«Î–¥≥ˆµÁº´∑¥”¶∑Ω≥Ã Ω£∫
’˝º´∑¥”¶∑Ω≥Ã ΩŒ™£∫
∏∫º´∑¥”¶∑Ω≥Ã ΩŒ™£∫
£®5£©“—÷™∂œø™1 molH-Hº¸°¢1mol Br-Brº¸°¢1mol H-Brº¸∑÷±–Ë“™Œ¸ ’µƒƒÐ¡øŒ™436kJ°¢193kJ°¢366kJ.°£ º∆À„H2∫ÕBr2∑¥”¶…˙≥…1mol HBr–Ë_______(ÃÓ°∞Œ¸ ’°±ªÚ°∞∑≈≥ˆ°±)ƒÐ¡ø_______kJ°£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫‘ƒ∂¡¿ÌΩ‚
£®18∑÷£©”¶”√ªØ—ß∑¥”¶–Ë“™—–æøªØ—ß∑¥”¶µƒÃıº˛°¢œÞ∂»∫ÕÀŸ¬ °£
![]() £®1£©“—÷™∑¥”¶£∫Br2£´2Fe2+=2Br£≠£´2Fe3+£¨œÚ10 mL 0.1 mol?L£≠1µƒFeBr2»Ð“∫÷–Õ®»Î0.001mol Cl2£¨∑¥”¶∫Û£¨»Ð“∫÷–≥˝∫¨”–Cl-Õ‚£¨ªπ“ª∂® (ÃÓ–Ú∫≈)°£
£®1£©“—÷™∑¥”¶£∫Br2£´2Fe2+=2Br£≠£´2Fe3+£¨œÚ10 mL 0.1 mol?L£≠1µƒFeBr2»Ð“∫÷–Õ®»Î0.001mol Cl2£¨∑¥”¶∫Û£¨»Ð“∫÷–≥˝∫¨”–Cl-Õ‚£¨ªπ“ª∂® (ÃÓ–Ú∫≈)°£
![]() ¢Ÿ ∫¨Fe2+£¨≤ª∫¨Fe3+ ¢⁄ ∫¨Fe3+£¨≤ª∫¨Br- ¢€ ∫¨Fe3+£¨∫¨”–Br-
¢Ÿ ∫¨Fe2+£¨≤ª∫¨Fe3+ ¢⁄ ∫¨Fe3+£¨≤ª∫¨Br- ¢€ ∫¨Fe3+£¨∫¨”–Br-
![]() £®2£©773 K£¨πÃ∂®Ãª˝µƒ»ð∆˜÷–£¨∑¥”¶CO(g)£´2H2(g)
£®2£©773 K£¨πÃ∂®Ãª˝µƒ»ð∆˜÷–£¨∑¥”¶CO(g)£´2H2(g) ![]() CH3OH(g)π˝≥Ã÷–ƒÐ¡ø±‰ªØ»Áœ¬Õº°£«˙œþ¢Ú±Ì æ π”√¥þªØº¡ ±µƒƒÐ¡ø±‰ªØ°£»ÙÕ∂»Îa mol CO°¢2a mol H2£¨∆Ω∫‚ ±ƒÐ…˙≥…0.1a mol CH3OH£¨∑¥”¶æÕæþ𧓵”¶”√º€÷µ°£
CH3OH(g)π˝≥Ã÷–ƒÐ¡ø±‰ªØ»Áœ¬Õº°£«˙œþ¢Ú±Ì æ π”√¥þªØº¡ ±µƒƒÐ¡ø±‰ªØ°£»ÙÕ∂»Îa mol CO°¢2a mol H2£¨∆Ω∫‚ ±ƒÐ…˙≥…0.1a mol CH3OH£¨∑¥”¶æÕæþ𧓵”¶”√º€÷µ°£
¢Ÿ »Ù∞¥…œ ˆÕ∂¡œ±» π∏√∑¥”¶æþ”–𧓵”¶”√º€÷µ£¨COµƒ∆Ω∫‚◊™ªØ¬ Œ™ £ª
¢⁄ ‘⁄»ð∆˜»ðª˝≤ª±‰µƒ«∞÷œ¬£¨”˚÷∏þH2µƒ◊™ªØ¬ £¨ø…≤…»°µƒ¥Î ©(¥¡ΩœÓº¥ø…) °¢ £ª
¢€ œ¬¡–”Î¥þªØº¡”–πÿµƒÀµ∑®÷–£¨’˝»∑µƒ « (ÃÓ◊÷ƒ∏–Ú∫≈)°£
a. π”√¥þªØº¡£¨ π∑¥”¶CO(g)£´2H2(g) ![]() CH3OH(g) ¶§H>£≠91 kJ?mol£≠1
CH3OH(g) ¶§H>£≠91 kJ?mol£≠1
b. π”√¥þªØº¡£¨≤ªƒÐ∏ƒ±‰∑¥”¶µƒ∆Ω∫‚≥£ ˝K
c. π”√¥þªØº¡£¨ƒÐπªÃ·∏þ∑¥”¶ŒÔ◊™ªØ¬
![]() £®3£©∏þÃ˙À·—Œ‘⁄ƒÐ‘¥ª∑±£¡Ï”Ú”–π„∑∫”√Õæ°£Œ“π˙—ß’þ÷≥ˆ”√ƒ¯(Ni)°¢Ã˙◊˜µÁº´µÁΩ‚≈®NaOH»Ð“∫÷∆±∏∏þÃ˙À·—ŒNa2FeO4µƒ∑Ω∞∏£¨◊∞÷√»Á”“ÕºÀ˘ æ°£
£®3£©∏þÃ˙À·—Œ‘⁄ƒÐ‘¥ª∑±£¡Ï”Ú”–π„∑∫”√Õæ°£Œ“π˙—ß’þ÷≥ˆ”√ƒ¯(Ni)°¢Ã˙◊˜µÁº´µÁΩ‚≈®NaOH»Ð“∫÷∆±∏∏þÃ˙À·—ŒNa2FeO4µƒ∑Ω∞∏£¨◊∞÷√»Á”“ÕºÀ˘ æ°£
¢Ÿ FeµÁº´◊˜ º´(ÃÓ°∞“ı°±ªÚ°∞—Ù°±)£ª
¢⁄ NiµÁº´µƒµÁº´∑¥”¶ ΩŒ™£∫ °£
£®4£©—ıªØªπ‘≠∑¥”¶÷– µº …œ∞¸∫¨—ıªØ∫Õªπ‘≠¡Ω∏ˆπ˝≥𣜬√Ê «HNO3∑¢…˙µƒ“ª∏ˆªπ‘≠π˝≥õƒ∑¥”¶ Ω£∫
NO3-£´4H+£´3e£≠= NO£´2H2O
¢ŸKMnO4°¢Na2CO3°¢CuO°¢KIÀƒ÷÷ŒÔ÷ ÷–µƒ (Ãѧ Ω)ƒÐ π…œ ˆªπ‘≠π˝≥Ã∑¢…˙°£
¢⁄”˚”√œ¬Õº◊∞÷√Õ®π˝≤‚∂®∆¯ÃÂ…˙≥…¡ø≤‚À„œıÀ·±ªªπ‘≠µƒÀŸ¬ £¨µ±∑¥”¶ŒÔµƒ≈®∂»°¢”√¡øº∞∆‰À˚”∞œÏÀŸ¬ µƒÃıº˛»∑∂®÷Æ∫Û£¨ø…“‘Õ®π˝≤‚∂® Õ∆(º∆)À„∑¥”¶ÀŸ¬ °£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com