
在下列各说法中,正确的是( )
|
科目:高中化学 来源:2012-2013学年云南省西双版纳州景洪四中高二(上)期中化学试卷(理科)(解析版) 题型:选择题
科目:高中化学 来源:2011年内蒙古包头市青山区北重三中高考化学一轮复习卷(三)(解析版) 题型:选择题
科目:高中化学 来源:不详 题型:单选题
| A.△H>0kJ?mol-1表示放热反应,△H<0kJ?mol-1表示吸热反应 |
| B.热化学方程式中的化学计量数只表示物质的量,可以是分数 |
| C.1molH2SO4与1molBa(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
| D.1molH2与0.5molO2反应放出的热就是H2的燃烧热 |
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:问答题

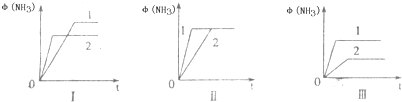
| 物 质 | 燃烧热(kJ?mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
科目:高中化学 来源:2009年安徽省高考化学押题试卷(解析版) 题型:解答题
 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.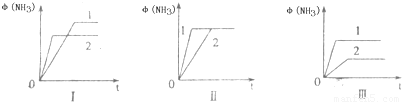
 H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发______(填:能或否).
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发______(填:能或否).| 物 质 | 燃烧热 |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
科目:高中化学 来源: 题型:阅读理解
 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.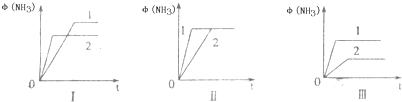
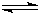 H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发| 物 质 | 燃烧热(kJ?mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
科目:高中化学 来源: 题型:
| 1 | 2 |
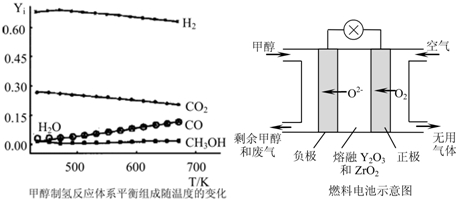
科目:高中化学 来源: 题型:阅读理解
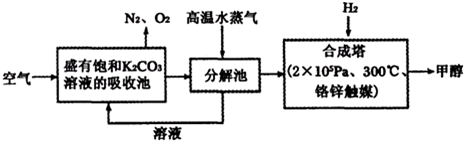
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol?L-1) | 0.2 | 0.2 | 0.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com