
| œ¬¡–∂‘ªØ—ß∆Ω∫‚”–πÿµƒ∑÷Œˆ÷–£¨≤ª’˝»∑µƒ «£®°°°°£© ¢Ÿ“—¥Ô∆Ω∫‚µƒ∑¥”¶C£®s£©+H2O£®g£©?CO£®g£©+H2£®g£©£¨µ±‘ˆº”∑¥”¶ŒÔŒÔ÷ µƒ¡ø ±£¨∆Ω∫‚“ª∂®œÚ’˝∑¥”¶∑ΩœÚ“∆∂Ø ¢⁄“—¥Ô∆Ω∫‚µƒ∑¥”¶N2£®g£©+3H2£®g£©?2NH3£®g£©£¨µ±‘ˆ¥ÛN2µƒ≈®∂» ±£¨∆Ω∫‚œÚ’˝∑¥”¶∑ΩœÚ“∆∂Ø£¨H2µƒ◊™ªØ¬ “ª∂®…˝∏þ ¢€ø…ƒÊ∑¥”¶2SO2+O2?2SO3£¨µ±ªÏ∫œ∆¯Ãµƒ√Ð∂»“ª∂® ±£¨∑¥”¶“ª∂®¥ÔµΩ∆Ω∫‚ ¢Ð”–∆¯ÃÂ≤Œº”µƒ∑¥”¶¥Ô∆Ω∫‚ ±£¨”¶µ±”–V’˝£®∆¯£©=VƒÊ£®∆¯£©=0£Æ
|
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2007-2008—߃ÍΩ≠À’ °¡¨‘∆∏€ –πý‘∆∏þº∂÷–—ß∏þ“ª£®œ¬£©∆⁄ƒ©ªØ—ß ‘æÌ£®“ª£©£®Ω‚Œˆ∞Ê£© –գ∫—°‘ÒÂ
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫∫”ƒœ °ƒ£ƒ‚ –գ∫ÃÓø’Â
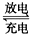 2PbSO4(s) +2H2O(l)°£µÁΩ‚“ª∂Œ ±º‰∫Û£¨œÚcº´∫Õdº´∏ΩΩ¸∑÷±µŒº”∑”Ù ‘º¡£¨cº´∏ΩΩ¸»Ð“∫±‰∫Ï£¨œ¬¡–Àµ∑®’˝»∑µƒ «____________£®ÃÓ–¥–Ú∫≈£©°£
2PbSO4(s) +2H2O(l)°£µÁΩ‚“ª∂Œ ±º‰∫Û£¨œÚcº´∫Õdº´∏ΩΩ¸∑÷±µŒº”∑”Ù ‘º¡£¨cº´∏ΩΩ¸»Ð“∫±‰∫Ï£¨œ¬¡–Àµ∑®’˝»∑µƒ «____________£®ÃÓ–¥–Ú∫≈£©°£ 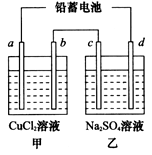
 H++A2-°£
H++A2-°£  CH3OH(g) °˜H=-90.8kJ/mol
CH3OH(g) °˜H=-90.8kJ/mol  CH3OCH3(g)+H2O(g) °˜H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) °˜H=-23.5kJ/mol  CO2(g)+H2(g) °˜H=-41.3kJ/mol
CO2(g)+H2(g) °˜H=-41.3kJ/mol  2SO3(g)°£‘⁄“ª∂®Œ¬∂»œ¬£¨Ω´0.23molSO2∫Õ0.11molO2Õ®»Î»ðª˝Œ™1Lµƒ√б’»ð∆˜÷–∑¢…˙∑¥”¶£¨¥ÔµΩ∆Ω∫‚∫Ûµ√µΩ0.12molSO3£¨‘Ú∑¥”¶µƒ∆Ω∫‚≥£ ˝K=__________°£»ÙŒ¬∂»≤ª±‰£¨‘ŸÕ®»Î0.50molO2∫Û÷ÿ–¬¥ÔµΩ∆Ω∫‚£¨‘ÚSO3µƒÃª˝∑÷ ˝Ω´__________£®ÃÓ°∞‘ˆ¥Û°±°∞≤ª±‰°±ªÚ°∞ºı–°°±£©°£
2SO3(g)°£‘⁄“ª∂®Œ¬∂»œ¬£¨Ω´0.23molSO2∫Õ0.11molO2Õ®»Î»ðª˝Œ™1Lµƒ√б’»ð∆˜÷–∑¢…˙∑¥”¶£¨¥ÔµΩ∆Ω∫‚∫Ûµ√µΩ0.12molSO3£¨‘Ú∑¥”¶µƒ∆Ω∫‚≥£ ˝K=__________°£»ÙŒ¬∂»≤ª±‰£¨‘ŸÕ®»Î0.50molO2∫Û÷ÿ–¬¥ÔµΩ∆Ω∫‚£¨‘ÚSO3µƒÃª˝∑÷ ˝Ω´__________£®ÃÓ°∞‘ˆ¥Û°±°∞≤ª±‰°±ªÚ°∞ºı–°°±£©°£ ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫‘ƒ∂¡¿ÌΩ‚
| ¥þªØº¡ |
| °˜ |
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫2014ΩÏ∫˛ƒœ °ª≥ªØ –∏þ∂˛…œ—ß∆⁄∆⁄ƒ©øº ‘¿Ìø∆ªØ—ß ‘æÌ£®Ω‚Œˆ∞Ê£© –գ∫ÃÓø’Â
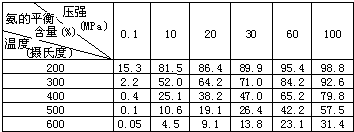
£®16∑÷£©π§“µ…œø…“‘‘⁄∫„»ð√б’»ð∆˜÷–≤…”√œ¬¡–∑¥”¶÷∆±∏º◊¥º£∫
CO£®g£©£´2H2£®g£© CH3OH£®g£©
CH3OH£®g£©
£®1£©œ¬¡–«Èøˆø…“‘◊˜Œ™≈–∂œ∑¥”¶¥ÔµΩ∆Ω∫‚◊¥Ã¨µƒ“¿æ𵃠«£®ÃÓ–Ú∫≈£© °£
A£Æ…˙≥…CH3OH µƒÀŸ¬ ”Îœ˚∫ƒH2µƒÀŸ¬ ÷Ʊ»Œ™1©U2
B£ÆªÏ∫œ∆¯Ãµƒ∆Ωæ˘œý∂‘∑÷◊”÷ ¡ø±£≥÷≤ª±‰
C£ÆªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
D£ÆÃÂœµƒ⁄µƒ—π«ø±£≥÷≤ª±‰
£®2£©œ¬±ÌÀ˘¡– ˝æðŒ™∏√∑¥”¶‘⁄≤ªÕ¨Œ¬∂»œ¬µƒªØ—ß∆Ω∫‚≥£ ˝£∫
|
Œ¬∂»/°Ê |
250 |
300 |
350 |
|
K |
2.041 |
0.270 |
0.012 |
¢Ÿ∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô ΩŒ™K= °£”……œ±Ì ˝æð≈–∂œ£¨∏√∑¥”¶µƒ°˜H 0£®ÃÓ°∞£æ°±°¢°∞£Ω°±ªÚ°∞£º°±£©°£…˝∏þŒ¬∂»£¨’˝∑¥”¶ÀŸ¬ £®ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±£©°£
¢⁄ƒ≥Œ¬∂»œ¬£¨Ω´2molCO∫Õ6molH2≥‰»Î“ª∏ˆ»ðª˝Œ™2Lµƒ√б’»ð∆˜÷–£¨¥ÔµΩ∆Ω∫‚ ±c(H2)=1.4mol/L£¨‘ÚCOµƒ◊™ªØ¬ Œ™ £¨¥À ±µƒŒ¬∂»Œ™ °£
£®3£©”˚÷∏þCOµƒ◊™ªØ¬ £¨ø…≤…»°µƒ¥Î © « °££®ÃÓ–Ú∫≈£©
A£Æ…˝Œ¬
B£Æº”»Î∏¸∏þ–ßµƒ¥þªØº¡
C£Æ∫„»ðÃıº˛œ¬≥‰»ÎCO
D£Æ∫„»ðÃıº˛œ¬≥‰»ÎH£≤
E£Æ∫„»ðÃıº˛œ¬≥‰»Î∫§∆¯
F£Æº∞ ±“∆◊þCH3OH
£®4£©“ª∂®Ãıº˛œ¬£¨CO∫ÕH2‘⁄¥þªØº¡◊˜”√œ¬…˙≥…1molCH3OHµƒƒÐ¡ø±‰ªØŒ™90.8kJ°£∏√Œ¬∂»œ¬£¨‘⁄»˝∏ˆ»ðª˝œýÕ¨µƒ√б’»ð∆˜÷–£¨∞¥≤ªÕ¨∑Ω ΩÕ∂¡œ£¨±£≥÷∫„Œ¬°¢∫„»ð£¨≤‚µ√∑¥”¶¥ÔµΩ∆Ω∫‚ ±µƒ”–πÿ ˝æð»Áœ¬£∫
|
»ð∆˜ |
º◊ |
““ |
±˚ |
|
|
Õ∂¡œ∑Ω Ω |
1molCO°¢ 2molH2 |
1molCH3OH |
2molCH3OH |
|
|
∆Ω∫‚ ˝æð |
C(CH3OH)/(mol/L) |
c1 |
c2 |
c3 |
|
ÃÂœµ—π«ø(Pa) |
p1 |
p2 |
p3 |
|
|
∑¥”¶µƒƒÐ¡ø±‰ªØ |
akJ |
bkJ |
ckJ |
|
|
‘≠¡œ◊™ªØ¬ |
¶¡1 |
¶¡2 |
¶¡3 |
œ¬¡–∑÷Œˆ’˝»∑µƒ « °££®ÃÓ–Ú∫≈£©
A£Æ2c1 £ºc3 B£Æ2 p1 £ºp3 C£Æ|a|£´|b|£Ω90.8 D£Æ¶¡1£´¶¡3£æ1
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫ÃÓø’Â
£®16∑÷£©π§“µ…œø…“‘‘⁄∫„»ð√б’»ð∆˜÷–≤…”√œ¬¡–∑¥”¶÷∆±∏º◊¥º£∫
CO£®g£©£´2H2£®g£© CH3OH£®g£©
CH3OH£®g£©
£®1£©œ¬¡–«Èøˆø…“‘◊˜Œ™≈–∂œ∑¥”¶¥ÔµΩ∆Ω∫‚◊¥Ã¨µƒ“¿æ𵃠«£®ÃÓ–Ú∫≈£© °£
A£Æ…˙≥…CH3OH µƒÀŸ¬ ”Îœ˚∫ƒH2µƒÀŸ¬ ÷Ʊ»Œ™1©U2
B£ÆªÏ∫œ∆¯Ãµƒ∆Ωæ˘œý∂‘∑÷◊”÷ ¡ø±£≥÷≤ª±‰
C£ÆªÏ∫œ∆¯Ãµƒ√Ð∂»±£≥÷≤ª±‰
D£ÆÃÂœµƒ⁄µƒ—π«ø±£≥÷≤ª±‰
£®2£©œ¬±ÌÀ˘¡– ˝æðŒ™∏√∑¥”¶‘⁄≤ªÕ¨Œ¬∂»œ¬µƒªØ—ß∆Ω∫‚≥£ ˝£∫
| Œ¬∂»/°Ê | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| »ð∆˜ | º◊ | ““ | ±˚ | |
| Õ∂¡œ∑Ω Ω | 1molCO°¢2molH2 | 1molCH3OH | 2molCH3OH | |
| ∆Ω∫‚ ˝æð | C(CH3OH)/(mol/L) | c1 | c2 | c3 |
| ÃÂœµ—π«ø(Pa) | p1 | p2 | p3 | |
| ∑¥”¶µƒƒÐ¡ø±‰ªØ | akJ | bkJ | ckJ | |
| ‘≠¡œ◊™ªØ¬ | ¶¡1 | ¶¡2 | ¶¡3 | |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫ÃÓø’Â
 CH3OH£®g£©
CH3OH£®g£©| Œ¬∂»/°Ê | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| »ð∆˜ | º◊ | ““ | ±˚ | |
| Õ∂¡œ∑Ω Ω | 1molCO°¢2molH2 | 1molCH3OH | 2molCH3OH | |
| ∆Ω∫‚ ˝æð | C(CH3OH)/(mol/L) | c1 | c2 | c3 |
| ÃÂœµ—π«ø(Pa) | p1 | p2 | p3 | |
| ∑¥”¶µƒƒÐ¡ø±‰ªØ | akJ | bkJ | ckJ | |
| ‘≠¡œ◊™ªØ¬ | ¶¡1 | ¶¡2 | ¶¡3 | |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫µ•—°Ã‚
| A£Æ¢Ÿ¢€¢Ð | B£Æ¢Ÿ¢⁄ | C£Æ¢⁄¢Ð | D£Æ¢Ÿ¢⁄¢€¢Ð |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫‘ƒ∂¡¿ÌΩ‚
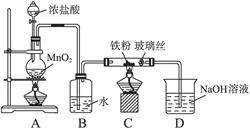
œ÷”–“ª∑ð∫¨”–FeCl3∫ÕFeCl2µƒπÃêÏ∫œŒÔ£¨Œ™≤‚∂®∏˜≥…∑÷µƒ∫¨¡øΩ¯––»Áœ¬¡Ω∏ˆ µ—È£∫
µ—È1
¢Ÿ≥∆»°“ª∂®÷ ¡øµƒ—˘∆∑£¨Ω´—˘∆∑»ÐΩ‚£ª
¢⁄œÚ»ÐΩ‚∫Ûµƒ»Ð“∫÷–º”»Î◊„¡øµƒAgNO3»Ð“∫£¨≤˙…˙≥¡µÌ£ª
¢€Ω´≥¡µÌπ˝¬À°¢œ¥µ”°¢∏…‘Ôµ√µΩ∞◊…´πÃÃÂ17.22 g°£
µ—È2
¢Ÿ≥∆»°”Î µ—È1÷–œýÕ¨÷ ¡øµƒ—˘∆∑£¨Ω´—˘∆∑»ÐΩ‚£ª
¢⁄œÚ»ÐΩ‚∫Ûµƒ»Ð“∫÷–£¨Õ®»Î◊„¡øµƒCl2£ª
¢€‘ŸœÚ¢⁄À˘µ√»Ð“∫÷–º”»Î◊„¡øµƒNaOH»Ð“∫£¨µ√µΩ∫Ï∫÷…´≥¡µÌ£ª
¢ÐΩ´≥¡µÌπ˝¬À°¢œ¥µ”∫Û£¨º”»»◊∆…’£¨µΩ÷ ¡ø≤ª‘Ÿºı…Ÿ£¨µ√µΩπÃÃÂŒÔ÷ 4 g°£
∏˘æ𠵗Ȫÿ¥œ¬¡–Œ £∫
£®1£©»ÐΩ‚π˝≥Ã÷–À˘”√µΩµƒ≤£¡ß“«∆˜”–_____________________________°£
£®2£© µ—È “±£¥ÊFeCl2»Ð“∫ ±Õ®≥£ª·œÚ∆‰÷–º”»Î…Ÿ¡ø ‘º¡______________∫Õ____________°£
£®3£© µ—È2Õ®»Î◊„¡øCl2µƒƒøµƒ «________________________________£ª…ʺ∞µƒªØ—ß∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «______________________________°£
£®4£©ºÏ—È µ—È2µƒ≤Ω÷Ë¢Ð÷–≥¡µÌ“—æ≠œ¥µ”∏…檵ƒ∑Ω∑® «_________________________°£
£®5£©º”»»FeCl3»Ð“∫£¨≤¢Ω´»Ð“∫’Ù∏… ±£¨Õ®≥£≤ªƒÐµ√µΩFeCl3πÃ㨫Γ‘∆Ω∫‚µƒπ€µ„Ω‚ Õ∆‰‘≠“Ú£®∑Ω≥Ã Ω”ÎŒƒ◊÷œýΩ·∫œ¿¥Àµ√˜£©°£________________________________________________°£
£®6£©FeCl3»Ð“∫ø…“‘”√”⁄÷𗙣¨÷˜“™ «“ÚŒ™FeCl3»Ð“∫ƒÐ π—™“∫æ€≥¡£¨’‚…ʺ∞Ω∫õƒÃÿ–‘°£“‘œ¬πÿ”⁄Ω∫õƒÀµ∑®≤ª’˝»∑µƒ «________________°£
A.Ω∫á£◊”ƒÐÕ∏π˝¬À÷Ω£¨µ´≤ªƒÐÕ∏π˝∞ÎÕ∏ƒ§
B.Ω∫á£◊”æþ”–Ωœ¥Ûµƒ±Ì√ʪ˝£¨ƒÐŒ¸∏Ω—Ù¿Î◊”ªÚ“ı¿Î◊”£¨π ‘⁄µÁ≥°◊˜”√œ¬ª·≤˙…˙µÁ”æœ÷œÛ
C.÷ª”–Ω∫á£◊”ƒÐ◊ˆ≤º¿ ‘À∂Ø
D.œÚFe(OH)3Ω∫ÃÂ÷–µŒº”¡ÚÀ·£¨ª·œ»≥ˆœ÷∫Ï∫÷…´≥¡µÌ£¨ÀÊ∫Û≥¡µÌœ˚ ß
E.‘⁄µ∞∞◊÷ »Ð“∫÷–º”»Îœ°µƒCuSO4»Ð“∫,ø… πµ∞∞◊÷ —ŒŒˆ
£®7£©Õ®π˝ µ—ÈÀ˘µ√ ˝æ𣨺∆À„πÃע∆∑÷–FeCl3∫ÕFeCl2µƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™________________°£
£®8£©ø…“‘≤…”√œ¬¡–◊∞÷√÷∆»°…Ÿ¡øµƒFeCl3πÃ㨓—÷™FeCl3“◊≥±Ω‚°££®≤ø∑÷º–≥÷“«∆˜“—¬‘»•£©
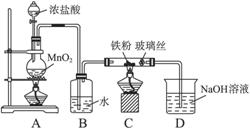
∏√◊∞÷√¥Ê‘⁄≤ª◊„£¨Õ˘Õ˘ŒÞ∑®µ√µΩFeCl3πÃ㨫΃„∂‘◊∞÷√÷≥ˆ∫œ¿Ìµƒ∏ƒΩ¯¥Î ©°£___________°£
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫≤ªœÍ –գ∫ µ—ÈÂ
| A£ÆΩ∫á£◊”ƒÐÕ∏π˝¬À÷Ω£¨µ´≤ªƒÐÕ∏π˝∞ÎÕ∏ƒ§ |
| B£ÆΩ∫á£◊”æþ”–Ωœ¥Ûµƒ±Ì√ʪ˝£¨ƒÐŒ¸∏Ω—Ù¿Î◊”ªÚ“ı¿Î◊”£¨π ‘⁄µÁ≥°◊˜”√œ¬ª·≤˙…˙µÁ”æœ÷œÛ |
| C£Æ÷ª”–Ω∫á£◊”ƒÐ◊ˆ≤º¿ ‘À∂Ø |
| D£ÆœÚFe(OH)3Ω∫ÃÂ÷–µŒº”¡ÚÀ·£¨ª·œ»≥ˆœ÷∫Ï∫÷…´≥¡µÌ£¨ÀÊ∫Û≥¡µÌœ˚ ß |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com