
如图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是( )
 |
科目:高中化学 来源: 题型:
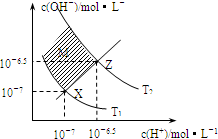
| A、图中T1>T2 | B、XZ线上任意点均有pH<7 | C、两条曲线间任意点均有c(H+)×c(OH-)=Kw | D、M区域内任意点对应的溶液中下列离子可以大量共存:Fe3+、Na+、Cl-、SO42- |
科目:高中化学 来源: 题型:单选题
如图表示溶液中c(H+)和c(OH-)的关系,下列判断正确的是
| A.图中T1>T2 |
| B.XZ线上任意点均有pH<7 |
| C.两条曲线间任意点均有c(H+)×c(OH-)=Kw |
| D.M区域内任意点对应的溶液中 |
科目:高中化学 来源:不详 题型:单选题
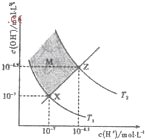
| A.两条曲线间任意点均有c(H+)×c(OH-)=Kw |
| B.M区域内任意点均有c(H+)<c(OH-) |
| C.图中T1<T2 |
| D.XZ线上任意点均有pH=7 |
科目:高中化学 来源:2013年全国统一高考化学试卷(大纲版)(解析版) 题型:选择题
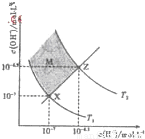
科目:高中化学 来源:不详 题型:单选题

| A.图中T1>T2 |
| B.XZ线上任意点均有pH<7 |
| C.两条曲线间任意点均有c(H+)×c(OH-)=Kw |
| D.M区域内任意点对应的溶液中 |
科目:高中化学 来源: 题型:
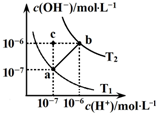
| A、ab线上任意点溶液均显中性 | B、b点时,溶液的pH=6,显酸性 | C、图中温度T1>T2 | D、在水中通入适量HCl气体可从a点变到c点 |
科目:高中化学 来源: 题型:填空题
(1) 25℃时,部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ki=1.7×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |

科目:高中化学 来源: 题型:
(1)已知下列热化学方程式:
① H2(g)+1/2O2(g) =H2O(g) ΔH=-241.8 kJ/mol
② C(s)+1/2O2(g) =CO(g) ΔH=-110.5 kJ/moL
则水煤气能源的制取原理:C(s)+H2O(g)=H2(g)+CO (g) ΔH= kJ/moL
(2)下图表示化学反应体系中反应物、产物的能量和活化能的关系,符合甲图的方程式为( )符合乙图的方程式为( )(填写“A”、“B”、“C”、“D”选项)

A.CO(g)+H2O(g)=CO2(g)+H2(g) B.H2(g)+I2(g)=2HI(g)
C.H+(aq)+OH-(aq)=H2O D.CaCO3(s)=CaO(s)+CO2(g)
 (3)如图所示,若两池中均为Cu(NO3)2溶液,甲、乙两池电极材料都是铁棒和石墨棒,反应一段时间后请回答下列问题:
(3)如图所示,若两池中均为Cu(NO3)2溶液,甲、乙两池电极材料都是铁棒和石墨棒,反应一段时间后请回答下列问题:
①有红色物质析出的是甲池中的______棒,乙池中的_______棒。
②乙池中阳极的电极反应式是___________________________。
(4)已知25℃时AgCl的溶度积为1.77×10-10,则在AgCl的饱和溶液中c(Ag+)为 。(已知![]() =1.33)
=1.33)
科目:高中化学 来源:不详 题型:填空题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ki=1.7×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com