
为使反应:Cu+2H2O═Cu(OH)2+H2↑能够发生,下列设计方案正确的是( )
|
科目:高中化学 来源:不详 题型:单选题
| A.用铜片做负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池 |
| B.用铜片做电极,外接直流电源电解硫酸铜溶液 |
| C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液 |
| D.用铜片作阴、阳电极,电解稀硫酸 |
科目:高中化学 来源:2010-2011学年浙江省金华市十校联考高一(下)期末化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:单选题
科目:高中化学 来源:2012-2013学年山东省高三上学期9月阶段性检测化学试卷(解析版) 题型:选择题
为使反应:Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是
A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池
B.用铜片作电极,外接直流电源电解硫酸铜溶液
C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液
D.用铜片作阴、阳电极,电解稀硫酸
科目:高中化学 来源:2013届山东省青岛二中高三上学期9月阶段性检测化学试卷(带解析) 题型:单选题
为使反应:Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是
| A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池 |
| B.用铜片作电极,外接直流电源电解硫酸铜溶液 |
| C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液 |
| D.用铜片作阴、阳电极,电解稀硫酸 |
科目:高中化学 来源:2015届广东省佛山市质量检测化学试卷(解析版) 题型:填空题
迄今为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
I.请仔细观察下列两种电池的构造示意图,完成下列问题:
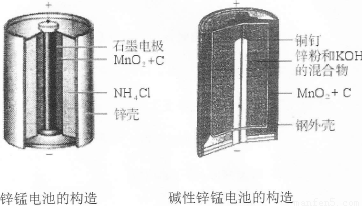
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是 。
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为 。
Ⅱ.下面是一个将化学能与电能相互转化的装置。回答下列问题:
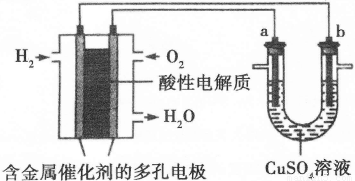
(1)写出通入O2一极的电极反应方程式为 。
(2)a电极是 极,能否写出其电极反应方程式 (填“能”或“不能”),若“能”写出其电极反应方程式,若“不能”说明其理由 。
(3)下列说法不正确的是( )
A.此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变
B.U型管中,OH—在a极放电
C.若a为纯净金属,b为粗制金属,该装置可用于粗制金属的精炼
D.电子经导线流入b电极
Ⅲ.某同学运用所学知识,自选材料设计实验,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑。请在下面框中画出能够实验这一反应的装置图,并在图中进行必要的标注。

科目:高中化学 来源: 题型:填空题
迄今为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
I.请仔细观察下列两种电池的构造示意图,完成下列问题: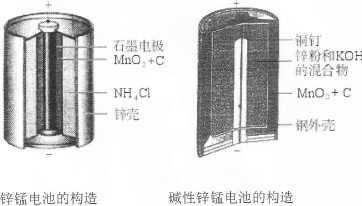
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是 。
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为 。
Ⅱ.下面是一个将化学能与电能相互转化的装置。回答下列问题: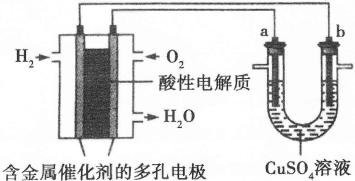
(1)写出通入O2一极的电极反应方程式为 。
(2)a电极是 极,能否写出其电极反应方程式 (填“能”或“不能”),若“能”写出其电极反应方程式,若“不能”说明其理由 。
(3)下列说法不正确的是( )
| A.此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变 |
| B.U型管中,OH—在a极放电 |
| C.若a为纯净金属,b为粗制金属,该装置可用于粗制金属的精炼 |
| D.电子经导线流入b电极 |

科目:高中化学 来源:不详 题型:填空题


| A.此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变 |
| B.U型管中,OH—在a极放电 |
| C.若a为纯净金属,b为粗制金属,该装置可用于粗制金属的精炼 |
| D.电子经导线流入b电极 |

科目:高中化学 来源: 题型:
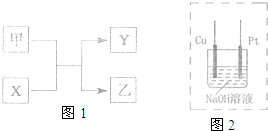 单质X、Y与化合物甲、乙有如图1所示的转化关系(必要的反应条件未标出),回答下列问题:
单质X、Y与化合物甲、乙有如图1所示的转化关系(必要的反应条件未标出),回答下列问题:湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com