
常温时,下列溶液的pH等于8或大于8的是( )
|
科目:高中化学 来源:2012年鲁科版高中化学选修4 3.1水溶液卷练习卷(解析版) 题型:选择题
常温时,下列溶液的pH等于8或大于8的是 ( )
A.0.1 mol·L-1的NaOH溶液滴定稀盐酸,用酚酞做指示剂滴定到终点
B.pH=6的醋酸用水稀释100倍
C.pH=10的氢氧化钠溶液稀释1000倍
D.0.1 mol·L-1的硫酸100 mL跟0.2 mol·L-1 NaOH溶液150 mL完全反应
科目:高中化学 来源:2010年湖北省高二上学期期中考试化学试卷 题型:选择题
常温时,下列溶液的pH等于8或大于8的是( )
A.0.1 mol/L的NaOH溶液滴定锥形瓶中的稀盐酸,用酚酞做指示剂滴定到终点
B.pH=6的醋酸用水稀释100倍
C.pH=10的氢氧化钠溶液稀释1000倍
D.0.1 mol/L的硫酸100 mL与0.1 mol/L NaOH溶液150 mL充分反应
科目:高中化学 来源:不详 题型:多选题
| A.0.1mol?L-1的NaOH溶液滴定稀盐酸,用酚酞做指示剂滴定到终点 |
| B.pH=6的醋酸用水稀释100倍 |
| C.pH=10的氢氧化钠溶液稀释1000倍 |
| D.0.1mol?L-1的硫酸100mL跟0.2mol?L-1NaOH溶液150mL完全反应 |
科目:高中化学 来源:2009-2010学年广东省中山一中高二(下)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:
常温时,下列溶液的pH等于8或大于8的是( )
A.0.1 mol/L的NaOH溶液滴定锥形瓶中的稀盐酸,用酚酞做指示剂滴定到终点
B.pH=6的醋酸用水稀释100倍
C.pH=10的氢氧化钠溶液稀释1000倍
D.0.1 mol/L的硫酸100 mL与0.1 mol/L NaOH溶液150 mL充分反应
科目:高中化学 来源: 题型:
常温时,下列溶液的pH等于8或大于8的是( )
A.0.1 mol/L的NaOH溶液滴定锥形瓶中的稀盐酸,用酚酞做指示剂滴定到终点
B.pH=6的醋酸用水稀释100倍
C.pH=10的氢氧化钠溶液稀释1000倍
D.0.1 mol/L的硫酸100 mL与0.1mol/L NaOH溶液150 mL充分反应
科目:高中化学 来源: 题型:
常温下,下列溶液的pH或微粒的物质的量浓度关系不正确的是 ( )
A.其他条件不变时,在0.1mol·L-1CH3COOH溶液中加水稀释,c(OH-)/c(CH3COOH)的值将增大
B.pH=3的二元弱酸H2R溶液和pH = 11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:2c(R2-)+c(HR-)=c(Na+)
C.pH=2的HA溶液与pH= 12的BOH溶液等体积混合后溶液pH等于8,则该碱溶液与pH=2的HCl溶液等体积混合时有:c(B+)=c(Cl-)>c(OH-)=c(H+)
D.0.1mol·L-1pH为5的NaHB溶液中:c(HB-)>c(B2-)>c(H2B)
科目:高中化学 来源: 题型:填空题
25 ℃时,有关物质的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平 衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K=3.0×10-8 |
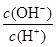
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题7电解质溶液练习卷(解析版) 题型:填空题
25 ℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平 衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K=3.0×10-8 |
回答下列问题。
(1)物质的量浓度为0.1 mol·L-1的下列四种物质,pH由大到小的顺序是________(填编号)。
a.Na2CO3 b.NaClO
c.CH3COONa d.NaHCO3
(2)常温下0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列各量一定变小的是________(填编号)。
A.c(H+) B.c(CH3COO-)
C.c(H+)·c(OH-) D.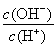
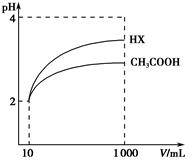
(3)体积均为10 mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1 000 mL,稀释过程中pH变化如图所示。则HX的电离平衡常数________(填“大于”、“等于”或“小于”)醋酸的电离平衡常数,理由是__________________;稀释后,HX溶液中水电离出来的c(H+)________(填“大于”、“等于”或“小于”)醋酸溶液中水电离出来的c(H+),理由是_________________________________________________________________。

(4)25 ℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中c(CH3COO-)-c(Na+)=________(填精确数值)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com