
为除去MgCl2酸性溶液中的Fe3+,不可以使用的试剂是(已知:Mg(OH)2的Ksp:5.6×10 -12,Fe(OH)3的Ksp:4.0×10 -38 )( )
|
科目:高中化学 来源: 题型:
科目:高中化学 来源:不详 题型:单选题
| A.NH3?H2O | B.MgO | C.Mg(OH)2 | D.MgCO3 |
科目:高中化学 来源:2012-2013学年湖南师大附中高二(上)期中化学试卷(解析版) 题型:选择题
科目:高中化学 来源: 题型:
为除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下,加入一种试剂,过滤后
再加入适量盐酸,这试剂不可以是
A.NH3·H2O B.MgO C.Mg(OH)2 D.MgCO3
科目:高中化学 来源:福建省福州市八中2011届高三年级上学期第一次月考试题化学试卷 题型:022
海水中蕴藏着丰富的资源,海水综合利用的流程图如下.
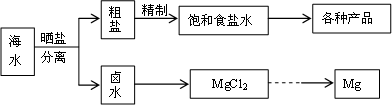
(1)用NaCl做原料可以得到多种产品.
①工业上由NaCl制备金属钠的化学方程式是________.
②实验室用惰性电极电解100 mL 0.1 mol/L NaCl溶液,若阴阳两极均得到112 mL气体(标准状况),则所得溶液的pH为________(忽略反应前后溶液的体积变化).
③电解氯化钠稀溶液可制备“84消毒液”,通电时产生的氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:________.
(2)分离出粗盐后的卤水中蕴含丰富的镁资源,经转化后可获得MgCl2粗产品.
①粗产品的溶液中含有Na+、Fe3+、Fe2+和Mn2+,需将Fe3+、Fe2+、Mn2+转化为沉淀除去;Fe(OH)2呈絮状,常将其转化为Fe(OH)3而除去(生成氢氧化物沉淀的pH见表).若只加入题(1)中得到的一种产品即可达到上述除杂目的,则该产品的化学式为________,最终控制溶液的pH值为________.

②在家用电热水器不锈钢内胆表面镶嵌镁棒,利用电化学原理来防止内胆腐蚀,写出正极的电极反应式:________.
(3)碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在.几种粒子之间有如下转化关系:
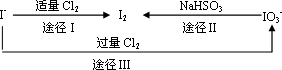
①如以途径Ⅰ制取I2,加的Cl2要适量,如过量就会发生途径Ⅲ的副反应,在该副反应产物中,IO3-与Cl-物质的量之比为1∶6,则氧化剂和还原剂物质的量之比为________.
②如以途径Ⅱ在溶液中制取I2,反应后的溶液显酸性,则反应的离子方程式是
________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com