
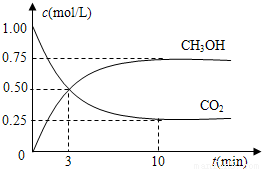
目前工业上有一种方法是用CO2来生产燃料甲醇.为探究其反应原理,现进行如下实验,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2 (g)+3H2 (g) CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )
 |
科目:高中化学 来源: 题型:
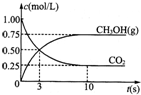 目前工业上有一种方法是用CO2来生产燃料甲醇.为探究其反应原理,现进行如下实验,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2 (g)+3H2 (g)
目前工业上有一种方法是用CO2来生产燃料甲醇.为探究其反应原理,现进行如下实验,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2 (g)+3H2 (g)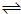 CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )
CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )科目:高中化学 来源: 题型:
 目前工业上有一种方法是用CO2来生产燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,为探究反应原理,现进行如下实验:
目前工业上有一种方法是用CO2来生产燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,为探究反应原理,现进行如下实验:| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
科目:高中化学 来源: 题型:
目前工业上有一种方法是用CO2来生产燃料甲醇。
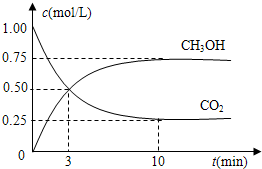
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
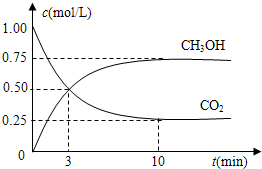
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1 mol CO2和4 mol H2
(4)如果在相同的容器中事先充入1 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
科目:高中化学 来源: 题型:
目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1 mol CO2和4 molH2
(4)如果在相同的容器中事先充入1 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
科目:高中化学 来源:2010-2011学年湖北省武汉市三角路中学高二上学期期末考试化学试卷 题型:填空题
目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g)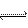 CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。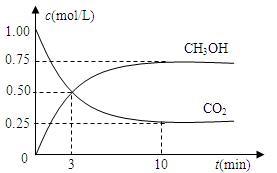
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1 mol CO2和4 mol H2 |
 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。科目:高中化学 来源:2012届湖北省武汉市高二上学期期末考试化学试卷 题型:填空题
目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
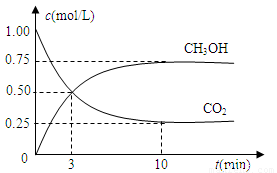
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1 mol CO2和4 mol H2
(4)如果在相同的容器中事先充入1 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
科目:高中化学 来源:不详 题型:单选题
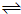
| A.2molCO2和6molH2反应达到平衡时放热73.5kJ |
| B.从反应开始到平衡,CO2的平均速率v(CO2)=0.0325mol/(L?S) |
| C.再充入1molCO2和3molH2,CO2的转化率不变 |
| D.反应进行到3S时v(正)=v(逆) |
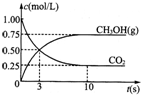
科目:高中化学 来源:2010-2011学年湖北省武汉市武昌区高二(上)期末化学试卷(解析版) 题型:解答题
科目:高中化学 来源:2011年四川省绵阳中学高考化学二模试卷(解析版) 题型:选择题
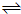 CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )
CH3OH(g)+H2O(g);△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )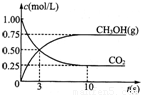
科目:高中化学 来源:不详 题型:问答题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com