
在恒温恒容下发生反应:N2(g)+3H2(g) 2NH3(g)△H<0.下列判断不正确的是( )
|
科目:高中化学 来源:不详 题型:单选题

| A.30s内,H2的浓度改变了0.30mol/L,则平均反应速率υ(N2)=0.01mol/(L?s) |
| B.当气体总压不随时间改变时,表明该反应达到平衡状态 |
| C.使用铁触媒可明显减少达到平衡的时间 |
| D.降温可提高N2的转化率 |
科目:高中化学 来源:2009-2010学年山东省聊城三中高三(上)月考化学试卷(12月份)(解析版) 题型:选择题
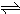 2NH3(g)△H<0.下列判断不正确的是( )
2NH3(g)△H<0.下列判断不正确的是( )科目:高中化学 来源:不详 题型:计算题
 2NH3(g);ΔH="-92.4" kJ·mol-1。请回答:
2NH3(g);ΔH="-92.4" kJ·mol-1。请回答: ,则N2的转化率a1= ,此时,反应放热 kJ;
,则N2的转化率a1= ,此时,反应放热 kJ;科目:高中化学 来源: 题型:
恒温恒压下,在一个容积可变的容器中发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
⑴若开始时放入1 molN2和3 mol H2,达到平衡后,生成a mol NH3,这时N2的物质的量为 mol。
⑵若开始时无NH3,只放入N2和H2,达到平衡时生成的NH3的物质的量为3a mol,则开始时放入N2和H2的物质的量分别为 mol和 mol 。[平衡时NH3的质量分数与⑴相同]
⑶若开始时放入x molN2和6mol H2和2mol NH3,达到平衡后,N2和NH3的物质的量分别为y mol和3a mol,则x= ,y= 。平衡时H2的物质的量 (选一个编号)。
A.大于6mol B.等于6mol
C.小于6mol D.可能大于、小于或等于6mol
作出判断的理由是 。
⑷若在⑶的平衡混合物中,再加入6mol NH3,再次达到平衡后,NH3的质量分数为
。
科目:高中化学 来源: 题型:
一定温度下,发生反应:N2(g)+3H2(g)![]() 2NH3(g)△H<0
2NH3(g)△H<0
(1)若在相同温度下,1mol N2和3mol H2 分别在恒压密闭容器A中和恒容密闭容器B中反应,开始时A、B的体积相同。则 容器中先达到平衡; 容器中的N2的转化率高
(2)当A中已达到平衡时,再加入1摩Ar,则N2的转化率 ;正反应速率会
(3)若B中反应达到平衡时,平衡混和物中N2、H2、NH3的物质的量分别为a、b、c摩。仍维持原温度,用x、y、z分别表示开始时N2、H2、NH3的加入量(mol),使达到平衡后N2、H2、NH3的物质的量也为a、b、c摩。则应满足的条件是:
①若x=0,y=0,则z=
②若x=0.75,则y应为 mol、z应为 mol。
③x、y、z应满足的一般条件是
科目:高中化学 来源:不详 题型:填空题
 2NH3(g)。
2NH3(g)。| A.大于6mol | B.等于6mol |
| C.小于6mol | D.可能大于、小于或等于6mol |
科目:高中化学 来源: 题型:
恒温恒压下在一个密闭容器中发生如下反应:N2(g)+3H2(g) ![]() 2NH3(g),若开始时放入1 mol N2 和3 mol H2达平衡时生成a mol NH3,若开始时放入x mol N2 y mol H2 和0.2 mol NH3,达到平衡状态时NH3的物质的量为0.5a mol,则x、y的值分别为 ( )
2NH3(g),若开始时放入1 mol N2 和3 mol H2达平衡时生成a mol NH3,若开始时放入x mol N2 y mol H2 和0.2 mol NH3,达到平衡状态时NH3的物质的量为0.5a mol,则x、y的值分别为 ( )
A.0.9、2.7 B.0.4、1.2 C.2、6 D.0.3、0.9
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
科目:高中化学 来源:2012-2013学年浙江省杭州二中高一下学期期中考试化学理科试卷(带解析) 题型:填空题
(1)在一个恒温恒容的密闭容器中,可逆反应N2(g)+3H2(g) 2NH3(g) △H<0达到平衡的标志是__________________________(填编号)
2NH3(g) △H<0达到平衡的标志是__________________________(填编号)
①反应速率v(N2):v(H2):v(NH3) =" 1" : 3 : 2 ②各组分的物质的量浓度不再改变
③体系的压强不再发生变化 ④混合气体的密度不变
⑤单位时间内生成n mol N2的同时,生成3n mol H2
⑥2V(N2正)= V(NH3逆)
⑦单位时间内3 mol H—H键断裂的同时2 mol N—H键也断裂
⑧混合气体的平均相对分子质量不再改变
(2) 现有八种物质:①干冰;②金刚石;③四氯化碳;④晶体硅;⑤过氧化钠;⑥二氧化硅晶体;⑦溴化铵;⑧氖。请用编号填写下列空白:
A.属于原子晶体的是_____________ ,其中熔点最高的是____________
B.属于分子晶体的是_____________________,其中分子构型为直线型的是____________ ,其电子式为_________________
C.含有非极性键的离子化合物是_______________,其中阳离子个数与阴离子个数之比为_________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com