
T℃下,在容积为2L的密闭容器中发生反应CO(g)+H2O(g)?CO2(g)+H2O(g),部分数据见下表(表中t2>t1):
|
科目:高中化学 来源:不详 题型:单选题
| 反应时间/min | N(CO)/mol | H2O/mol | N(CO2)/mol | N(H2)/mol |
| 0 | 1.20 | 0.60 | 0 | 0 |
| t1 | 0.80 | |||
| t2 | 0.20 |
A.反应在t1min内的平均速率为v(H2)=
| ||
| B.平衡时CO的转化率为66.67% | ||
| C.该温度下反应的平衡常数为1 | ||
| D.其他条件不变,若起始时n(C0)=0.60 mol,n(H20)=1.20 mol,则平衡时n(C02)=0.20 mol |
科目:高中化学 来源:2011-2012学年浙江省温州市苍南县七校联考高二(下)期中化学试卷(解析版) 题型:选择题
| 反应时间/min | N(CO)/mol | H2O/mol | N(CO2)/mol | N(H2)/mol |
| 1.20 | 0.60 | |||
| t1 | 0.80 | |||
| t2 | 0.20 |
 mol?L-1?min-1
mol?L-1?min-1科目:高中化学 来源: 题型:
(2012?郑州一模)T℃下,在容积为2L的密闭容器中发生反应CO(g)+H2O(g)?CO2(g)+H2O(g),部分数据见下表(表中t2>t1):
|
科目:高中化学 来源: 题型:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
| c(CO) |
| c(CO2) |
| c(CO) |
| c(CO2) |

 ).
).科目:高中化学 来源: 题型:
反应① Fe(s)+CO2(g)===FeO(s)+CO(g);△H1= a kJmol-1
反应② CO(g)+1/2O2(g)===CO2(g);△H2= b kJmol-1
测得在不同温度下,在密闭容器中进行的反应①的平衡常数K值随温度的变化如下:
![]()
(1)反应①的化学平衡常数表达式为 ,a 0(填“>”、“<”或“=”)。 在 500℃2L 密闭容器中进行反应①,Fe 和 CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为 ,用CO表示的化学反应速率为 。
(2)700℃反应①到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有 (填序号)。
A.缩小反应器体积 B.通入CO2 C.升高温度到900℃ D.使用合适的催化剂
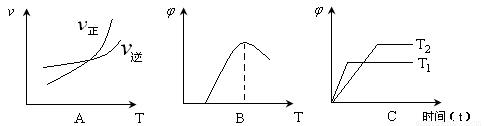
(3)下列图像符合反应①的是 (填序号)(图中v是速率、![]() 为混合物中CO的含量,T为温度)。
为混合物中CO的含量,T为温度)。
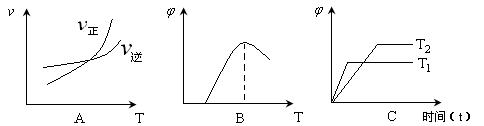
(4)由反应①和②可求得反应2Fe(s)+O2(g)===2FeO(s) △H3中的△H3= (用含a、b的代数式表示)。
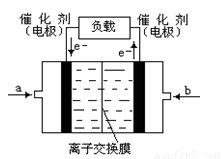
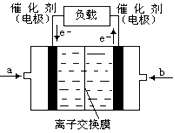
(5)如下图是甲醇燃料电池(电解质溶液为KOH溶液)的结示意图,则a处通入的是
(填“甲醇”或“氧气”),b处电极上发生的电极反应是:
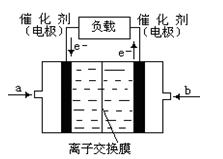
科目:高中化学 来源: 题型:
反应① Fe(s)+CO2(g)===FeO(s)+CO(g);△H1= akJmol-1
反应② CO(g)+1/2O2(g)===CO2(g);△H2= bkJmol-1
测得在不同温度下,在密闭容器中进行的反应①的平衡常数K值随温度的变化如下:
(1)反应①的化学平衡常数表达式为 ,a 0(填“>”、“<”或“=”)。 在500℃2L 密闭容器中进行反应①,Fe 和 CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为 ,用CO表示的化学反应速率为 。
(2)700℃反应①到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有 (填序号)。
A.缩小反应器体积 B.通入CO2 C.升高温度到900℃ D.使用合适的催化剂
(3)下列图像符合反应①的是 (填序号)(图中v是速率、为混合物中CO的含量,T为温度)。
(4)由反应①和②可求得反应2Fe(s)+O2(g)===2FeO(s) △H3中的△H3= (用含a、b的代数式表示)。
(5)如下图是甲醇燃料电池(电解质溶液为KOH溶液)的结示意图,则a处通入的是
(填“甲醇”或“氧气”),b处电极上发生的电极反应是:
科目:高中化学 来源:2011届河南省许昌市三校高三上学期期末考试(理综)化学部分 题型:填空题
反应① Fe(s)+CO2(g)===FeO(s)+CO(g);△H1=" a" kJmol-1
反应② CO(g)+1/2O2(g)===CO2(g);△H2=" b" kJmol-1
测得在不同温度下,在密闭容器中进行的反应①的平衡常数K值随温度的变化如下:
(1)反应①的化学平衡常数表达式为 ,a 0(填“> ”、“<”或“="”)。" 在 500℃2L 密闭容器中进行反应①,Fe 和 CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为 ,用CO表示的化学反应速率为 。
”、“<”或“="”)。" 在 500℃2L 密闭容器中进行反应①,Fe 和 CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为 ,用CO表示的化学反应速率为 。
(2)700℃反应①到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有 (填序号)。
| A.缩小反应器体积 | B.通入CO2 | C.升高温度到900℃ | D.使用合适的催化剂 |
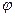 为混合物中CO的含量,T为温度)。
为混合物中CO的含量,T为温度)。

科目:高中化学 来源:2010-2011学年河南省许昌市三校高三上学期期末考试(理综)化学部分 题型:填空题
反应① Fe(s)+CO2(g)===FeO(s)+CO(g);△H1= a kJmol-1
反应② CO(g)+1/2O2(g)===CO2(g);△H2= b kJmol-1
测得在不同温度下,在密闭容器中进行的反应①的平衡常数K值随温度的变化如下:

(1)反应①的化学平衡常数表达式为 ,a 0(填“>”、“<”或“=”)。 在 500℃2L 密闭容器中进行反应①,Fe 和 CO2的起始物质的量均为4mol,10min后达到平衡状态,平衡时CO2的转化率为 ,用CO表示的化学反应速率为 。
(2)700℃反应①到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有 (填序号)。
A.缩小反应器体积 B.通入CO2 C.升高温度到900℃ D.使用合适的催化剂
(3)下列图像符合反应①的是
(填序号)(图中v是速率、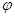 为混合物中CO的含量,T为温度)。
为混合物中CO的含量,T为温度)。
(4)由反应①和②可求得反应2Fe(s)+O2(g)===2FeO(s) △H3中的△H3= (用含a、b的代数式表示)。
(5)如下图是甲醇燃料电池(电解质溶液为KOH溶液)的结示意图,则a处通入的是
(填“甲醇”或“氧气”),b处电极上发生的电极反应是:
科目:高中化学 来源: 题型:单选题
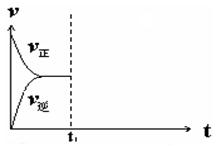
Ⅰ.800℃时,向容积为2L的恒容密闭容器中充入一定量的CO和H2O维持恒温,发生反应CO(g)+H2O(g) H2(g)+CO2(g),反应过程中测定的部分数据见下表:
H2(g)+CO2(g),反应过程中测定的部分数据见下表:
| 反应时间/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | | 0.80 |
| n(H2O)/ mol | 0.60 | | 0.20 | |
| 组别 | 药品1 | 药品2 | 实验现象 |
| I | 0.01 mol/L NaOH溶液 | 0.01 mol/L MgCl2溶液 | 生成白色沉淀 |
| II | 0.01 mol/L氨水 | 0.01 mol/L MgCl2溶液 | 无现象 |
| III | 0.1 mol/L氨水 | 0.1 mol/L MgCl2溶液 | 现象III |
| IV | 0.1 mol/L氨水 | 0.01 mol/L MgCl2溶液 | 生成白色沉淀 |
| V | 0.01 mol/L氨水 | 0.1 mol/L MgCl2溶液 | 无现象 |
 2NH4+(aq) + Mg(OH)2(s)该反应化学平衡常数的表达式为K= ,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式 。
2NH4+(aq) + Mg(OH)2(s)该反应化学平衡常数的表达式为K= ,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式 。科目:高中化学 来源:模拟题 题型:单选题

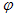 为混合物中CO的含量,T为温度)。
为混合物中CO的含量,T为温度)。 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com