
分别将下列各组内的三种物质同时放入水中,只得到无色透明溶液的是( )
|
科目:初中化学 来源:不详 题型:单选题
| A.FeCl3、KOH、NaCl | B.K2SO4、HCl、BaCl2 |
| C.CuSO4、HCl、KCl | D.Na2SO、Na2CO3、NaNO3 |
科目:初中化学 来源:2004年湖北省黄冈市中考化学模拟试卷(解析版) 题型:选择题
科目:初中化学 来源: 题型:单选题
科目:初中化学 来源:新课标读想用 九年级化学 下 题型:013
分别将下列各组内的三种物质同时放入水中,只得到无色透明溶液的是
[ ]
A.FeCl3、KOH、NaCl
B.K2SO4、HCl、BaCl2
C.CuSO4、HCl、KCl
D.Na2SO4、Na2CO3、NaNO3
科目:初中化学 来源: 题型:阅读理解
| 猜想 | 可行的实验方案 | 观察到的实验现象 |
| 猜想① | 将一小块果肉浸入盛有蒸馏水的烧杯中,观察现象. | 果肉表面不变色 |
| 猜想② | 将切开的苹果放入盛有氧气的集气瓶中,观察现象 |
果肉表面变色 |
| 猜想③ | 将切开的苹果放入盛有氮气的集气瓶中,观察现象. | 果肉表面不变色 |
| 猜想④ | 各取一小块苹果分别放入两支集满氧气的试管中,将其中一支试管放入热水中,观察两试管中苹果的变色速度 |
温度高的先变色 |
科目:初中化学 来源:2009年江苏省连云港市高中段学校招生统一文化考试化学试卷 题型:022
NaNO2(亚硝酸钠)、NaCl和物质M(不含结晶水)的溶解度曲线如图所示,请根据图像和有关信息回答下列问题:

(1)t2℃时,NaNO2、NaCl和M的溶解度由大到小的顺序是________.
(2)如图所示,当往试管中加入5 mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发).请判断:该饱和溶液中的溶质是NaNO2、NaCl和M中的________.
(3)分别将NaNO2、NaCl和M的饱和溶液从t2℃降温到t1℃时,三种溶液中溶质的质量分数由大到小的顺序是________.
(4)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故.为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息:NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271℃,NaCl熔点为801℃.
①小明同学设计的鉴别实验方案如下:
20℃时分别取NaNO2、NaCl各5.0 g于两只小烧杯中,分别加入10 mL水(水的密度近似看作1 g/cm3),用玻璃棒充分搅拌后观察.你认为此方案是否可行________(填“可行”或“不可行”).
②该小组其他同学又设计出与小明不同的实验方案,并获得成功.你认为该方案可能是________(只填写一种方案并简单叙述).
科目:初中化学 来源:江苏中考真题 题型:填空题

科目:初中化学 来源: 题型:
NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图24-1所示,请根据图像和有关信息回答下列问题:
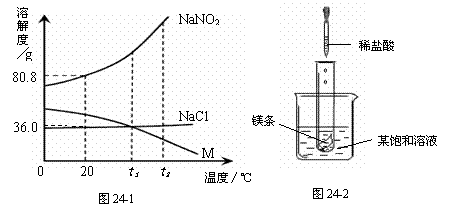 |
(1)t2 ℃时,NaNO2、NaCl和M的溶解度由大到小的顺序是 。
(2)如图24-2所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发)。请判断:该饱和溶液中的溶质是NaNO2、NaCl和M中的 。
(3)分别将NaNO2、NaCl和M的饱和溶液从t2℃降温到t1℃时,三种溶液中溶质的质量分数由大到小的顺序是 。
(4)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故。为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息: NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271 ℃,NaCl熔点为801 ℃。
① 小明同学设计的鉴别实验方案如下:
20℃时分别取NaNO2、NaCl各5.0g于两只小烧杯中,分别加入10mL水(水的密度近似看作1g/cm3),用玻璃棒充分搅拌后观察。你认为此方案是否可行 (填“可行”或“不可行”)。
② 该小组其他同学又设计出与小明不同的实验方案,并获得成功。你认为该方案可能是 (只填写一种方案并简单叙述)。
科目:初中化学 来源: 题型:解答题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com